Электролитическая диссоциация. Механизм растворения в воде веществ с ионной связью. Степень диссоциации. Сильные электролиты.
Электролитическая диссоциация- это процесс распада электролита на ионы при растворении его в воде или расплавлении.
Электролиты– это вещества, водные растворы или расплавы которых проводят электрический ток.
Неэлектролиты – это вещества, водные растворы или расплавы которых не проводят электрический ток.

Механизм растворения в воде кристалла NaCl:
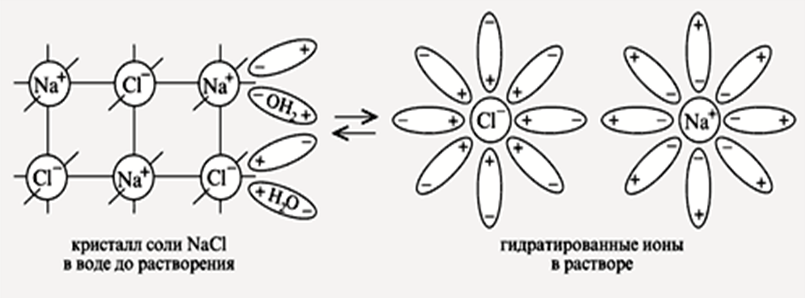
Степень диссоциации (α)– отношение числа распавшихся на ионы молекул (n) к общему числу растворенных молекул (N):


n –число диссоциированных молекул
N –общее число молекул
| Электролиты | |
| сильные | слабые |
| α > 30% | α < 3% |
| 1. Растворимые соли; 2. Сильные кислоты (НСl, HBr, HI, НNО3, НClO4, Н2SO4(разб.)); 3. Сильные основания – щёлочи. | 1. Почти все органические кислоты (CH3COOH- уксусная и др.); 2. Некоторые неорганические кислоты (H2CO3, H2S и др.); 3. Почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH); 4. Вода. |
Кислоты и их химические свойства.
Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка.
Классификация кислот.
1) По содержанию кислорода:
| Кислоты | |
| Бескислородные | Кислородсодержащие |
| HF | HNO3 |
| H2S | H3PO4 |
По количеству кислорода
| Кислоты | ||
| Одноосновные | Двухоосновные | Трехосновные |
| HCl | H2S | H3PO4 |
| HNO3 | H2SO4 | |
По растворимости в воде
| Кислоты | |
| Нерастворимые | Растворимые |
| H2SiO3 | Все остальные |
По стабильности
| Кислоты | |
| Стабильные | Нестабильные |
| HCl | H2SO3 |
| H2SO4 | H2SiO3 |
| H3PO4 | H2CO3 |
Химические свойства.
Действие их на индикаторы.
Индикаторы - вещества, изменяющие окраску в зависимости от среды – кислотной или щелочной (лакмус, метилоранж, фенолфталеин).
В кислотах:
| Лакмус | Метилоранж | Фенолфталеин |
| красный | розовый | бесцветный |
Диссоциация кислот.
1) HCl ↔ Н+ + Cl-
| Н+ определяют кислую среду раствора. |
2) H2SO4 ↔ 2Н+ + SO42-
3) H3PO4 ↔ 3Н+ + PO43-
Кислоты взаимодействуют с металлами, оксидами металлов, основаниями и солями. Во всех случаях основным продуктом реакции будет соль.

Взаимодействие кислот с металлами.
Если металл находится в ряду активности до водорода, то он реагирует с кислотами, если после, то – нет.

Zn + 2HCl = ZnCl2 + H2↑ (реакция замещения)
Fe + 2HCl = FeCl2 + H2↑ (реакция замещения)
Cu + HCl ≠
Взаимодействие кислот с оксидами металлов.
CuO + H2SO4 = CuSO4 + H2O (реакция обмена)
| реакция нейтрализации |
NaOH + HCl = NaCl + H2O (реакция обмена)
Cu(OH)2 + 2HCl = CuCl2 + 2H2O (реакция обмена)
Взаимодействие кислот с солями.
BaCl2 + H2SO4 = BaSO4↓ + 2HCl (реакция обмена)
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑ (реакция обмена)
Основания и их химические свойства.
Основания- сложные вещества, которые состоят из ионов металла или иона аммония и гидроксогруппы (-ОН). Хорошо растворимые в воде основания называются щелочами.
Общая формула оснований Ме(ОН)n
где n – число ОН- групп, численно равное значению заряда иона (степени окисления) металла.
+1 +2 +3
NaOH, Ca(OH)2, Fe(OH)3.
Названия оснований состоят из слова "гидроксид" и наименования металла в родительном падеже:
NaOH - гидроксид натрия
Са(ОН)2 - гидроксид кальция.
Если металл проявляет переменную степень окисления, то ее величину указывают римской цифрой в скобках и произносят в конце названия основания:
CuOH - гидроксид меди (I) (читают "гидроксид меди один)
Cu(OH)2 - гидроксид меди (II) (читают "гидроксид меди два)
Классификация.
По растворимости в воде.
| Основания | |
| Растворимые | Нерастворимые |
| NaOH, КОН, Ba(OH)2 | Cr(OH)2, Mn(OH)2, Fe(OH)3 |
Химические свойства.
Действие индикаторов.
Индикаторы- вещества, изменяющие цвет в зависимости от среды.
В щелочах:
| Лакмус | Метилоранж | Фенолфталеин |
| синий | желтый | малиновый |
Нерастворимые основания в воде не растворяются и окраску индикаторов не изменяют.
Диссоциация оснований.
| OH- определяют щелочную среду раствора. |
2) Ba(OH)2 ↔ Ba2+ + 2OH-
Взаимодействие с кислотами.
NaOH + HCl = NaCl + H2O (реакция нейтрализации - взаимодействие щелочей с кислотами)
3. Взаимодействие щелочей с кислотными оксидами:
2NaOH + SO3 = Na2SO4 + H2O
Ca(OH)2 + CO2 = CaCO3↓ + H2O
3. Разложение нерастворимых оснований при нагревании:
t
Cu(OH)2 = CuO + H2O
Дата добавления: 2018-05-13; просмотров: 1437; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
