Реакция на гликоли и многоатомные спирты.
Nbsp;
ЛАБОРАТОРНАЯ РАБОТА № 2
Функциональный анализ кислородсодержащих органических соединений.
Цель работы:Познакомиться с качественными реакциями спиртов, фенолов, карбонильных соединений, карбоновых кислот, установить формулу неизвестного вещества на основе функциональногоанализа и данных количественного элементного состава.
Часть 1. Качественные реакции кислородсодержащих органических соединений.
Опыт 1.Качественные реакции спиртов.
Спирты – производные углеводородов, в молекулах которых гидроксильная группа образует σ-связь с sp3-гибридизованной орбиталью атома углерода.
Существуют (в зависимости от характера углеводородного радикала) алифатические спирты (предельные и непредельные: например, метиловый, этиловый спирты) и ароматические спирты (например, бензиловый).

Спирты могут быть первичными, вторичными, третичными, в зависимости от того, с каким атомом углерода связана гидроксильная группа.
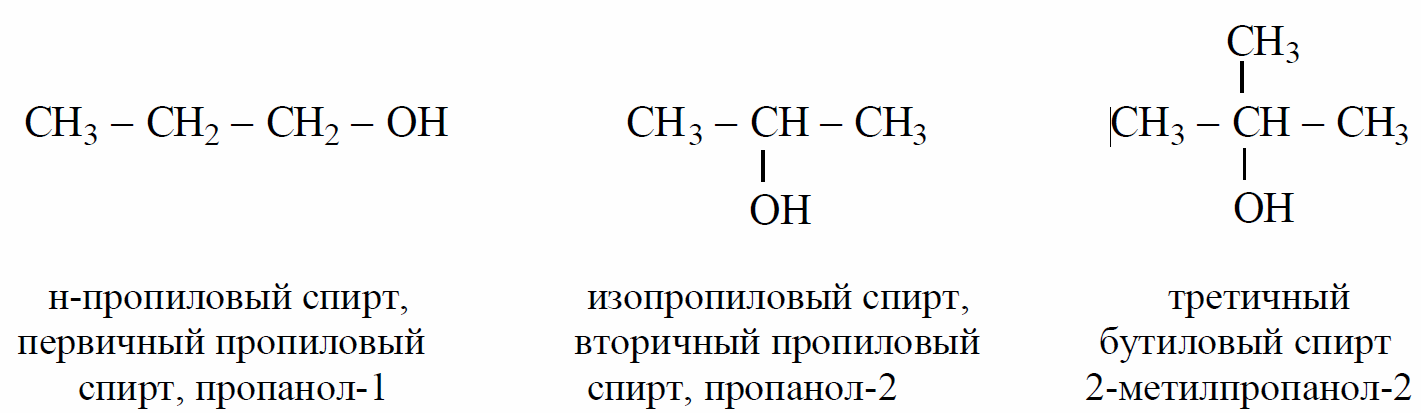
Название спиртов по заместительной номенклатуре ИЮПАК состоят из названия соответствующего углеводорода, суффикса –ол и цифры, указывающей положение гидроксигруппы.
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами –диол (две ОН-группы), -триол (три ОН-группы) и т.д.
|
|
|
Химические свойства спиртов определяются электронным строением молекулы и характером ковалентной связи.
Все многочисленные реакции спиртов можно разделить на три группы:
- реакции, идущие с участием атома водорода гидроксильной группы (отщепление протона – кислотные свойства);
- реакции, происходящие с замещением или отщеплением гидроксильной группы;
- реакции, затрагивающие углеводородный радикал, в том числе реакции окисления.
Спирты обладают слабокислотными свойствами, в меньшей степени, чем у воды (для воды рКа = 15,7, для этилового спирта – рКа = 16,0) и поэтому окраска индикаторов не подтверждает кислую среду в спирте.
Спирты не взаимодействуют с водными растворами щелочей, но реагируют с щелочными металлами образуя алкоголяты, легко разлагающиеся водой. С карбоновыми кислотами спирты образуют сложные эфиры (реакция этерификации).
Спирты можно рассматривать как очень слабые основания, так как они могут протонизироваться за счет неподеленной электронной пары атома кислорода с образованием непрочного оксониевого катиона.
Реакции замещения гидроксильной группы на галоген (нуклеофильное замещение SN) и отщепления группы – ОН в реакциях дегидратации (внутримолекулярной или межмолекулярной), как и реакции дегидрирования и окисления приводят к получению продуктов в зависимости от характера спирта (первичного, вторичного или третичного). Большинство полиатомных спиртов, содержащих оксигруппы у соседних атомов углерода, образуют растворимые в воде и окрашенные в ярко-синий цвет хелатные комплексы с ионами меди (II). Эти комплексы устойчивы в щелочной среде, но разлагаются на исходные соединения в кислой среде.
|
|
|
Для доказательства присутсвия гидроксильной группы лучше всего использовать ИК-спектроскопию. Химические методы малослективны и позволяют в основном приблизительно установить строение спиртов.
1.1.Окисление спиртов оксидом меди (II) В пламени спиртовки сильно прокаливают медную проволоку,имеющую на конце петлю. Затем опускают ее в пробирку с 1 мл этанола. Вопросы и задания1. Какого цвета становится медная проволока после прокаливания? Почему? Напишите уравнение реакции.2. Какого цвета становится проволока после ее опускания в этанол? Появляется ли запах? Какому веществу он соответствует? Свои рассуждения подтвердите уравнениями реакций.3. Как еще можно доказать основной продукт окисления этанола? Проведите дополнительный качественный анализ. 1.2.Окисление спирта сильными окислителями В пробирку наливают 2–3 капли раствора серной кислоты, 0,5 млраствора перманганата калия (или бихромата калия) и столько же этилового спирта. Содержимое пробирок осторожно нагревают на водяной бане до изменения окраски. Вопросы и задания1. Составьте уравнение реакции.2. Что происходит с окраской раствора? Отметьте характерный запах образующегося вещества (какого?)Реакция на гликоли и многоатомные спирты.
|
|
|
В пробирку наливают 1мл 3% раствора CuSO4 и несколько капель 5% раствора NaOH до выпадения голубого осадка гидроксида меди(II). К смеси быстро прибавляют три капли раствора глицерина. Повторяют опыт с раствором глюкозы.
Вопросы и задания1. Запишите наблюдения.
2. Составьте уравнения реакций.
Дата добавления: 2018-05-12; просмотров: 655; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
