Составление уравнения зависимости от температуры величины теплового эффекта и изменения энтропии
Зависимость теплового эффекта реакции от температуры определяется законом Кирхгофа (1):

Рассчитаем  по уравнению (2):
по уравнению (2):
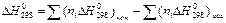

Рассчитаем  :
:


Рассчитаем 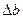 :
:


Рассчитаем  :
:


Рассчитаем  :
:

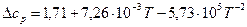
Найдем тепловой эффект по уравнению (1):

Уравнение зависимости от температуры величины теплового эффекта:

Составим теперь уравнение зависимости от температуры изменения энтропии.
Изменение энтропии системы в результате протекания процесса определяется по уравнению (7)

Рассчитаем  по уравнению (8):
по уравнению (8):

Значения  для соответствующих веществ приведены в таблице 2, после их подстановки получим:
для соответствующих веществ приведены в таблице 2, после их подстановки получим:

Найдем изменение энтропии системы по уравнению (7):

Уравнение зависимости от температуры изменения энтропии:

2. Вычисление величин 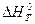 ,
,  ,
,  и
и  при различных температурах и построение графиков в координатах
при различных температурах и построение графиков в координатах  ;
; 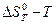 ;
;  и
и 
Определение теплового эффекта реакции при различных
температурах


Рассчитаем по аналогии тепловой эффект реакции для других температур заданного интервала (300 – 750 К) и данные занесем в таблицу 3.
Таблица 3
Величина 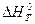 при различных температурах для реакции:
при различных температурах для реакции: 
| T, K | |||||

| -108975 | -109045 | -109028 | -108947 | -108817 |
| Т, К | |||||

| -108645 | -108437 | -108198 | -107931 | -107637 |
По данным таблицы 3 построим график  (рис.1)
(рис.1)

Рис.1 Зависимость теплового эффекта реакции
 от температуры
от температуры
Определение изменения энтропии при различных
температурах
|
|
|


Рассчитаем по аналогии изменение энтропии для других температур заданного интервала (300 – 750 К) и данные занесем в таблицу 4.
Таблица 4
Значения изменения энтропии  при различных
при различных
температурах
| Т, К | |||||

| -136,91 | -137,13 | -137,08 | -136,89 | -136,62 |
| Т, К | |||||

| -136,29 | -135,93 | -135,55 | -135,15 | -134,75 |
По данным таблицы 4 построим график  (рис.2)
(рис.2)

Рис.2 Зависимость изменения энтропии от температуры для реакции

Расчет изменения стандартной энергии Гиббса
При расчете изменения стандартной энергии Гиббса для реакции воспользуемся уравнением Гиббса- Гельмгольца(9):


Рассчитаем по аналогии изменение стандартной энергии Гиббса для других температур заданного интервала (300 - 750К) и данные занесем в табл.5
Таблица 5
Значения изменения стандартной энергии Гиббса ( ) при различных температурах
) при различных температурах
| Т, К | |||||

| - 67903 | -61051 | -54195 | - 47345 | - 40507 |
| Т, К | |||||

| - 33684 | - 26878 | -20091 | -13324 | -6576 |
По данным таблицы 5 построим график  (рис.3)
(рис.3)
Расчет константы равновесия
Константа равновесия связана с изменением стандартной энергии Гиббса соотношением (10):


Рассчитаем по аналогии  для других температур заданного интервала (300 - 750К) и данные занесем в табл.6.
для других температур заданного интервала (300 - 750К) и данные занесем в табл.6.
|
|
|
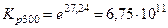

Рис.3 Зависимость изменения Стандартной энергии Гиббса от температуры для реакции 
Таблица 6
Константы равновесия для реакции
 при различных температурах
при различных температурах
| Т, К | |||||

| 3,33 | 2,86 | 2,50 | 2,22 | 2,00 |

| 27,24 | 20,99 | 16,30 | 12,66 | 9,75 |

| 6,75∙1011 | 1,31∙109 | 1,20∙107 | 3,15∙105 | 1,71∙104 |
| Т, К | |||||

| 1,82 | 1,67 | 1,54 | 1,43 | 1,33 |

| 7,37 | 5,39 | 3,72 | 2,29 | 1,05 |

| 1,59∙103 | 2,19∙102 | 4,13∙10 | 9,88 | 2,87 |
Реакции, для которых значения константы равновесия находятся в пределах от10-3 до 103 (10-3 < Kp < 103) принято считать практически обратимыми. Уменьшение Кр с ростом температуры означает, что равновесие реакции при этом сдвигается справа налево.
При 650 Креакция  обратимая.
обратимая.
По данным табл.6 построим график  (рис.4).
(рис.4).

Рис.4 Зависимость  от обратной температуры для реакции
от обратной температуры для реакции 
Дата добавления: 2015-12-21; просмотров: 26; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
