Теоретические основы
Согласно заданию необходимо составить уравнение зависимости от температуры величины теплового эффекта и изменения энтропии, а также вычислить величины,, и при нескольких температурах.
Зависимость теплового эффекта реакции от температуры
определяется законом Кирхгофа:


где  - стандартный тепловой эффект реакции при 298К;
- стандартный тепловой эффект реакции при 298К;
 - изменение теплоемкости системы в результате протекания реакции.
- изменение теплоемкости системы в результате протекания реакции.
 Значение
Значение  определяется по закону Гесса:
определяется по закону Гесса:

Стандартные тепловые эффекты  для соответствующих веществ приведены в колонке 2 приложения 4.
для соответствующих веществ приведены в колонке 2 приложения 4.
Изменение теплоемкости  рассчитывается по уравнению:
рассчитывается по уравнению:


где 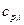 - мольная изобарная теплоемкость i -гo вещества;
- мольная изобарная теплоемкость i -гo вещества;
 - стехиометрический коэффициент i -го вещества в уравнении реакции.
- стехиометрический коэффициент i -го вещества в уравнении реакции.
Теплоемкость зависит от температуры по уравнению:


где а,b,с' - эмпирические коэффициенты.
В результате реакции теплоемкость изменяется, и разность теплоемкостей определяется по уравнению:


где 



Коэффициенты а,b,с' приводятся в колонках 4,5,6 приложения 5.
Изменение энтропии системы в результате протекания процесса определяется по уравнению:
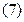

где  - стандартное изменение энтропии для реакции при 298К.
- стандартное изменение энтропии для реакции при 298К.
Его можно определить по мольным стандартным энтропиям веществ  :
:


Значения  для соответствующих веществ приведены в колонке 3 приложения 5.
для соответствующих веществ приведены в колонке 3 приложения 5.
 При расчете изменения стандартной энергии Гиббса для реакции необходимо воспользоваться уравнением Гиббса - Гельмгольца:
При расчете изменения стандартной энергии Гиббса для реакции необходимо воспользоваться уравнением Гиббса - Гельмгольца:
|
|
|
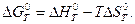
Константа равновесия связана с изменением стандартной энергии Гиббса соотношением:


где R - универсальная газовая постоянная, равная 
Т - абсолютная температура, К.
Далее необходимо определить количество фаз, независимых компонентов и число степеней свободы по правилу фаз Гиббса, а также возможное направление протекания исследуемой реакции и равновесный состав газовой смеси; установить направление смещения состояния равновесия рассматриваемой системы.
Количество фаз определяют исходя из определения фазы – это однородная часть гетерогенной системы, с одинаковыми физическими и химическими свойствами, имеющая границы раздела, при переходе через которые свойства системы меняются скачком.
Например, реакция 
Рассматриваемая система состоит из одной фазы (газообразной), которая представляет смесь газов  ,
,  ,
, 
Или, например, реакция

Рассматриваемая система состоит из трех фаз: двух твердых фаз  и
и  , а также одной газообразной, которая представляет смесь двух газов:
, а также одной газообразной, которая представляет смесь двух газов:  и
и  .
.
Число независимых компонентов k равно наименьшему числу составных частей системы, необходимых для образования всех ее фаз при равновесии. Это число определяют как общее число веществ в системе т за вычетом числа связей между ними r, то есть:
|
|
|


Число степеней свободы с (вариантность системы) равно наибольшему числу термодинамических параметров (давления, температуры, концентрации компонентов), которые можно изменять в некоторых пределах так, чтобы число и природа фаз в равновесной системе оставались прежними.
 Число степеней свободы определяют по правилу фаз Гиббса:
Число степеней свободы определяют по правилу фаз Гиббса:

где п - число внешних параметров, влияющих на состояние равновесия
системы. Обычно это давление и температура, то есть п = 2.
Для определения возможного направления протекания реакции необходимо воспользоваться уравнением изотермы Вант-Гоффа:


где П - произведение фактических парциальных давлений газовых
компонентов реакции;
 - константа равновесия реакции при данной температуре.
- константа равновесия реакции при данной температуре.
В соответствии со вторым законом термодинамики в изобарно-изотермических условиях возможно самопроизвольное протекание процессов, сопровождающихся уменьшением энергии Гиббса системы:


В применении к химической реакции это означает, что процесс самопроизвольно может идти слева направо при  и справа налево при
и справа налево при  . Из уравнения (14) следует, что первое условие (
. Из уравнения (14) следует, что первое условие ( ) выполняется при
) выполняется при  , а второе (
, а второе ( ) – при
) – при  .
.
|
|
|
Равновесный состав газовой смеси рассчитывается при заданной температуре по известной константе равновесия. Рассмотрим эту задачу на примере реакции

Дано: общее давление  , исходные количества веществ равны (слева направо) 1,0; 5,0; 2,0; 0,1 молей, Кр = 0,0495.
, исходные количества веществ равны (слева направо) 1,0; 5,0; 2,0; 0,1 молей, Кр = 0,0495.
Пусть при переходе в состояние равновесия прореагировало х молей компонента со стехиометрическим коэффициентом 1, в данном случае кислорода. Запишем под уравнением реакции исходные и равновесные числа молей компонентов:






 |  |  |  | ||||||
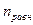 | |||||||||
Суммарное количество молей газообразных веществ равно

Мольные доли каждого вещества в момент равновесия равны:
 ;
; 
 ;
; 
Умножим каждую мольную долю на общее давление, выраженное в относительных единицах. При этом получим парциальные давления газообразных реагентов (конденсированные вещества при этом не учитываются).
 ;
; 
 ;
; 
Равновесный состав газовой смеси рассчитывается из выражения константы равновесия изучаемой реакции:


где  ,
, 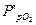 ,
,  ,
,  - равновесные парциальные
- равновесные парциальные
давления  ,
,  ,
,  ,
,  соответственно, выраженные в относительных единицах.
соответственно, выраженные в относительных единицах.
Для нахождения относительного давления следует давление, выраженное в паскалях, разделить на стандартное давление, равное 101325 Па.
|
|
|
Найдем общее давление, выраженное в относительных единицах:


Подставим  ,
,  ,
,  ,
,  в выражение (15).
в выражение (15).
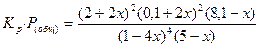
Учитывая, что Р = 0,1, можно записать
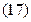

Это уравнение можно решить любым численным методом, например методом половинного деления. После нахождения корня х можно рассчитать числа молей каждого компонента в состоянии равновесия и мольные доли газообразных реагентов. Это и будет результатом расчета состава равновесной системы.
Если константа равновесия очень велика или очень мала, то уравнение типа (17) можно легко решить методом последовательных приближений.
Предположим, что в уравнении (17) справа стоит очень большое число, например 1010. Это означает, что какой-то множитель в знаменателе очень мал. Очевидно, мал может быть только множитель  , так как ни одна из скобок не может быть отрицательной и
, так как ни одна из скобок не может быть отрицательной и  .Введем обозначение
.Введем обозначение  ,причем
,причем  .Тогда
.Тогда  и выражение (17) можно записать в виде:
и выражение (17) можно записать в виде:

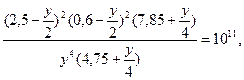

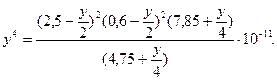
Поскольку величина «у» очень мала, то в первом приближении отбросим «у» во всех скобках. Тогда находим

Откуда

Это - первое приближение. Для следующего приближения подставим во все скобки уравнения (19) величину у. При этом получается второе приближение:  , которое мало отличается от первого. Аналогично находим третье приближение:
, которое мало отличается от первого. Аналогично находим третье приближение:  . На этом вычисления можно закончить. Теперь находим
. На этом вычисления можно закончить. Теперь находим  . Зная х, рассчитываем мольные доли.
. Зная х, рассчитываем мольные доли.
Следует иметь в виду, что у одного из компонентов при этом получится очень малая величина мольной доли. Ясно, что ее надо вычислять не через х, а непосредственно через у.
Аналогично решается задача, если константа Кр очень мала. Тогда надо искать тот множитель в числителе выражения (18), который очень мал, обозначить его через у и действовать, как описано выше.
Последний пункт задания выполняется исходя из принципа Ле Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то в системе самопроизвольно происходят процессы, ослабляющие это воздействие.
ПРИЛОЖЕНИЕ 1
ТРЕБОВАНИЯ К ОФОРМЛЕНИЮ ЗАДАНИЯ
Расчетно-графическая работа должна содержать:
титульный лист;
формулировку задания;
задания (исходные данные);
Расчет, включая таблицы и рисунки. Расчетно-графические задания пишут от руки или печатают на машинке или компьютере на одной стороне листа белой бумаги формата 297х210мм с полями не менее 25мм слева и не менее 8мм справа, которые затем скрепляют. Страницы нумеруются арабскими цифрами в середине верхней части листа. Все страницы рукописи должны быть пронумерованы. Первой считается титульный лист, на ней цифра «1» не ставится. На следующей странице ставится цифра «2» и т.д.
Каждый новый раздел следует начинать с новой страницы. Разделы и подразделы должны иметь наименования. Точка в конце заголовка, раздела и подраздела не ставится. Разделы, подразделы и пункты нумеруются арабскими цифрами.
Рисунки и таблицы должны иметь порядковый номер и название, их нумерация сквозная по всему тексту расчетно-графической работы. В тексте слова «рисунок» и «таблица» пишутся сокращенно, как «рис.» и «табл.», а в заголовке слово таблица пишется полностью. Остальные сокращения в тексте не допускаются.
Формулы должны быть вписаны в текст тщательно, разборчиво и иметь сквозную нумерацию.
Дата добавления: 2015-12-21; просмотров: 23; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
