Тиоцианатометрическое титрование. Сущность метода. Титрант метода, его приготовление, стандартизация. Индикатор метода. Расчеты результатов титрования.


Меркурометрическое титрование. Сущность метода. Титрант метода, его приготовление, стандартизация. Индикаторы метода. Расчеты результатов титрования.

Гексацианоферратометрическое титрование. Сущность метода. Титрант метода, его приготовление, стандартизация. Расчеты результатов титрования.


Сульфатометрическое титрование. Сущность метода. Титрант метода, его приготовление, стандартизация. Индикаторы метода. Способ проведения титрования. Расчеты результатов титрования.

Титрование в неводных средах. Сущность метода кислотно-основного титрования в неводных средах. Классификация растворителей, применяемых в неводном титровании (протонные, апротонные). Влияние природы растворителя на силу (кислотность, основность) растворенного протолита (нивелирующее и дифференцирующее действие растворителей, диэлектрическая проницаемость растворителя). Полнота протекания реакций в неводных растворителях. Факторы, определяющие выбор протолитического растворителя. Расчеты результатов титрования.
Титрование в неводных средах, неводное титрование, - такое титрование, при котором средой служит неводный растворитель с минимальным содержанием воды.
Растворители:
1)Апротонные растворители не проявляют кислотно-основных свойств. Молекулы таких веществ не отдают и не присоединяют протоны. К их числу относятся бензол, толуол, гексан, четыреххлорисый углерод, хлороформ и некоторые другие. Апротонные растворители мало влияют на кислотно-основные свойства растворенных в них веществ.
|
|
|
2) Протонные, или протолитические, рaстворители обладают выраженными кислотно-основными свойствами. Молекулы подобных растворителей способны отдавать или присоединять протоны. При таком определении протонных растворителей к ним могут относиться: 1) как жидкости, молекулы которых сами содержат способные к отщеплению протоны (пример: спирты, амины, карбоновые кислоты, минеральные кислоты), 2) так и жидкости, молекулы которых не содержат протоны, которые могли бы отщепляться при ионизации молекулы растворителя (пример: пиридин).
Нивелирующее действие проявляется в выравнивании силы растворенных в нем протолитов. Нивелирующее действие оказывают протофильные растворители на силу растворенных в них кислот. Так, хлорная и хлороводородная кислоты в водных растворах — сильные, а уксусная кислота - слабая. В растворе протофильного растворителя — жидкого аммиака — все эти три кислоты становятся сильными, включая и уксусную кислоту.
Дифференцирующее действие растворителя проявляется в увеличении различий в силе растворенных в нем протолитов. Такие растворители используют для раздельного титрования смесей кислот или оснований, поскольку различия в показателях констант кислотности или основности веществ, растворенных в подобных растворителях, возрастают по сравнению с водными растворами, вследствие чего становится возможным их раздельное титрование.
|
|
|
Влияние диэлектрической проницаемости растворителя. Диэлектрическая проницаемость ε характеризует способность растворителя уменьшать силу электростатического взаимодействия заряженных частиц по сравнению с вакуумом. Чем больше величина диэлектрической проницаемости (диэлектрической постоянной) растворителя, тем меньше сила электростатического притяжения между катионом и анионом растворенного вещества, тем более глубоко должна протекать его электролитическая диссоциация.
Полнота протекания реакций в неводных растворителях.
Она зависит от величины К-const равновесия той реакции, которая протекает в неводном растворе. Чем К больше, тем полнее идет реакция.
Здесь возможно 2 случая:
1) Титрование слабого основания В сильной кислотой.
Пример: В – основание, его титруют сильной кислотой НСlO4 в растворителе – безводной CH3COOH. Если Кв – const основности основания В, КSH – const автопролиза растворителя, то константа равновесия реакции титрования слабого основания В хлорной кислотой в среде безводной уксусной кислоты равна:
|
|
|
К = 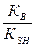
Из соотношения следует, что полнота протекания реакции, характеризуемая величиной константы равновесия К, тем больше, чем выше константа основности Кв титруемого основания В и чем меньше константа автопролиза KSHрастворителя.
2) Титрование слабой кислоты НВ сильным основанием.
Пример: слабую кислоту НВ титруют сильным основанием C2H5OH (это SH).
Тогда для константы равновесия К получаем:
К =  , где
, где  - константа кислотности
- константа кислотности
где КSH = [С2Н5ОН2+][С2Н5О-] —константа автопротолиза растворителя (этанола).
Из уравнения следует, что полнота протекания реакции титрования слабой кислоты НВ сильным основанием, характеризуемая величиной константы равновесия К, тем больше, чем выше константа кислотной диссоциации слабой кислоты НВ и чем меньше константа автопротолиза КSH растворителя.
Дата добавления: 2020-04-25; просмотров: 298; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
