Глюкоза – представитель моносахаридов, химическое строение, физические и химические свойства, применение
Углеводы – это органические вещества в состав молекул которых входит углерод, водород и кислород, причём соотношение водорода и кислорода как и в молекуле воды 2:1
Углеводы делятся на три основных группы:
Моносахариды – углеводы которые не гидролизуются
Пример: C6H12O6– глюкоза
Дисахариды – это углеводы, которые гидролизуются с образованием двух молекул моносахаридов C12H22O11 + H2O = 2C6H12O6
К дисахаридам относятся сахароза, мальтоза (солодовый сахар), лактоза (молочный сахар).
Полисахариды – подвергаются гидролизу с образованием множества молекул моносахаридов
(C12H10O5)n + nH2O = nC6H12O6
Глюкоза C6H12O6
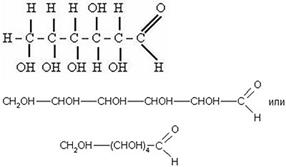
Глюкоза – это этоальдегидоспирт
Физические свойства:
Глюкоза – бесцветное, кристалическое, растворимое в воде вещество, сладкое на вкус, без запаха.
Химические свойства:
Глюкоза реагирует с Cu(OH)2
2NaOH + CuSO4 = Cu(OH)2 + Na2SO4\
Реакция серебрянного зеркала
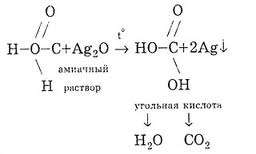
Реакция гидрирования
|
 CH2OH + (CHOH)4 – C =O + H2 = CH2OH (CHOH)4 – CH2OH
CH2OH + (CHOH)4 – C =O + H2 = CH2OH (CHOH)4 – CH2OH
Спиртовое брожение
C6H12O6 = 2C2H5OH + CO2
Молочнокислое брожение
C6H12O6 = CH3 – CHOH – COOH - молочная кислота
Масленно-кислое брожение:
C6H12O6 = C3H7COOH + 2CO2 + 2H2 бутановая кислота
Применение:
Глюкоза применяется в медицине, в кондитерской промышленности, глюкоза в составе патоки используется для изготовления мармелада, карамели, пряников и т.д
Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим превращениям в результате которых образуется диоксид углерода и вода, при это выделяется энергия согласно итоговому уравнению:
|
|
|
C6H12O6 + 6O2 → 6H2O + 6CO2 + 2800 кДж
Реакция серебряного зеркала применяется при изготовлении зеркал и елочных украшений. Используется в текстильной промышленности.
ВОПРОС №18
Крахмал Нахождение в природе практическое значение гидролиз крахмала
Физические свойства
Это белый порошок, нерастворимый в холодной воде и образующий коллоидный раствор (крахмальный клейстер) в горячей воде. Существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
Нахождение в природе
Крахмал – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах:
6CO2 + 6H2O свет, хлорофилл → C6H12O6 + 6O2
nC6H12O6 → (C6H10O5)n + nH2O
глюкоза крахмал
Содержится в клубнях картофеля, зёрнах пшеницы, риса, кукурузы.
Гликоген (животный крахмал), образуется в печени и мышцах животных.
Строение
Состоит из остатков α - глюкозы.
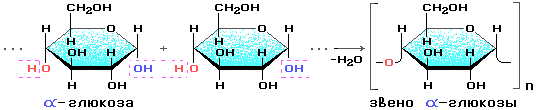
В состав крахмала входят:
· амилоза (внутренняя часть крахмального зерна) – 10-20%
|
|
|
· амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 – 1000 остатков α-глюкозы и имеет неразветвленное строение.

Амилопектин состоит из разветвленных макромолекул, молекулярная масса которых достигает 1 - 6 млн.
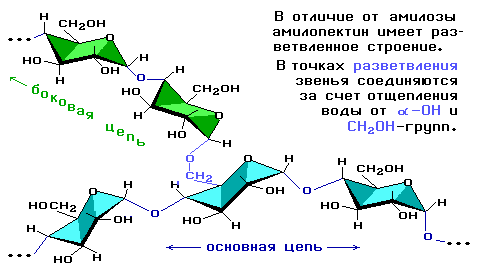
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах. Поэтому крахмал – необходимый резервный углевод питания.
Видео-опыт "Кислотный гидролиз крахмала" .
Подобно амилопектину построен гликоген (животный крахмал), макромолекулы которого отличаются большей разветвлённостью:

Применение
Крахмал широко применяется в различных отраслях промышленности (пищевой, бродильной, фармацевтической, текстильной, бумажной и т.п.).
· Ценный питательный продукт.
· Для накрахмаливания белья.
· В качестве декстринового клея.
Дата добавления: 2019-07-15; просмотров: 840; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
