Фенол его химическое строение свойства получение и применение
Фенол С6Н5ОН– бесцветное, кристаллическое вещество с характерным запахом. Его t плавления = 40,9 С. В холодной воде он мало растворим, но уже при 70◦С растворяется в любых отношениях. Фенол ядовит. В феноле гидроксильная группа соединена с бензольным кольцом.
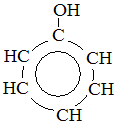
фенол
Химические свойства
1. Взаимодействие с щелочными металллами.
2C6H5OH + 2Na → 2C6H5ONa + H2 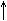
фенолят натрия
2. Взаимодействие со щелочью (фенол – слабая кислота)
C6H5OH + NaOH → C6H5ONa + H2O
3. Галогенирование.
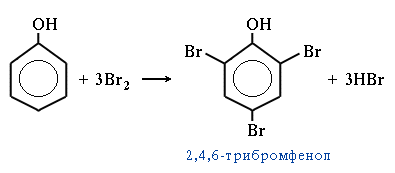
4. Нитрование
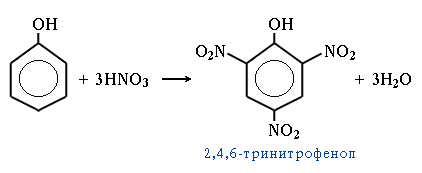
5.Качественная реакция на фенол
3C6H5OH +FeCl3 → (C6H5O)3Fe +3HCl (фиолетовое окрашивание)
Применение
Для дезинфекции, получение лекарств, красителей, взрывчатых веществ, пластмасс.
Получение спиртов из предельных и непредельных углеводородов. Промышленный способ получения метанола.
Наибольшее промышленное значение имеют метанол и этанол.
ВОПРОС №14
Альдегиды их химическое строение и свойства Получение применение муравьного и уксусного альдегидов
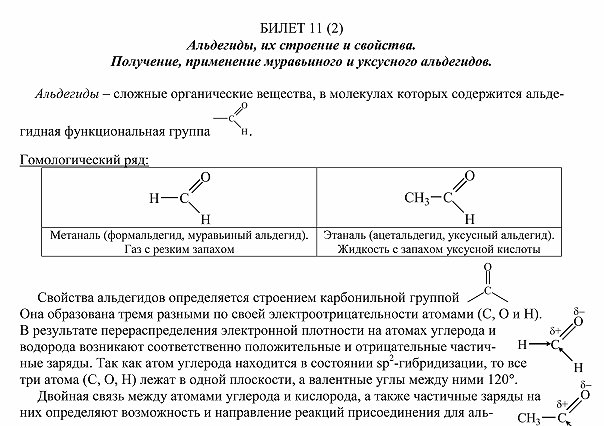
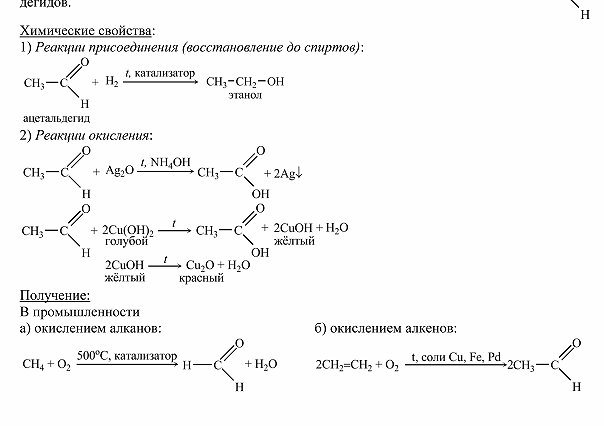
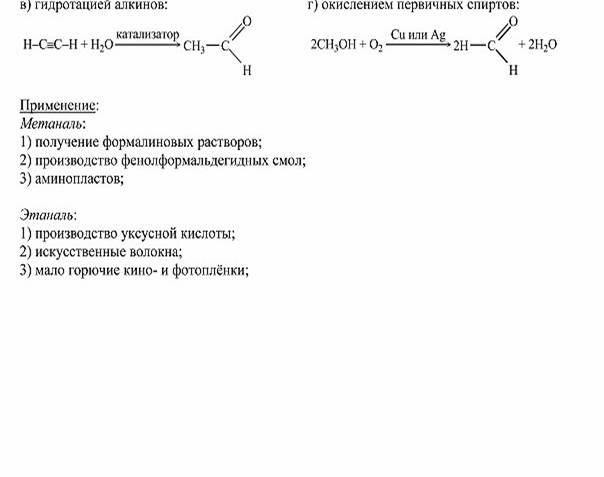
ВОПРОС №15
Предельные одноосновные карбоновые кислоты их строение и свойства на примере уксусной кислоты
Предельные одноосновные карбоновые кислоты– это органические соединения, состоящие из функциональной карбоксильной группы атомов (– CООН), соединенной с радикалом предельного углеводорода.
Общая формула: R-CООН , или Cn H 2n+2 – CООН , где n= 1,2,3 …
Физические свойства: Уксусная кислота – жидкость с острым неприятным запахом, хорошо растворима в воде (как и другие низшие кислоты). Высшие кислоты – твердые вещества, нерастворимы в воде. 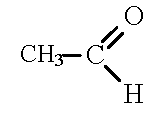
Строение молекулы уксусной кислоты:
В результате сдвига электронной плотности в карбоксильной группе атом водорода в гидроксильной группе становится более подвижным, чем в спиртах, но менее подвижен, чем в муравьиной кислоте. Поэтому уксусная кислота слабее муравьиной.
Химические свойства.
1.Общие с минеральными кислотами:
Диссоциирует в воде (индикатор лакмус дает красный цвет):
CH3 COOH CH3 COO - + H +
Взаимодействует с металлами, стоящими в ряду напряжений до водорода:
2 CH3 COOH + Mg (CH3 COO)2 Mg + H2
ацетат магния
Взаимодействует с основными оксидами с образованием соли и воды:
2 CH3 COOH + MgO (CH3 COO) 2 Mg + H2O
Взаимодействует со щелочами с образованием соли и воды:
CH3 COOH + NaOH CH3 COONa + H2O
ацетат натрия
Взаимодействует со спиртами с образованием сложных эфиров:
CH3 COOH + CH3 OH CH3 CO–O–CH3 + H2O
метиловый спирт метиловый эфир уксусной кислоты
ВОПРОС №16
Жиры их состав и свойства Жиры в природе превращение жиров в организме Продукты технической переработки жиров понятие о синтетических моющих средствах
Жиры – это сложные эфиры глицерина и карбоновых кислот.
Общая формула жиров:
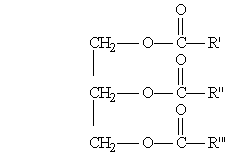
Твёрдые жиры образованы преимущественно высщими предельными карбоновыми кислотами – стеариновой C17H35COOH, пальмитиновой C15H31COOH и некоторыми другими. Жидкие жиры образованы главным образом высшими непредельными карбоновыми кислотами – олеиновойC17H33COOH, ленолевойC17H31COOH
Жиры наряду с углеводородами и белками входят в состав организмов животных и растений. Они являются важной составной частью пищи человека и животных. При окислении жиров в организме выделяется энергия. Когда в органы пищеварения поступают жиры, то под влиянием ферментов они гидролизуются на глицерин и соответствующие кислоты.
Продукты гидролиза всасываются ворсинками кишечника, а затем синтезируется жир, но уже свойственный организм. Потоком крови жиры переносятся в другие органы и ткани организма, где накапливаются или снова гидролизуются и постепенно окисляются до оксида углерода (IV) и воды.
Жиры чаще всего образуются не одной, а разными кислотами.
Вследствие этого различают:
1) жидкие жиры (масла), в составе которых остатки непредельных кислот;
2) твёрдые жиры, в составе которых остатки предельных кислот.
Реакция получения жиров называется этерификация, т.к. жиры это сложные эфиры
Химические свойства жиров определяются принадлежностью их к классу эфиров, следовательно наиболее характерна для них реакция – гидролиз, процесс, обратный этерификации.
Химические свойства жиров.
+вода (гидролиз) – образуются глицерин и карбоновые кислоты, происходит в организме под действием ферментов.
+ Щелочь (щелочной гидролиз) – образуются глицерин и соли карбоновых кислот (мыла)
+Н2 (гидрирование, для жидких жиров, содержащих остатки непредельных кислот) – образуются твердые жиры.
Физические свойства:
Жиры- легкоплавкие вещества, легче воды, нерастворимы в воде, растворимы в органических растворителях, имеют низкую теплопроводность.
Жиры - одна из основных групп веществ, входящих, наряду с белками и углеводами, в состав всех растительных и животных клеток. Жиры обладают высокой энергетической ценностью, при полном окислении в живом организме 1 г жира выделяется 37,7 кДж, что в два раза больше, чем при окислении 1 г белка или углевода.
Гидролиз жиров в технике – источник получения карбоновых кислот, глицерина, мыла. Мыло также получают и при гидрировании жиров.
В настоящее время для стирки в быту и для промывки шерсти и ткани в промышленности используют синтетические моющие средства (СМС). Они обладают более сильными моющим действием по сравнению с мылом. Сырьё для получения СМС – продукты переработки нефти, но не пищевые жиры. Моющая способность СМС примерно в 10 раз выше моющей способности обычного мыла, они моют в жёсткой воде, про этом не создают щелочную среду, так как не гидролизуются.
Жиры в природе превращение жиров в организме
Люди давно научились выделять жир из натуральных объектов и использовать его в повседневной жизни. Жир сгорал в примитивных светильниках, освещая пещеры первобытных людей, жиром смазывали полозья, по которым спускали на воду суда. Жиры – основной источник нашего питания. Но неправильное питание, малоподвижный образ жизни приводит к избыточному весу. Животные пустынь запасают жир как источник энергии и воды. Толстый жировой слой тюленей и китов помогает им плавать в холодных водах Северного Ледовитого океана.
Жиры широко распространены в природе. Наряду с углеводами и белками они входят в состав всех животных и растительных организмов и составляют одну из основных частей нашей пищи. Источниками жиров являются живые организмы. Среди животных это коровы, свиньи, овцы, куры, тюлени, киты, гуси, рыбы (акулы, тресковые, сельди). Из печени трески и акулы получают рыбий жир – лекарственное средство, из сельди – жиры, используемые для подкормки сельскохозяйственных животных. Растительные жиры чаще всего бывают жидкими, их называют маслами. Применяются жиры таких растений, как хлопок, лен, соя, арахис, кунжут, рапс, подсолнечник, горчица, кукуруза, мак, конопля, кокос, облепиха, шиповник, масличная пальма и многих других.
Строение жиров выяснили благодаря трудам французских химиков Шевреля и Бертло. Нагрев жиры с водой в присутствии щелочи, еще в начале XIX века выяснил, что они разлагаются на глицерин и высшие карбоновые кислоты. М. Бертло в 1854, совершил обратную реакцию. Он нагрел смесь глицерина с высшими кислотами и получил жироподобные вещества.


(см с конца на начало 2 . 1)
ВОПРОС №17
Дата добавления: 2019-07-15; просмотров: 2323; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
