Роль воды в химической реакции
Вода играет огромную роль на планете. Входит в состав многих веществ, большую роль играет как растворитель, т.к. в большинстве своѐм вещества растворяются в ней.
Химические свойства Н2О:
Вода – очень активный реагент по следующим причинам:
а) за счет ориентационного взаимодействия с полярными молекулами других веществ;
б) установления водородных связей;
в) проявления донорных свойств со стороны атома кислорода по отношению к частицам – акцепторам электронных пар;
г) электролитической диссоциации при обычных условиях (ионы Н+гидратируются, образуя ионы Н3О+).
1. При температуре выше 1000°С диссоциация водяного пара, но равновесие сдвинуто в сторону воды.
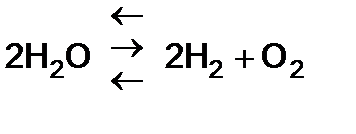 .
.
2. Оксиды металлов и неметаллов соединяются с водой, образуя основания и кислоты (гидрооксиды).


3. Некоторые соли образуют с водой кристаллогидраты. При растворении веществ с ионной структурой молекулы растворителя удерживаются около иона силами электростатического притяжения, т.е. за счет ион -дипольного взаимодействия.
Например: кристаллогидрат сульфата натрия Na2SO4×10H2O (глауберова соль), Na2CO3×10H2O - кристаллическая сода.
Гидраты, образующиеся в результате донорно-акцепторного взаимодействия (где ионы растворенного вещества выступают обычно в качестве акцепторов, а молекулы растворителя в качестве доноров электронных пар) представляют собой частный случай комплексных соединений.
|
|
|
Аквакомплексы– лигaндами является вода, [Co(H2O)6]Cl2, [Al(H2O)6]Cl3, [Cr(H2O)6]Cl3 и др. Некоторые аквакомлексы в кристаллическом состоянии удерживают кристаллизационную воду [Cu(H2O)4]SO4×H2O – медный купорос.
Виды растворов. Истинные растворы. Классификация веществ по их растворимости в воде.
Раствор-это однородная смесь веществ, состоящая из нескольких компонентов.
Различаютистинные, коллоидные растворы и суспензии.
Истинные растворы характеризуются прозрачностью, имеют малые размеры растворённых частиц, легко проходят через биологические мембраны. В зависимости от концентрации солей существует три типа растворов: изотонические; гипертонические; гипотонические.
И з о т о н и ч е с к и ер а с т в о р ыимеют одинаковую концентрацию солей, как и в плазме крови, и такое же осмотическое давление.
К ним относят растворы, имеющие концентрацию солей 0,9%.
Одним из таких растворов является физиологический раствор - это раствор хлорида натрия - NaCl 0,9%. В таком растворе в клетку и из клетки молекулы воды будут перемещаться в равном количестве в обе стороны.
Применение физиологического раствора.
Вводят физраствор через рот, внутривенно, внутримышечно, подкожно, в прямую кишку:
|
|
|
· при некоторых заболеваниях – тяжелые длительные поносы, холера, неукротимая рвота, обширные ожоги хлорид натрия выделяется из организма в больших количествах, чем обычно. Также его много теряется с потом при работе в горячих цехах. В таких случаях в организме возникает его недостаточность, что сопровождается развитием ряда болезненных явлений: спазмы, судороги, нарушения кровообращения, угнетение ЦНС;
· при интоксикациях, кровопотерях, обезвоживании, высокой температуре для промывания глаз, носовой полости.
· натрий хлористый является составной частью растворов применяющихся в качестве кровозамещающих (плазмозамещающих) жидкостей.
Г и п е р т о н и ч е с к и й р а с т в о р(2%, 5%, 10%, 15%) - это раствор в котором концентрация солей выше, чем в плазме крови.
К ним относятся растворы, содержащие более 0,9% солей. Если клетку поместить в такой раствор, то вода из клетки поступает в окружающую среду, при этом падает в клетке тургорное (осмотическое) давление, содержимое клетки сжимается, она теряет форму, происходит обезвоживание. Это явление называется – плазмолиз.Явление плазмолиза обратимое, если поместить клетку в гипотонический раствор, то в таком растворе она восстановит объем и форму Н2 0 клетка.
|
|
|
Применяют гипертонический раствор для:
· полосканий горла, для ванн, обтираний;
· назначают при запорах для опорожнения кишечника.
· в виде компрессов и примочек применяются при лечении гнойных ран, раны очищаются от гноя;
· 2 – 5% растворы используют для промывания желудка при отравлении нитратом серебра;
· внутривенно используют при отёке лёгких и внутренних кровотечениях.
Г и п о т о н и ч е с к и й р а с т в о р- это раствор, имеющий меньшую концентрацию солей, чем в плазме крови. К ним относят дистиллированную воду, талую воду ледников. Если клетку поместить в гипотонический раствор, то в нее из раствора будет поступать вода, осмотическое давление возрастает, клетка набухает. Это явление получило название – деплазмолиз.
Применяют гипотонические растворы в качестве растворителей для водорастворимых лекарственных препаратов. Путём пиноцитоза в клетки поступают питательные вещества из кровяного русла, гормоны, ферменты, лекарственные вещества.
Суспензии, или взвеси, — мутные жидкости, частицы которых размером более 0,2 мкм. При отстаивании взвешенные частицы оседают.
Коллоидные растворы.Если частицы имеют промежуточные размеры от 0,1 до 0,001 мкм, т. е. слишком велики, чтобы образовать истинный раствор, но и слишком малы, чтобы выпасть в осадок, возникает коллоидный раствор (греч. со11а— клей).
|
|
|
По агрегатному состоянию растворы делятся натвердые, жидкие и газообразные. Твердые – сплавы металлов, газообразные – воздух.
Любой раствор, особенно жидкий, как правило, состоит из двух компонентов.
Классификация веществ по их растворимости в воде:
- Хорошо растворимые - если при комнатной температуре в 100 г воды растворяется больше 1 г этого вещества.
- Малорастворимые – если при таких условиях растворяется меньше 1 г вещества в 100 г воды.
- Практически нерастворимые вещества – такие вещества, растворимость которых меньше 0,01 г в 100 г воды.
Виды растворов:
Насыщенный раствор - в котором при данной температуре вещество больше не растворяется.
Ненасыщенный раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе.
Пересыщенный раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях.
Растворение - это химический процесс-взаимодействие молекул растворителя с частицами растворенного вещества.
3.Факторы, от которых зависит растворимость веществ в воде:
1.Природа реагирующих веществ. Полярные молекулы веществ способны растворяться в полярном растворителе – воде.
2. При увеличении температуры жидкости и твердые вещества растворяются лучше, а газы – хуже.
3. При увеличении давления, объем уменьшается и молекул чаще сталкиваться друг с другом, поэтому растворение увеличивается.
4.Значение водныхрастворов для организма человека:
Все вещества поступают в клетки в растворенном виде и выводятся яды из клеток так же в виде растворов.
Вода является участников большинства химических реакций, протекающих в нашем организме. Наш организм на 70% состоит из воды. Содержание растворенного вещества в растворе называют концентрацией.
Способы выражения концентрации растворов: массовая доля растворенного вещества: w(раств.в-ва) = m(вещества) m(раствора) х100%.
Дата добавления: 2018-02-28; просмотров: 4794; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
