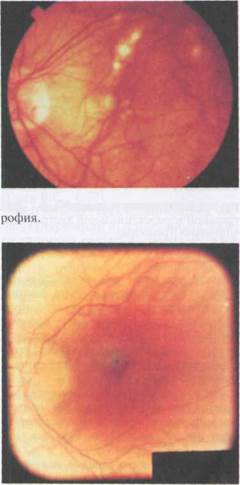
Клиническая картина осложненной близорукости
Глава 6

 ПРИМЕНЕНИЕ РЕТИНОМЕТРИИ У ДЕТЕЙ
ПРИМЕНЕНИЕ РЕТИНОМЕТРИИ У ДЕТЕЙ
Е . И . Шапиро
Исследование сенсорного аппарата глаза является одним из основных показателей оценки функционирования зрительного анализатора. Однако один из самых старых и в настоящее время основных методов исследования органа зрения — визометрия — далеко не всегда позволяет выявить его возможности определить остроту зрения, на-пример в случае помутнения. При этом удается осмотреть глазное дно и приходится дифференцировать причины снижения остроты зрения (помутнение преломляющих сред глаза или поражение сетчатки). Другие способы оценки состояния сенсорного аппарата глаза — исследование ощущения света, локализации источника света, феномена Гайдингера, энтопических феноменов, электрофизиологические методы — часто не позволяют адекват-
но определять состояние сетчатки и количественно оценить зрительные функции.
В последнее время вее большее распространение получает исследование ретинальной остроты зрения (РОЗ), или ретинометрия. Метод основан на многоканальной теории зрения, со-гласно которой зрительная система преобразует изображение в элементар-ные зрительные стимулы: решетки, со-стоящие из чередующихся светлых и темных полос [Глезер В.Д., 1959; Campbell F.W. et al., 1968]. Качество зрительней системы оценивают по со-стоянию так называемой модуляцион-но-передаточной функции (МПФ). Исследование пространственной со-ставляющей МПФ позволяет разде-лить оптические (зависящие от оптического аппарата глаза) и сенсорные
|
|
|
132
факторы передачи изображения, что и даёт возможность дифференцировать причины снижения остроты зрения.
Наиболее эффективным методом оценки сенсорной составляющей МПФ является ретинометрия.
Суть метода заключается в фокуси-ровке вблизи узловых точек оптической системы глаза двух точечных изо-бражений когерентного света; от них в направлении сетчатки распространя-ются расходящиеся пучки света, в области пересечения которых на сетчатке происходит интерференция, воспри-нимаемая глазом как чередование тем-ных и светлых полос, т.е. в виде решет-ки. Преимущество ретинометрии заключается в возможности исследования зрительной способности сенсор-ного аппарата глаза без влияния по-грешностей оптической системы (аберрации, астигматизм, помутнение и др.). В качестве источника света ис-пользуют лазер, так как лазерное излучение обладает когерентностью и мо-нохроматичностью, которые и обеспе-чивают возможность интерференции световых лучей.
В настоящее время ретинометрия широко применяется в офтальмологии для исследования сенсорного аппарата органа зрения и позволяет количест-венно оценить различительную спо-собность сетчатки в общепринятых ви-зометрических единицах (0,1, 0,2, 0,3 и т.д.). Существуют несколько моделей ретинометров, в которых, как правило, используется газовый гелий-неоновый лазер, работающий в красном диапазоне (длина волны 632,8 мм). Разные типы приборов имеют разные интер-ференционные элементы (интерферо-метр Майкельсона, решетка Ронши, призма Дове и др.) и конструкцию (стационарные и ручные приборы, на-: садки на щелевые лампы). В клинической практике в основном исследова-i ние РОЗ проводят для прогнозирова-ния послеоперационнего визуального исхода при помутнениях преломляю-ших сред глаза (главным образом при | катаракте). Исследования разных авто-! ров показали высокий коэффициент
|
|
|
корреляци и между предоперационной и послеоперационной РОЗ (от 63 до 95 %). Ретинометрия используется также для оценки динамики патологического процесса, локализующегося в заднем полюсе глаза.
Известно, что при сложных формах аномалий рефракции, например при высокой степени астигматизма, нередко не удается с помощью оптической коррекции добиться максимальной клинической остроты зрения (КОЗ) и ставится диагноз амблиопии. Э.С. Аветисов и соавт. (1968) показали, что при РОЗ 1,0 и выше причиной чаще всего является недостаточная коррекция и требуется ее уточнение, применение контактных линз и др.
|
|
|
В педиатрической офтальмологии определение РОЗ используется также в диагностических целях, в том числе для диагностики амблиопии.
Клиническая практика показала, что ретинометрию можно применять у детей, начиная с 3—4 лет, а иногда и раньше.
Кроме диагностики, ретинометрию применяют у детей и в лечебных целях при амблиопии.
Как известно, лечение при амблиопии является одной из актуальных проблем детской офтальмологии. Это объясняется распространенностью указанной патологии (примерно у 5 % населения) и трудностью реабилита-ции пациентов.
Предварителы-! ые исследования РОЗ в нормальных глазах и при патологических изменениях в заднем отрезке глаз позволили выявить некото-рые закономерности МПФ зрительной системы. Между РОЗ и КОЗ имеются различия. Как правило, РОЗ примерно на 10 % выше КОЗ. Установлено также наличне (примерно у 25 % обследован-ных) функциональной анизотропни сетчатки, т.е. разная РОЗ в разных меридианах [Бегишвили Д.Г., 1983]. На это же указывают F. Campbell и соавт. (1968), которые определили, что глаз лучше различает горизонтальные и вертикальные линии, чем косо направленные (косые). Позднее Э.С. Авети-
|
|
|
133
сов и соавт. (1974), D. Mitchell и соавт. (1973) выявили феномен так называе-мой меридиональней амблиопии, ко-торый наиболее часто встречается при астигматизме. При этом наблюдается снижение РОЗ в одном из меридианов, что объясняет нередко наблюдаемую неэффективность оптической коррек-ции астигматизма. По мнению D. Mitchell и соавт. (1973), меридиональная амблиопия формируется в первые 6 мес жизни ребенка и связана с нерез-ким изображением в плоскости с более сильной рефракцией, что приводит к изменению ретинонейронных связей в этом меридиане. Как известно, патогенетической основой амблиопии явля-ется стойкое торможение функции центрального зрения в результате по-стоянного выключения косящего глаза из зрительного акта при дисбиноку-лярной амблиопии или отсутствия на сетчатке резкого, контрастного изо-бражения в случае рефракционной или анизометропической амблиопии [Аве-тисов Э.С., 1968].
Поэтому в основе плеоптического лечения лежит растормаживающее воздействие на сенсорную систему амблиопического глаза. С этой целью производят окклюзию лучше видящего глаза или поочередную окклюзию (при двусторонней амблиопии), локальное раздражение светом фовеолярной области, применяют метод отрицательного последовательного образа и др. Вее указанные методы дают достаточ-но хороший терапевтический эффект, однако в значительной части случаев не удается добиться приемлемого для реабилитации пациентов визуального результата.
В связи с этим продолжаются работы по развитию и совершенствованию методов плеоптического лечения на основе новых исследований, главным образом в области нейрофизиологии зрения. В частности, установлено, что форменное зрение обеспечивается сложным взаимодействием рецептор-ных и нейронных полей на всех уров-нях зрительных путей, для возбужде-ния которых необходимо наличне в
134
поле зрения структуры с разными элементами яркости. Зрительная система слабо отвечает на диффузиые световые раздражения, но лучше реагирует на световые стимулы, имеющие опреде-ленный рисунок [Глезер В.Д., 1959; Banks R. et al., 1978].
Поэтому В.А. Розенберг (1976) предложил использовать для локального раздражения макулярной зоны при амблиопии световые поля разной конфигурации, разного размера, со сложным рисунком.
Дальнейшие нейрофизиологические исследования показали, что зрительная система, как указывалось выше, представляет собой ряд независимых каналов, каждый из которых селектив-но чувствителен к относительно узкой полосе пространственных частот. Зрительная система путем так называемых преобразований Фурье осуществляет разложение изображений на совокуп-ность периодических решеток разной пространственной частоты с синусои-дальным распределением освещенно-сти, ориентированием, контрастом, к которому чувствителен фазоспецифи-ческий канал. Таким образом, орган зрения осуществляет обнаружение, выделение и селективный анализ параметров изображения: пространственной частоты, ориентации, контраста, направления движения и др. [Davis Е., Graham N., 1981]. Дальнейшая трансформация и передача информа-ции происходит в высших отделах зрительного анализатора [Глезер В.Д., 1959; Campbell F. et al., 1966]. Установлено, что при функциональных нару-шениях в случае амблиопии частотно-контрастная характеристика обычно значительно снижена в области средних и высоких частот [Thomas J. et al., 1978]. В связи с этим при лечении пациентов с амблиопией необходимо преимущественно активизировать ре-тинокортикальные элементы, воспри-нимающие пространственные частоты с пониженной амплитудой. Для этого необходимо адекватное стимулирование периодической структурой, имею-щей высокий контраст и частоту, соот-
ветствующую области пониженной чувствительности. Простейшим стимулом являются, как указывалось вы-ше, решетки с синусоидальным распределением освещенности. На осно-вании принципов R. Banks и соавт. в 1978 г. описали метод лечения амблио-пии с помощью элементарных зри-тельных стимулов — решеток с разны-ми пространственной частотой, ори-ентацией и контрастом. Это позволило стабилизировать процессы возбужде-ния и торможения в макулярной области, восстановить ретинокортикаль-ные связи и способности к первично-му частотно-контрастному анализу параметров зрительного стимула. Для этого использовали проецирование синусоидальных решеток с разными частотами и ориентацией на дисплее. Однако этот метод имеет недостатки, так как из-за влияния погрешностей оптической системы глаза далеко не всегда удается получить контрастное, четкое изображение на сетчатке.
Ретинометр позволяет получать на сетчатке контрастное изображение решетки независимо от недостатков оптики глаза (аберрации, помутнения и др.). Поэтому Э.С. Аветисов и соавт. (1982) предложили метод лечения па-циентов с амблиопией с помощью ре-тинометра.
Возможность плавного изменения периода чередования интерференци-онных полос и их ориентации при ле-чении пациентов с амблиопией имеет большое значение, так как позволяет воздействовать с необходимой интен-сивностью на каналы со сниженной частотно-контрастной характеристикой.
Лечение с помощью лазерной ин-терференционной картины позволяет избирательно восстанавливать редуцированные функции зрительных нейронов, отвечающих за передачу про-странственно-частотной зрительней информации. Раздражение же сетчат-ки обычным диффузным световым излучением воздействует на вею систему информационных каналов в целом.
Кроме того, в отличие от метода
Банка—Кампбелла интерференцион-ные решетки представляют собой идеальный тест почти со 100 % контрастом.
Лечение с помощью ретинометра осуществляется следующим образом: на глазное дно амблиопичного глаза проецируется интерференционный тест-объект с размером поля 5—6°, за-полненный чередующимися черными и красными полосами. Пациенту предъявляют картинку с хорошо раз-личимыми пространственными частотами. Затем постепенно уменьшают период чередования полос, достигая пороговего значения, при котором структура не различается и тест вос-принимается как окрашенный с равным распределением освещенности. Предъявление теста на пороге воспри-ятия производят в течение 3—5 с по 7—10 циклов путем прерывания светового потока, затем возвращаются к уровн ю пространственных частот, хорошо различимых пациентом, и вновь повторяют цикл раздражения макулярной зоны.
Во время предъявления теста изме-няют положение полос, располагая их в разных меридианах: 45, 90, 135 и 180°. При налични меридиональней амблиопии на меридиан с низкой РОЗ воздействуют более длительно (10— 15 циклов). Процедура длится пример-но 5 мин. Ежедневно возможно проведение 2 сеансов с интервалом 30— 40 мин. Куре лечения состоит из 10 сеансов, о процессе восстановления зри-тельной функции судят по повыше-нию РОЗ. Как правило, в результате лечения удается добиться повышения РОЗ и КОЗ у большинства пациентов. Так, по данным Г.В. Белаловой (1985), при применении описанного метода острота зрения повысилась у 78 % пациентов с амблиопией. Д.Ю. Говоров-ский (2001) показал, что в результате лечения с помощью ретинометра доля детей с остротой зрения выше 0,6 уве-личилась с 34,3 до 64 %, т.е. почти вдвое.
Клиническая практика показывает, что повышение РОЗ было, как прави-
135
ло, больше, чем КОЗ. Для повышения КОЗ при амблиопии необходимо применение других методов лечения, глав-ным образом окклюзии лучшевидяще-го глаза. Различие показателей РОЗ и КОЗ после лечения с помощью рети-нометра может быть объяснено тем, что различение объектов с периодической структурой легче, чем распознавание оптотипов, так как осуществля -ется с минимальным участием высших отделов зрительного анализатора. При распознавании же оптотипов необходимо различать не только отдельные детали, но и объединять их в единый образ.
Необходимо также учесть результаты лазерной ретинометрии и исследова-ния нормальных глаз у детей, показав-шие, что различительная способность сетчатки у детей существенно не отли-чается от таковой у взрослых. В то же время известно, что у детей до 5— 12 лет КОЗ ниже, чем у взрослых, из-за недостаточной дифференцировки зри-тельной системы [Мануйлов В.Г., 1971; Ковалевский Е.И., 1980, и др.].
По данным указанных исследова-ний, сенситивный период формирова-ния различительной способности сетчатки, вероятнее всего, заканчивается в раннем детском возрасте (не позднее 3 лет), а предметное зрение формиру-ется постепенно на базе сложившейся различительной ретинальной способности. По веей вероятности, факт су-ществования функциональной разобщенное™ между различительной спо-собностью сетчатки и предметным зрением и объясняет различие по времени нормализации РОЗ и повышения КОЗ. Высшие отделы зрительного анализатора как бы заново обучаются пре-образованию элементарных стимулов в зрительный образ.
Это указывает на необходимость применения при амблиопии комбинированного лечения методов с использованием разных способов плеоптики. Повышение РОЗ, особенно при мери-диональной амблиопии, позволяет значительно улучшить результаты функциональной реабилитации детей.
136
СПИСОК ЛИТЕРАТУРЫ
Аветисов Э. С. Дисбинокулярная амблиопия и ее лечение. — М: Медицина, 1968. — 208 с.
Аветисов Э.С., Урмахер Л.С., Шапиро Е.И., Аникина Е.Б. Исследование интерферен-ционной остроты зрения // Материалы 6-й Республиканской конференции оф-тальмологов Лит. ССР. — Каунас,
1974. -С. 125-126.
БегишвилиД.Г. Применение лазерной ретинометрии в оптико-реконструктивной хирургии глаза: Автореф. дис. ... канд. мед. наук. — М., 1983. — 22 с.
Белалова Г.В. Лазерплеоптика и факторы ее действия // VI Всесоюзный съезд оф-тальмологов. Т. 5. — М., 1985. — С. 14.
Глезер В.Д. К характеристике глаза как сле-дящей системы // Физиол. журн. — 1959. - Т. 45, № 3. - С. 271-279.
Говоровский Д.Ю. Сравнительная характеристика методов лечения амблиопии // Труды международного симпозиума «Близорукость, нарушения рефракции, аккомодации и глазодвигательного аппарата». - М., 2001. - С. 172-173.
Мануйлов В.Г. К вопросу об остроте зрения детей дошкольного возраста // Глаукома и другие заболевания глаз: Труды Ленинградского санитарно-гигиенического мед. института. Т. 95. — Л., 1971. — С. 129-133.
Сорокина PC . Восстановление бинокуляр-ных функций при односторонней мио-пии, корригированной контактными линзами // Материалы III Всероссийского съезда офтальмологов. — М.,
1975. - С. 55-59.
Davis Е ., Graham N. Spatial fraguncy uncertainty effecte in the detection of sinusoidal gratinge // Vis. Res. — 1981. — Vol. 21, N 5. - P. 705-712.
Lawden M., Hess R., Campbell F. The discriminability of special phase relation-shine in ambliopia // Vis. Res. — 1982. — Vol. 22, N 8. - P. 1005-1016.
Mitchell D., Freeman R., Miloclot M. et al. Meridional ambliopia evidence for modification of the human visual system by early visual experience // Vis. Res. — 1973. — Vol. 13, N 3. - P. 539-557.
Thomas J. Normal and ambliopic contrast sensitivity functions in central and perifhericul retinas // Invest. Ophthalm. — 1978. - Vol. 17, N 8. - P. 746-753.
Campbell F.W., Robson J. Application of fourier analysis to the visibility of gratings // J. Physiol. - 1968. - Vol. 197, N 3. -P. 551-564.
Глава 7

 ОСЛОЖНЕННАЯ БЛИЗОРУКОСТЬ : ВРОЖДЕННАЯ И ПРИОБРЕТЕННАЯ
ОСЛОЖНЕННАЯ БЛИЗОРУКОСТЬ : ВРОЖДЕННАЯ И ПРИОБРЕТЕННАЯ
ЕЛ . Тарутта
Близорукость является наиболее частой аномалией рефракции. Ее распро-страненность в популяции в развитых странах составляет 25—40 %, достигая в ряде регионов Востока 50—70 % [Аветисов Э.С., 1999].
В большинстве случаев вызванное близорукостью снижение зрения легко корригируется, и острота зрения, a также другие функции глаза в условиях адекватной оптической коррекции со-ответствуют нормальным значениям. Такую миопию называют простой, физиологической, подчеркивая отсутствие необратимых функциональных расстройств. Более редкими, но гораз-до более важными в медико-социаль-ном отношении являются формы мио-пии, при которых снижение и даже утрата зрительных функций не поддают-ся оптической или хирургической коррекции и нередко являются необрати-мыми. Такую миопию называют патологической, дегенеративной, ослож-ненной, иногда миопической болез-нью. Именно эта форма близорукости является одной из ведущих причин ин-валидности по зрению, занимая 2—3-е ранговое место в нашей стране, Анг-лии, Германии, 5—7-е в США [Южа-ков A.M. и др., 1991; Либман Е.С. и ■ др., 2001; Sorsby A., 1972]. Инвалид-I ность вследствие миопии наступает, [ как правило, в возрасте до 50 лет, в I среднем на 10 лет раньше, чем при диабетической ретинопатии, глаукоме, катаракте, сосудистых заболеваниях. В возрастной группе до 60 лет ослож-ненная миопия является ведущей причиной инвалидности [Соловьев В.В., Шестакова Г.Ф., 1996; Sorsby A., 1972]. Частота осложненной миопии составляет, по разным данным, от 0,2 до 9,6 % [Sorsby A., 1972; Curtin B.J.,
1985]. Такой разброс показателей, оче-видно, свидетельствуёт об отсутствии единых критериев оценки, однако на частоту осложненной миопии, как и на распространен ность миопии в це-лом, оказывают влияние половые, этнические, географические и социально-экономические факторы. Она наиболее высока среди женщин в высших социально-экономических классах и с высокой академической нагрузкой. Минимальная частота отмечается среди чернокожих, максимальная — у представителей азиатской расы.
Причиной некорригируемого сниже-ния зрения при близорукости оказыва-ются, как правило, изменения на глазном дне, локализующиеся в области желтого пятна, отслойка сетчатки, а также различные аномалии развития зри-тельного анализатора и амблиопия. Последние характерны только для врожденной миопии, являющейся неред-кой причиной слабовидения у детей: около 30 % среди всех детей с врожденной близорукостью [Аветисов Э.С., Мац К.А., 1989].
Диагноз осложненной миопии ста-вят при обнаружении патологических изменений на глазном дне.
Этиология и патогенез
В настоящее время признано, что в происхождении миопии играёт роль сочетание генетических (полигенный характер наследования, чаще по ауто-сомно-рецессивному типу) и средовых факторов. Влияние последних может проявиться как во внутриутробном (токсоплазмоз, краснуха, токсикозы беременных, часто являющиеся причиной недоношенности), так и в пост-натальном периоде (острые и хрониче-
137
ские инфекции, в особенности сопро-вождающиеся гипертермией, длительным течением, уменьшением массы тела, недостаток полноценных белков в пище, тяжелый физический, а также зрительно-напряженный труд).
Точная патофизиология развития дегенеративной миопии не раскрыта, однако отдельные звенья ее патогенеза изучены достаточно полно и схемати-чески могут быть представлены сле-дующим образом: ослабление опорных свойств склеральной капсулы вследст-вие ее структурных и метаболических нарушений —» растяжение склеры и внутренних оболочек глаза под действием внутриглазного давления -» ише-мия и истончение оболочек, повреждение их сосудистых и нервных элементов, развитие дистрофических из-менений и разрывов; одновременно ликвификация стекловидного тела вследствие нарушения гематорети-нального барьера —> изменение его метаболизма —> деструкция стекловидного тела, формирование витреорети-нальных сращений, развитие задней отслойки стекловидного тела —> витре-оретинальная тракция -» возникновение разрывов и отслойки сетчатки.
В патогенезе прогрессирующей миопии и ее осложнений играёт роль не только аномальное удлинение глаза, но и увеличение всех его размеров (горизонтального, вертикального, косых) и соответственно объема [Авети-совЭ.С. идр., 1988; Свирин А.В., 1991; Епишева С.Н., 2001].
Согласно современным данным, об-ласть экватора и задний полюс глаза у разных пациентов вовлекаются в патологический процесс в разной степени, что и приводит к повреждению тех или иных отделов глазного дна [Авети-сов Э.С. и др., 1988; Curtin B.J., 1985].
Гистологически обнаружи ваются изменения в склере, хороидее, сетчат-ке (особенно в ретинальном пигмент-ном эпителии), стекловидном теле. Наблюдается уменьшение диаметра и нарушение организации коллагеновых фибрилл склеры, генерализованное истончение хороидеи вплоть до потери
138
хориокапилляриса, приводящее к полному отсутствию хороидеи, особенно в основании стафиломы. Клетки пигме нтного эпителия сетчатки более плоские и крупные, чем в норме. Изменения в мембране Бруха разнооб-разны: истончения, трещины, разрывы.
Стекловидное тело претерпевает значительные изменения при прогрессирующей близорукости, нарастаю-щие по мере увеличения ее степени и играющие важную роль в развитии осложнений. Оформленное стекловидное тело не может увеличивать свой обьем [Аветисов Э.С, 1999; Soub-rane G. et al., 1999]. При увеличении размеров глазного яблока стекловидное тело вначале заполняет увеличи-вающийся обьем за счет своего разжи-жения (ликвификация), однако со времёнём наступает срыв этого механизма и происходит коллапс стекловидного тела [Pereins E.S., 1979]. Ликвификация стекловидного тела является наи-более ранним симптомом, отмечае-мым уже при слабой миопии и уже в детском возрасте. A. Hosaka и соавт. [1988], отметившие с помощью флюо-рофотометрии ликвификацию стекловидного тела при миопии более 2,5 дптр, считают ее признаком нарушения гематоретинального барьера. Жидкость может проникать в стекловидное тело в области его основания. В этой зоне коллагеновые фибриллы стекловидного тела примыкают к ре-тинальным клеткам, пенетрируя внут-реннюю пограничную мембрану [Soubrane G. et al., 1999]. В периферических кортикальных отделах стекловидного тела находят наиболее высокую концентрацию растворимых белков, проникающих в стекловидного тело, по-видимому, из сосудов сетчатки [Колотов В.В., Шастина Е.А., 1976]. R.K. Blach (1964) обнаруживал цен-тральную ликвификацию стекловидного тела при миопии в глазах с нормальным основанием стекловидного тела. О возможности проникновения жидкости через неповрежденную пограничную гиалоидную мембрану
стекловидного тела свидетельствуют результаты экспериментов на живот-ных [Устинова Е.И., 1976].
Другим путем ликвификации стекловидного тела считают поступление камерной влаги, возможно через зону-лярную щель Зальцмана, расположенную несколько кпереди от начала ос-нования стекловидного тела, между ним и зонулярной частью передней гиалоидной мембраны [Колотов В.В., Шастина Е.А., 1976].
Клинически начальную генерализо-ванную ликвификацию стекловидного тела можно определить по увеличен-ной продолжительности движений фибрилл стекловидного тела в ответ на глазные саккады [Goldstein J.H. et al., 1976]. Больные часто предъявляют жалобы на плавающие «запятые», пятна или «бактериеподобные» объекты, ви-димые на ярком однородном фоне.
В норме гидратированные полимеры гиалуроновой кислоты находятся в определенных пространственных взаи-моотношениях с дипольными молеку-лами воды и другими свободными компонентами стекловидного тела (белки, электролиты). Пространственная целостность стекловидного тела утрачивается при изменении степени полимеризации гиалуроновой кислоты вследствие нейтрализации ее отрицательных валентностей положительно заряженными молекулами. Это приво-дит к синерезису геля стекловидного тела. Суть этого процесса состоит во фракционировании стекловидного тела на структурную и жидкую части со скоплением жидкости в макроскопических полостях [Горбань А.И. и др., 1976]. Эти изменения при миопии на-зывают лакунарной дегенерацией стекловидного тела [Curtin B.J., 1985]. Co времёнём лакуны, или синеретиче-ские полости, отодвигаются кзади, a оформленный гель перемещается кпереди, к основанию стекловидного тела. В этих условиях наступает дегенерация
цавленных внутри компактной массы юкон стекловидного тела. Эту кар-
шу называют микрофибриллярной
ггенерацией. Жидкость внутри сине-
ретических полостей в дальнейшем проникает в потенциальное субгиало-идное пространство и отделяет основание кортекса от сетчатки. А.И. Горбань (1976) указывает, что этому пред-шествует ослабление витреоретиналь-ной связи: постепенный распад погра-ничных мембран на больших участках зоны контакта стекловидного тела с сетчаткой, расщепление кортикально-го коллагена или даже поверхностных слоев глии сетчатки. В итоге формиру-ются условия для отделения основной массы геля стекловидного тела от внутренней поверхности сетчатки на всех участках, где отсутствует их проч-ная связь. Как известно, участками та-кой прочной связи являются основание стекловидного тела, область диска зрительного нерва, макулы, а также вдоль крупных сосудов сетчатки в тан-генциальных направлениях [Soub-rane G. et al., 1999].
Задняя отслойка стекловидного тела, нередкая в пожилом и старческом возрасте, при близорукости наступает го-раздо раньше, и ее частота и интенсив-ность увеличиваются в соответствии со степенью миопии. У детей с миопией высокой степени отслойка стекловидного тела отмечена уже в 6-летнем возрасте. В глазах с миопией 8,0 дптр стекловидное тело крайне редко быва-ет неизмененным даже в детском возрасте. При остром развитии задняя отслойка стекловидного тела может со-провождаться фотопсиями, возникаю-щими из-за витреоретинальных трак-ций, и внезапным появлением множе-ства мелких темных пятен (мигрирую-щие скотомы или плавающие помут-нения), вызванных мелкими нежными кровоизлияниями в стекловидное тело из поврежденных сосудов сетчатки. Типичным является также «подни-мающийся дымок» или «задымлен-ность» видения, также обусловленные кровоизлиянием в стекловидное тело. При повреждении крупных сосудов возможны массивные преретинальные и интравитреальные геморрагии. В случае отделения стекловидного тела от диска зрительного нерва глиальные
139
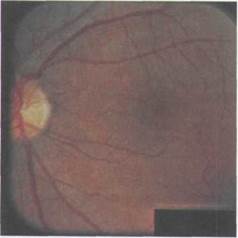
Рис. 7.1. Глазное дно при неосложнен-ной миопии слабой степени. Миопиче-ский конус у височного края диска зри-тельного нерва.
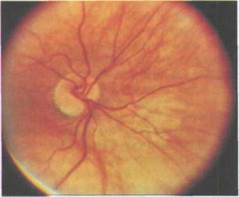
Рис. 7.2. Диффузная хориоретинальная атрофия заднего полюса.
элементы периферии диска остаются на задней гиалоидной мембране в виде кольцевидного помутнения. В этих случаях пациенты отмечают плаваю-щее по кругу черное колыдо в цен-тральном поле зрения. Возникновение задней отслойки стекловидного тела, помимо кровоизлияний, может приво-дить к формированию тракционных разрывов и отслойке сетчатки, а также к развитию транссудатавных процессов в макуле и даже кистозной макуло-
140
патии [Kanski J.J., 1975; Curtin B.J., 1985]. Последнее объясняют ликвида-цией поддерживающего давления стекловидного тела на оболочки глаза, а также действием прямых витреорети-нальных тракций в макулярной области [Авербах Г.И., 1989].
Клиническая картина осложненной близорукости
Дистрофические изменения на глазном дне при осложненной близорукости могут локализоваться как в его нейтральных отделах, так и на периферии. Центральные изменения касают-ся диска зрительного нерва (ДЗН) и макулярной области. Изменения ДЗН — это формирование миопиче-ского конуса, наклонное положение диска и супертракция оболочек (рис. 7.1).
Конус — одно из наиболее часто встречающихся клинических проявле-ний миопии. Он формируется в результате ретракции комплекса стекло-видной пластинки (пигментный эпи-телий — стекловидная пластинка — хориокапиллярис) от края диска зрительного нерва. В результате возни каёт концентрическая область, в которой белая склера хорошо просматривается через прозрачную нейросенсорную сетчатку. С противоположной стороны диска часто обнаруживается утолщенный край оболочек, покрывающий часть оптического отверстия и назы-ваемый супертракцией. Наиболее часто конус располагается с височной стороны ДЗН, но может иметь и лю-бую другую локализацию. По мере прогрессирования миопии размеры конуса увеличиваются, нередко фор-мируются круговые конусы. С возрастом у больных с высокой прогресси-рующей близорукостью развивается перипапиллярная атрофия хороидеи с вовлечением в неё края конуса, кото-рый при этом становится неровным. Возникает как бы двойной конус: внутренний склеральный и наружный хороидальный, что является признаком активного растяжения склеры,
|
|
| Рис. 7.3. Очаговая хориоретинальная ат- |
прогрессирования миопии и, возмож-но, начала формирования стафиломы. 06 этом же свидетельствуют наклон-ное положение ДЗН (в сторону фор-мирующейся стафиломы) и супертрак-ция оболочек с противоположной стороны. У части взрослых пациентов с высокой прогрессирующеи близоруко-стью развивается частичная атрофия ДЗН, предположительно сосудистого генеза, с соответствующим его поблед-нением. Изменяется также ход сосудов ДЗН (в виде лежачей буквы «Т» или «У») и уменьшается их калибр.
Центральные хориоретинальные дистрофии (ЦХРД) при миопии — это «сухая» (атрофическая) и «влажная» (транссудативная) дистрофии макулы, лаковые трещины, центральное пиг-ментное пятно Фукса.
Сухая форма ЦХРД характеризуется вначале побледнением глазного дна вследствие частичней утраты пигмент-ного рпителия и хориокапиллярного слоя (рис. 7.2). Атрофия этих слоев делаёт видимыми при офтальмоскопни крупные сосуды хороидеи. Это создаёт картину так называемого мозаичного \ глазного дна. По мере прогрессирова-; ния процесса запустевают мелкие, средние и крупные сосуды хороидеи. Истончение нейросенсорной сетчатки в макулярной зоне, ее атрофия, особенно при формировании стафиломы, приводят к выпрямлению ретиналь-ных сосудов и уменьшению или исчез-: новению желтой окраски макулы. Нередко при дегенеративной миопии от-мечают аномальное распределение хо-роидальных вен. Водоворотоподобные вены, хорошо видимые через истон-ченные ткани, могут пересекать маку-лярную зону или окружать ДЗН.
Описанная картина представляет собой диффузную хориоретинальную атрофию и может затрагивать весь задний полюс, а также периферию глазного дна. В макуле и парамакулярно, a также вокруг ДЗН вначале могут появ-ляться мелкие округлые бело-желтые очажки, иногда с пигментированными краями: развивается очаговая хориоре-тинальная атрофия (рис. 7.3). С воз-
Рис. 7.4. Геморрагическая форма цен-тральной хориоретинальной дистрофии: формирующаяся неоваскулярная мембрана.
растом и по мере прогрессирования миопии очаги увеличиваются и имеют тенденцию к слиянию.
Атрофическая, или «сухая», форма ЦХРД сопровождается постепенным медленным снижением зрения. Возможей переход «сухой» формы ЦХРД во «влажную»; это, по разным данным, происходит в 13—60 % случаев [Авер-бах Г.И., 1989; Иванишко Ю.А., 1994].
Транссудативная, или «влажная», форма ЦХРД при миопии встречается
141
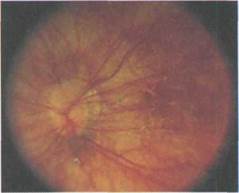
Рис. 7.5. Миопия, осложненная цен-тральной хориоретинальной дистрофией. «Лаковые» трещины.
значительно реже, чем «сухая», однако характеризуется относительно ранним началом и тяжелым течением и сопро-вождается резкой внезапной потерей зрения. Патогенетическую основу этой формы макулодистрофии составляют хориоретинальные изменения с повреждением мембраны Бруха и в части случаев с развитием субретинальной неоваскуляризации. Наиболее частой формой транссудативной миопиче-ской макулодистрофии является геморрагическая (рис. 7.4).
Различают два основных патогенетических типа кровоизлияний при миопии: связанные с разрывами стек-ловидной пластинки (формирование так называемых лаковых трещин — ЛТ) без неоваскуляризации и связанные с формированием субретинальной неоваскулярной мембраны [Ципур-ская С.С., 1988].
Кровоизлияния первого типа могут встречаться у молодых пациентов, a также у детей и подростков с врожденной или, реже, рано приобретенной миопией и быть одним из ранних признаков ее осложненного течения. Они имеют вид единичных или множественных темно-красных округлых пя-тен с четкими контурами, как правило, небольшого размера: от точечных до у^ диаметра диска (ДД). Их нередко на-зывают монетовидными. Они распола-
гаются в наружных (глубоких) слоях сетчатки, где аксоны располагаются перпендикулярно поверхности мембраны Бруха. В этих слоях экстраваза-ция крови имеет дискретную локали-зацию, поскольку элементы крови раз-горожены окружающими аксонами [Eagle R.C., 1999].
С помощью флюоресцентной ан-гиографии показана возможность ло-кализации кровоизлияний первого типа и в хороидее [Ципурская С.С., 1988]. Как правило, они быстро расса-сываются без значительного снижения функции.
Как уже упоминалось, происхождение этих кровоизлияний связывают с формированием ЛТ (рис. 7.5). ЛТ имеют вид желто-белых ломаных линий неравномерного калибра, часто ветвя-щихся, звездчатых, пересекающих задний полюс в косом, радиальном или, чаще, горизонтальном направлении. Болыиинство ЛТ образуется в маку-лярной зоне, в основании стафиломы, некоторые достигают височного пери-папиллярного конуса. Они локализу-ются в самых глубоких слоях сетчатки. Сосуды хороидеи могут пересекать ЛТ сзади, ход этих сосудов, по данным ФАГ, не прерывается. Внутренние елой сетчатки над ЛТ не повреждени [Ципурская С.С., 1988; Soubrane G. et al., 1999]. Происхождение ЛТ связано с механическим повреждением комплекса пигментный эпителий — стек-ловидная пластинка — хориокапилля-рис. Впоследствии разрывы замещают-ся рубцовой тканью и могут со времёнём растягиваться в большие атрофи-ческие очаги. Повреждение хориока-пилляров при разрыве этого комплекса и является источником геморрагий. Появление ЛТ может сопровождаться субъективными ощущениями: вспыш-ками света, метаморфопсиями, поло-жительной скотомой в поле зрения, что может свидетельствовать о маку-лярном кровоизлияний. Даже при центральной локализации геморрагий прогноз восстановления зрительных функций после их рассасывания в 80—90 % случаев благоприятими
142
[Pruett R.C. et al., 1987]. Однако в це-лом при ЛТ прогноз следует делать ос-торожно ввиду их нередкого сочетания с субретинальной неоваскуляризацией и очаговыми атрофическими пораже-ниями, постепенно вовлекающими об-ласть макулы. ЛТ и монетовидные кровоизлияния чаще встречаются в глазах с высокой миопией и ПЗО > 28,0 мм, однако отмечены и в 4,3 % [ глаз с ПЗО > 26,5 мм.
Кровоизлияния второго типа связаны сформированием неоваскулярной мембраны — НВМ (см. рис. 7.4). Трещины в I мембране Бруха могут сопровождаться | врастанием новообразованных сосудов из хориокапиллярного слоя через де-фект стекловидной пластинки в субре-[ тинальное пространство. Источником ; геморрагий в этом случае являются не-j состоятельные порозные новообразованные сосуды. Кровоизлияния могут располагаться суб-, интра- или пререти-нально, имеют неправильную форму в [ виде пятен, полос, полуколец с не все-[ гда четкими границами и большие размеры (до 1,5 ДД), могут сопровождаться перифокальным отеком. По мере расса-сывания геморрагии становится виден проминирующий очаг серо-аспидного или зеленоватого цвета, нередко с участками гиперпигментации и отека сет-чатки. Клинически появление НВМ часто сопровождается метаморфопсия-ми, а затем резким снижением зрения и положительной скотомой в поле зрения. Ведущими офтальмоскопическими про-явлениями являются серозная и/или геморрагическая отслойка нейроэпителия и/или пигментного эпителия [Иваниш-ко Ю.Л., 19941.
Миопия является второй по частоте причиной хороидальной неоваскуляри-зации (первая — это возрастная макуло-дистрофия). Неоваскулярная мембрана может располагаться либо под сенсор-эй сетчаткой (субретинальная мембра-либо под пигментным эпителием называемая субпигментная, или хо-зидальная НВМ). Последнюю ввиду ее эытого расположения за пигментным елием, затрудняющего не только тьмоскопическую, но и флюорес-
центно-ангиофафическую диагностику, называют скрытой или оккультной. Только ангиофафия с индоцианиновым зеленым (ICG) на ранних фазах иссле-дования позволяет визуализироваь та-кие мембраны. Отмечено развитие комбинированных НВМ с субретинальны-ми и субпигментными компонентами [Mietz H. et al., 1997]. Типичным для хо-роидальных НВМ является развитие субпигментных геморрагии, которые вы-глядят очень темными и могут быть приняты за увеальную меланому [Eagle R.C., 1999].
Факторами, способствующими не-оваскуляризации при миопии, являются гипоксия сетчатки, развивающаяся вследствие нарушения микроциркуля-ции, и трещины в мембране Бруха, возникающие из-за деформации обо-лочек глаза при растяжении склеры. Гистологическое исследование НВМ у детей показало их идентичность с мем-бранами при возрастной макулодист-рофии, что позволило считать хорои-дальную неоваскуляризацию стерео-типным неспецифическим ответом на специфический стимул [Spraul G.V. et al., 1997]. Таким стимулом может быть окислительный стресс, затрагивающий макулярный пигментный эпителий [Frank R.H. et al., 1999].
Отличительными признаками НВМ при миопии являются ее локализация вблизи фовеолы, относительно не-большие размеры (около j/^ ДД), бы-строе рубцевание с отложением пигмента в виде кольца и образованием перифокального атрофического хо-риоретинального очага.
Меньшую активность процесса и более высокий процент спонтанного рубцевания НВМ при миопии связы-вают с атрофическими изменениями хориокапиллярного слоя, являющего-ся источником роста новообразованных сосудов. Этим же объясняется и редкое появление неоваскуляризации в глазах с ЛТ и монетовидными крово-излияниями при чрезмерном удлине-нии глазного яблока (ПЗО > 28,0 мм) [Ципурская С.С., 1988].
При завершении обратнего разви-
143
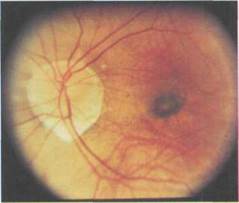
Рис. 7.6. Исход формирования неоваску-лярной мембраны. Пигментированный фиброваскулярный очаг — пятно Фер-стера—Фукса.
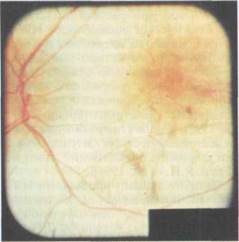
Рис. 7.7. Далеко зашедшая хориорети-нальная атрофия при осложненнои миопии.
тия НВМ на ее месте формируется пигментированный фиброваскулярный очаг: пятно Ферстера—Фукса (рис. 7.6). Однако НВМ склонны к ре-цидивирующему течению, увеличива-ясь по площади, рубцуясь с одной стороны и продолжая создавать геморра-гии с другой. Отмечено, что у больных с пятном Ферстера—Фукса наиболее часто выявляется врожденная или рано приобретенная миопия.
В наиболее тяжелых случаях осложненнои миопии формируется задняя стафилома. Так называют истинное выпячивание (экстазия) склеры в заднем отделе глазного яблока, сопровож-дающееся типичными офтальмоскопическими признаками. В зависимости от локализации B.J. Curtin (1985) различал заднеполюсную, макуляр-ную, перипапиллярную, назальную, нижнюю стафиломы), а также от стадии развития она может варьировать по площади и глубине, иметь более или мёнее четкие и острые края, через которые перегибаются сосуды сетчат-ки. В зоне эктазии наблюдаются гру-бые хориоретинальные изменения, представляющие собой различные комбинации перечисленных выше и в наиболее тяжелых случаях соответст-вующие описанию IV—V стадии изме-нений глазного дна по Аветисову— Флику [Аветисов Э.С., 1999] обшир-ные атрофические очаги, сливающие-ся между собой, со скоплением пигмента в виде глыбок и сохранением ткани сетчатки в виде редких остров-ков. Края стафиломы нередко также вовлекаются в атрофический процесс (рис. 7.7).
He мёнее важными в клинической картине осложненнои миопии являют-ся периферические витреохориорети-нальные дистрофии (ПВХРД). Важ-ность ПВХРД определяется их ролью в возникновении дистрофической отслойки сетчатки. Риск возникновения отслойки сетчатки в глазах с миопией, растянутых как в аксиальном, так и во фронтальном, вертикальном и косых направлениях, увеличивается из-за не-скольких факторов: развития задней отслойки стекловидного тела, периферических хориоретинальных дистро-фий и витреоретинальной тракции.
В образовании ПВХРД принимают участие 3 анатомических субстрата: стекловидное тело, хороидея и сетчат-ка, что и нашло отражение в их назва-нии. Согласно наиболее принятой в нашей стране классификации Е.О. Сак-соновой и соавт. (1979), выделяют сле-дующие виды ПВХРД:
144
|
|
отслойки стекловидного тела) объяс-няет более высокую частоту возникно-вения отслойки сетчатки при симптоматических разрывах. У детей и подростков разрывы выявляются достаточно часто: в 6,4—25 % случаев в зависимости от контингента обследуемых.
Патологическая гиперпигментация может быть выражена по-разному: от легкого диффузного потемнения или пигментных глыбок разной величины и формы до наличня больших пигмен-тированных наложений, которые мо-гут сливаться в широкую полосу между экватором и зубчатой линией. Процесс может сочетаться с витреоретинальной тракцией, которая проявляется серо-ватым налетом на поверхности пиг-ментированных очагов и может явить-ся причиной формирования тракцион-ных разрывов (по некоторым данным, почти в 32 % случаев).
Возникновение указанной формы ПВХРД объясняют пролиферацией пигментного эпителия сетчатки. Одни авторы считают причиной этого биохимические изменения и витреорети-нальную тракцию, другие — аномалии развития пигментного эпителия.
Кистовидная дистрофия встречается почти у всех пациентов с миопией старше 8 лет, а в глазах пожилых людей считается закономерным явлением [Byer N.E., 1999]. Однако она может приводить к формированию атрофиче-ских дырчатых разрывов.
Периферический дегенеративный ре-тиношизис — патологический процесс, в основе которого лежит расслоение сетчатки. В I стадии по крайней пери-ферии глазного дна, чаще всего в ниж-ненаружном квадранте, появляется резко ограниченный участок непро-зрачной сетчатки сероватого цвета, иногда слегка приподнятый. Во II стадии ретиношизис распространяется как к центру, так и по окружности, нередко занимая в виде пояса вею периферическую часть сетчатки. На поверхности пораженной зоны нередко наблюдаются блестящие желтоватые крапинки. (В отличие от картины ре-шетчатой дистрофии они более круп-
146
ные и расположены хаотично на большой площади.) Bill стадии выявляются большие пузыревидные возвыше-ния сетчатки (буллезный ретиношизис), появляются разрывы в его стен-ках, как правило, сначала во внутренней, с последующим развитием в части случаев отслойки сетчатки [Саксоно-ва Е.О. и др., 1975].
Хориоретинальная атрофия типа «бу-лыжной мостовой» чаще встречается в возрасте старше 40 лет и в типичном виде представляет собой округлые желто-белые очаги, расположенные на 1—2 ДД кзади от зубчатой линии, размером от 0,1 до 1,0 ДД. Они могут рас-полагаться поодиночке или группами и имеют тенденцию к слиянию в сплошную полосу с фестончатыми краями, разделенную разным количе-ством пигмента. Хороидальные сосуды часто пересекают область дистрофии сзади. Причиной развития этой дистрофии являются сосудистые изменения, приводящие к дегенерации хо-риоретинального комплекса. Измене-ний стекловидного тела, связанных с этой дистрофией, в отличие от всех прочих не отмечено. Считается, что эта форма ПВХРД не предрасполагает к развитию отслойки сетчатки и даже может выполнять роль барьера при ее возникновении (за счет отложения пигмента, укрепляющего связь сетчатки с хороидеей). Если отслойка вее же захватывает область «булыжной мостовой», то бывшие атрофические очаги из-за резкого истончения сетчатки вы-глядят на фоне отслоенной сетчатки как ярко-красные фокусы (псевдораз-рывы).
Э.С. Аветисов и Л.П. Флик в 1974 г. предложили классификацию цен-тральных хориоретинальных измене-ний при близорукости. В I стадии от-мечается только небольшой конус у диска зрительного нерва. Во II стадии конус увеличивается и исчезают арео-лярные рефлексы в макуле без признаков дистрофических изменений. Стадии III—V отражают нарастающую центральную хориоретинальную дис-трофию от мелких дефектов пигмент-
ного эпителия до развития стафиломы и формирования обширных атрофиче-ских и пигментных очагов [Авети-совЭ.С, 1999].
В начале развития близорукости у детей глазное дно обычно соответствует I стадии, реже — II. Однако дистрофические изменения глазного дна в части случаев встречаются уже в детском возрасте, особенно при врожденной и раноприобретенной близорукости.
Врожденная близорукость — особая форма, которая формируется в период внутриутробного развития плода [Аве-тисовЭ.С. идр., 1988].
Частота миопии у новорожденных составляет 6—15 % [Аветисов Э.С., 1999; Curtin B.J., 1985], a no некоторым данным, до 25—50 % [Grosvenor T., Goss D.A., 1999]. В подавляющем большинстве случаев это преходящая рефракционная миопия новорожденных, обусловленная более сильной преломляющей способностью хрусталика, недостаточным действием цик-лоплегических средств на незрелую цилиарную мышцу, некоторой дис-корреляцией анатомо-оптических элементов рефракции. В течение первых месяцев жизни эта миопия исчезает в результате созревания цилиарной мышцы, уменьшения преломляющей силы роговицы и хрусталика, углубле-ния передней камеры, и к концу 1 года частота миопии у детей составляет 1,4-4,5 % [Аветисов Э.С., 1999; Grosvenor Т., Goss D.A., 1999]. Как правило, это высокая близорукость, которая сохранилась в период эмметропиза-ш. 06 этом свидетельствуёт и совпадение ее частоты с частотой миопии высокой степени, выявляемой у ново-эжденных: 1,0—3,2 % [Аветисов Э.С., 1999; Goldshmidt E., 1969; Curtin B.J., 1985]. Транзиторная миопия новорож-гнных, называемая физиологиче-юй, очевидно, может служить небла-эприятным признаком, предраспола-эщим к развитию приобретенной 4иопии вдальнейшем. Так, например, вечено, что 42 % детей, имевших ри рождении миопию, исчезнувшую
к 3 годам, вновь стали близорукими к 8—9 годам, в то время как среди новорожденных с гиперметропической рефракцией миопия к 9 годам появи-лась только у 10 % [Gwizda J. et al., 1993].
Врожденную близорукость разделя-ют на преходящую, как правило, сла-бую, миопию новорожденных и ис-тинную, или первично врожденную, миопию, выявляемую в возрасте от 1 года до 3 лет. Последняя обычно ха-рактеризуется высокой степенью, увеличением длины переднезадней оси глаза, изменениями на глазном дне, что даёт основание считать ее патологической по своей природе. Врожденная (и появившаяся на первом году жизни) миопия нередко бывает связа-на с системными мезо- и эктодермаль-ными пороками. У таких детей значительно чаще наблюдаются голубые склеры, деформации грудной клетки, плоскостопие, пупочные грыжи, арах-нодактилия, синдром Марфана и другие типы дисплазии соединительной ткани [Curtin B.J., 1985]. А.В. Хватова и соавт. (1993) при обследовании 40 детей с дисплазиями соединительной ткани (синдромы Марфана, Стик-лера—Маршалла, Маркезани) выяви-ли в большинстве случаев миопию (от —8,0 до —20,0 дптр) в возрасте от 1 года до 3 лет. Миопия имела прогрессирую-щий характер, сочеталась с иридодоне-зом (с первых дней жизни), эктопией, подвывихом, вывихом, колобомой хрусталика, деструкцией стекловидно-го тела, голубыми склерами, в ряде случаев — с факоматозами [Хватова А.В. и др., 1993].
М. Tost (1990), указывая на нередкое сочетание осевой миопии с аномалия-ми зрительного нерва (ложный неврит, псевдозастойный сосок, колобома, атипичные конусы ДЗН), расценил это как проявление эктодермальных пороков развития. По его мнению, атипичные, особенно нижние, конусы ДЗН являются результатом неправильной индукции зачатка эктодермы глаза, на-рушения закрытия щели глазного бокала.
147
В то же время нередко встречается и врожденная миопия средней степени. В целом пациенты с врожденной бли-зорукостью представляют гетероген-ную группу, различающуюся по наследственному фону, картине глазного дна, степени функциональных рас-стройств. На ее возникновение и ха-рактер дальнейшего развития может оказывать влияние ряд пре- и перина-тальных факторов, таких как болезни матери (токсикоз беременных, краснуха, алкоголизм), недоношенность, малая масса тела при рождении.
Э.С. Аветисов (1999), Э.С. Аветисов и К.А. Мац (1989) выделяют по проис-хождению 3 формы врожденной мио-пии:
1. Врожденная миопия вследствие дис-
корреляции между анатомическим и
оптическим компонентами рефрак
ци и как результат сочетания относи
тельно длинной оси глаза с относи
тельно сильной преломляющей спо-
собностью его оптических сред
(плавным образом хрусталика). Если
это не сочетается со слабостью скле
ры, то такая близорукость обычно
не прогрессирует: удлинение глаза в
процессе роста сопровождается
компенсаторным уменьшением пре
ломляющей силы хрусталика.
2. Врожденная миопия, связанная со
слабостью склеры и ее повышенной
растяжимостью. Такая близорукость
интенсивно прогрессирует и пред-
ставляет собой одну из наиболее не-
благоприятных в прогностическом
отношении форм.
3. Врожденная миопия при пороках
развития глазного яблока. Миопи-
ческая рефракция, обусловленная
анатомо-оптической дискорреляци-
ей, сочетается в этом случае с раз-
ными видами патологии и анома-
лиями развития глаза (косоглазие,
нистагм, колобомы оболочек глаза,
подвывих хрусталика, частичное его
помутнение, частичная атрофия
зрительного нерва и др.). При усло-
вии ослабления склеры такая близо
рукость может прогрессировать
148
[Аветисов Э.С. и др., 1989; Аветисов Э.С, 1999]. A. Franceshetti и со-авт. [цит. no Curtin B.J., 1985] no картине глазного дна различают 3 типа первичной врожденной высокой близорукости:
1. Врожденная стационарная мио
пия без изменений глазного дна:
как крайний вариант нормально
го распределения рефракции; по
природе рефракционная.
2. Врожденная миопия пигментного
типа: гиперпигментация макулы в
сочетании с маленькими дисками,
сужение ретинальных сосудов;
часто сочетается с нистагмом.
3. Альбинотический тип (вторичный
по отношению к тотальной или
локальной гипоплазии и истонче-
нию пигментного эпителия сет-
чатки); этот тип соответствует
описанию М. Mawas (1934), кото-
рый считал наиболее характер-
ным для врожденной миопии аль
бинотический тип глазного дна
вследствие дефектного пигмент
ного эпителия: побледнение глаз
ного дна, хорошо просматриваю-
щиеся сосуды хороидеи, в ряде
случаев сочетание с частичней ат-
рофией ДЗН [цит. no Curtin B.J.,
1985].
Характерным признаком врожденной миопии является сочетание с врожденными изменениями глазного дна, связанными с аномалиями развития глаза. К ним относят изменения формы ДЗН, чаще в виде горизонтального или вертикального овала, уменьшение размеров диска, частичную его атро-фию, гиперпигментацию макулярной зоны (так называемая темнопигменти-рованная макула), альбинизм. Наряду с этим выделяют приобретенные изменения глазного дна, связанные с удлинением ПЗО в процессе прогрессиро-вания близорукости и свойственные как врожденной, так и приобретенной миопии: конусы, супертракцию оболочек у края диска, мозаичность и побледнение глазного дна, а также те или иные формы нейтральных и перифе-
рических хориоретинальных дистро-фий. He исключают, что конусы, моза-ичность и побледнение могут быть врожденными или появиться на пер-вом году жизни как следствие внутри-утробного растяжения оболочек.
Из 230 глаз с врожденной миопией, исследованных в Московском НИЙ глазных болезней им. Гельмгольца, врожденные изменения глазного дна выявлены в 153 (66,5 %). Изменения диска зрительного нерва (рис. 7.9 и 7.10) обнаружены в 98 (42,6 %) глазах: в виде вертикального овала в 30 (в ряде случаев в сочетании с косым вхождением в склеру), в виде горизонтального овала в 15, неправильной формы (в виде треугольника или четырехугольника со сглаженными углами) в 35 глазах. Диск нормальной округлой, слегка вытянутой в вертикальном направле-нии формы, но уменьшенный в размерах отмечен в 18 глазах. При этом мо-нотонная окраска диска зрительного нерва наблюдалась в 67 (29,1 %) глазах, умеренная его деколорация — в 21 (9,1 %). Изменения макулярной области (см. рис. 7.9 и 7.11) выявлены в 55 (23,9 %) глазах: равномерная усиленная пигментация макулы в 24 (10,4 %), гипоплазия макулярной области в 17 (7,4 %), «паркетное» («тигроидное») дно в 14 (6,1 %) [Тарутта Е.П., 1993].
В то же время при приобретенной миопии только в 6 глазах из 981 (0,6 %) отмечены изменения ДЗН: в виде косо ориентированного овала в 2, в виде вертикального овала в 3, миелиновые волокна в 1. Ни в одном случае эти изменения не сопровождались снижением корригированной остроты зрения.
Наличне конусов у ДЗН также весь-ма характерно для врожденной миопии: в указанной группе они наблюда-лись в 96,9 % случаев, отсутствуя только в 7 глазах у 4 детей в возрасте от 7 до 12 лет с миопией средней и высокой степени. Диагноз врожденной миопии во всех случаях основы вал ся на раннем (до 3 лет) ее выявлении и длительном наблюдении в Московском НИЙ глазных болезней им. Гельмгольца. Характерно, что максимальная корри-
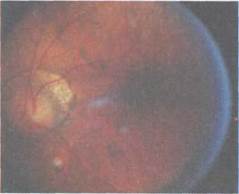
Рис. 7.9. Врожденная миопия. Атипич-ная форма и локализация конуса диска зрительного нерва. Темнопигментиро-ванная макула. Макулярный рефлекс отсутствует.
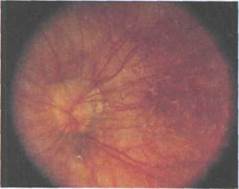
Рис. 7.10. Врожденная миопия. Атипич-ная форма диска зрительного нерва.
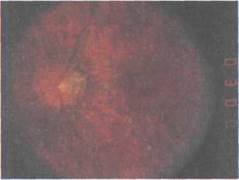
Рис. 7.11. Врожденная миопия. Атипич-ная форма диска зрительного нерва. Тем-нопигментированная макула.
149
гированная острота зрения у всех 4 больных была снижена до 0,5—0,6, что подтверждает дифференциально-диагностическое значение этого пока-зателя для врожденной миопии [Аве-тисов Э.С., Мац К.А., 1989].
Локализация и размеры конусов при врожденной миопии также часто име-ют специфические особенности. Обычное для приобретенной близору-кости расположение конуса с височ-ной стороны ДЗН при врожденной миопии не является преобладающим. Отмечены круговые (35,2 %), нижние, нижневисочные (16,1 %), назальные (4,3 %) конусы. При этом горизонталь-но-овальная форма ДЗН сочетается, как правило, с круговыми конусами, a вертикально-овальная — с височными. Округлые и атипичные диски сочета-ются со всеми видами конусов.
Характерными для врожденной миопии являются и большие размеры конусов. Так, конусы величиной более Yi ДД отмечены в 46,9 % случаев уже в детском возрасте, а в 27,4 % глаз веей группы они превышали 1 ДД [Тарут-та Е.П., 1993].
На фоне описанных врожденных изменений у больных с врожденной близорукостью с возрастом и по мере ее прогрессирования часто развивают-ся приобретенные дистрофические из-менения. Их клиническая картина не отличается от картины известных форм ЦХРД и ПВХРД при приобретенной миопии. Для конкретизации диагноза рекомендуется указывать «врожденная миопия с изменениями на глазном дне» [Ковалевский Е.И., 1995] для обозначения врожденных изменений и «осложненная центральной и/или периферической хориорети-нальной дистрофией» для обозначения дистрофического процесса.
Присущим врожденной миопии признаком является снижение оптимальной корригированной остроты зрения. Э.С. Аветисов (1999) указывал, что прич и нами этого снижения являются органические изменения в зри-тельной системе и относительная амб-лиопия, связанная как с этими изме-
150
нениями, так и с длительным проецированием на сетчатку неясных изобра-жений.
Другой характерной чертой врожденной миопии является частое (более чем в половине случаев) сочетание с астигматизмом [Юсупов А.А., 1992; Аветисов Э.С, 1999]. Чаще наблюдает-ся астигматизм прямого типа, но встречается и обратный, и с косыми осями (оба главных меридиана лежат в секторах от 30 до 60° и от 120 до 150° по шкале ТАБО). Величина астигматизма, как правило, превышает 2,0 дптр и может достигать 5,0—6,0 дптр. В последнем случае нередко несовпадение величины общего и роговичного астигматизма, очевидно за счет хруста-ликового компонента.
В глазах с врожденной миопией чаще, чем обычно, встречаются изменения формы хрусталика (сферофакия, лентиконус), а также врожденные, час-тичные или полные катаракты.
Одной из важных особенностей врожденной миопии является отсутствие параллелизма между остротой зрения, с одной стороны, и степенью миопии и картиной глазного дна — с другой. Может наблюдаться низкая острота зрения с коррекцией при относительно невысокей степени миопии и нормальном глазном дне и, наоборот, довольно высокая острота зрения с коррекцией при высоких степенях миопии с типичными врожденными изменениями глазного дна [Аветисов Э.С, Мац К.А., 1989].
При позднем (в 5—6 лет) обнаруже-нии врожденной миопии нередко можно наблюдать одинаковую остроту зрения без коррекции и с оптимальной коррекцией по данным объективной рефрактометрии. При этом некорри-гированная острота зрения оказывает-ся неожиданно высокой (например, 0,1 при миопии 10,0 дптр с астигматизмом), что свидетельствуёт об адапта-ционных механизмах, позволяющих различать изображение в кругах свето-рассеяния, и в то же время оптимальная корригированная острота зрения при первом обследовании также равна
0,1. Как уже указывалось, это снижение вызвано комплексом органических и функциональных причин. Оп-ределить долю влияния каждой из них по офтальмоскопической картине, как правило, не удается. Исключение со-ставляют случаи выраженной тяжелой патологии, например выраженная ат-рофия, гипоплазия ДЗН, синдром «вьюнка», колобома зрительного нерва или оболочек, аплазия макулы, когда острота зрения с коррекцией не пре-вышает нескольких сотых. Сущест-; вующие способы дифференциальной диагностики функциональной сохран-ности зрительного анализатора при врожденной миопии нередко оказыва-
■ ются малоинформативными. Электро
физиологические показатели у боль-
I шей части детей с врожденной миопи-I ей находятся в пределах нормы. Маку-[ лярная электроретинограмма (ЭРГ) у
■ 75 % обследованных бывает нормаль-
I ной. В ряде случаев наряду с нормаль-
I ной ЭРГ встречается снижение клас-
|сических а- и b-волн ЭРГ, ранних ре-
I цепторных и осцилляторных потен-
I циалои, что свидетельствуёт об изме-
I нениях н наружных слоях сетчатки
I [Шамшинова A.M., Мац К.А., 1986;
Иветисов Э.С., Мац К.А., 1989].
1 Ретинальная острота зрения, опре-Щвленная с помощью гелий-неонового ■изера, при врожденной близорукости ■рачительно выше обычной и нередко Иэстигает нормальных значений. Бо-Ве информативиым оказался разрабо-I танный В.Э. Аветисовым и соавт. I (1992) способ сочетанной ретиномет-I рии с помощью гелий-неонового ( X = ■638 нм) и гелий-кадмиевого ( X = ■41,6 нм) лазеров. Этот способ позво-I ляет оценить долю участия органиче-Ккого фактора и определять порог, до ■рторого может повыситься острота Врения в результате лечения.
■В последние годы важную роль в вы-^■щении амблиопии играёт регистрация I зрительных вызванных потенциалов
(ЗВП), отражающих суммарную био-■кктрическую активность нейронов ■иггельной проекционной области
коры головного мозга и позволяющих
оценить пределы разрешения зритель-ной системы. При врожденной миопии выявлены изменения паттерн-ЗВП, от-ражающие нарушения пространственной контрастной чувствительности в низкочастотном диапазоне. Эти нарушения при рефракционнои амблиопии у больных с высокой врожденной бли-зорукостью носят в основном тот же характер, что и при обскурационной амблиопии [Шпак А.А., 1996].
В то же время даже при перечислен-ных выше органических изменениях — аномалиях развития зрительного нерва — острота зрения может варьиро-вать в очень широком диапазоне: от нескольких сотых до 1,0. Стольже широко варьируют и ЗВП. Отмечено, что такие колебания остроты зрения, в частности у детей с синдромом косого вхождения ДЗН, во многом зависят от продолжительности зрительней де-привации и тяжести рефракционнои амблиопии, развивающейся у детей при отсутствии адекватной оптической коррекции [Мосин И.М., 2001].
Лечебные меры
При врожденной близорукости
Оптическая коррекция при врожденной миопии является наиболее важ-ным лечебным и профилактическим пособием. Она призвана не только компенсировать ошибку рефракции, но и создать условия для развития зрительного анализатора, профилактики и лечения амблиопии. Даже в случае вы-раженных изменении на глазном дне и неблагоприятных результатов психофизических и электрофизиологических исследований веем детям с врожденной близорукостью показана как можно более ранняя и полная коррекция аметропии. Э.С. Аветисов и К.А. Мац (1989) рекомендуют постепенно, с интервалом 3—4 мес, увеличивать силу линз до значений, соответствую-щих величине рефракции, определен-ной одним из объективных способов в условиях циклоплегии. Учитывая ранний возраст ребенка, лучшим циклоп-легическим средством следует считать
151
0,3 % раствор атропина, а лучшей методикой — скиаскопию. При возможности целесообразно сочетать ее с ав-торефрактометрией для уточнения вы-раженности и осёй астигматизма. Последний рекомендуется тщательно корригировать начиная с 1,0—1,5 дптр. При высоких степенях астигматизма возможна легкая гипокоррекция сферического компонента в пределах 2,0 дптр. Учитывая свойственное детям с врожденной близорукостью значительное ослабление аккомодации, помимо полной коррекции вдаль, в школьном возрасте рекомендуется назначение второй пары очков для близи — на 2,0—3,0 дптр слабее [Авети-сов Э.С., Мац К.А., 1989].
Очки являются первым и основным корригирующим средством при врожденной миопии. Дети раннего возраста хорошо переносят разницу в силе кор-ригирующих стекол до 6,0 дптр и цилиндры до 5,0 дптр [Ковалевский Е.И., 1995], что делаёт очковую коррекцию методом выбора даже при анизометро-пической миопии и высоком астигматизме. В более старшем возрасте (в 3—5 лет) лучшим методом коррекции являются контактные линзы, а при односторонней врожденной высокой миопии контактную коррекцию следует признать методом выбора.
Наряду с ранней и адекватной оптической коррекцией детям с врожденной близорукостью показано проведение курсов плеоптического лечения. При-меняют практически вее существующие методы лечения амблиопии в разных комбинациях: локальный засвет сетчат-ки, лазерплеоптику, лазерстимуляцию, лечение на аппарате «Амблиокор», цве-тоимпульсную терапию. Положитель-ные результаты у детей с врожденной миопией даёт также чрескожная элек-тростимуляция зрительного нерва. Эф-фективность этого метода объясняют поляризующим действием электрического тока на зрительныи нерв и сетчат-ку, направленной активацией зритель-ной коры, а также иммуномодулирую-щим действием [Мосин И.М., 2001; По-номарчук B.C. и др., 2001].
152
Е.И. Сидоренко и соавт. (2001) со-общили об удовлетворительных результатах лечения сочетанием чре-скожной электростимуляции и назальных инстилляций ноотропного препарата семакса при амблиопии.
В отличие от приобретенной врожденная близорукость нередко бывает стабильной, особенно у детей дошко-льного возраста. В ряде случаев отме-чается некоторое ослабление рефрак-ции в результате действия эмметропи-зирующих факторов, главным образом уплощения хрусталика. Отмечено также, что стабильной чаще всего бывает врожденная миопия очень высокой степени [Аветисов Э.С., Мац К.А., 1989; Юсупов А.А., Бабаев С.А., 2001; Curtin B.J., 1985]. Однако в 48-75 % случаев врожденная близорукость при-обретает прогрессирующий характер, примерно в половине из них — быстро прогрессирующий. Прогрессирование обычно начинается в школьные годы и может продолжаться в течение веей жизни с периодами временной стаби-лизации. Многие авторы подчеркива-ют, что увеличение ПЗО у значительной части детей с врожденной и приобретенной дегенеративной миопией продолжается даже на фоне стабильных показателей рефракции, компен-сируясь уплощением хрусталика и от-части роговицы.
При прогрессирующей врожденной миопии дистрофические осложнения развиваются раньше, чем при приобретенной.
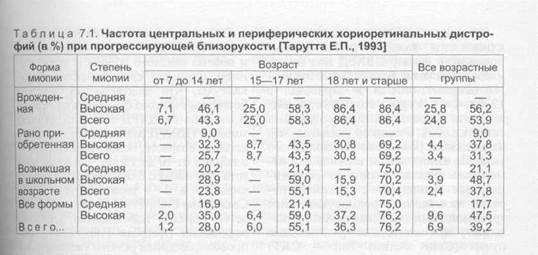
Сравнительная оценка состояния центральных и периферических отделов глазного дна 1211 глаз 608 больных в возрасте от 7 до 49 лет с разными формами прогрессирующей близору-кости (табл. 7.1) показала, что ЦХРДу детей встречались только при врожденной миопии (6,7 %), а у подростков — при врожденной (25 %) и рано приобретенной (8,7 %). При миопии, возникшей в школьном возрасте, ЦХРД не обнаружены ни в одном из 535 глаз у детей и подростков и встречались только у взрослых. Минимальный возраст, в котором были выявле-
|
|
ны ЦХРД, составил при врожденной близорукости 12 лет, при рано приоб-ретенной — 17 лет, при школьной — 23 года [Тарутта Е.П., 1993]. Однако в целом можно считать, что миопия, возникшая в школьном возрасте, ос-ложняется ЦХРД, за редким исключением, после 30 лет.
Помимо более раннего появления, ЦХРД при врожденной миопии отли-чаются и более тяжелым течением. Так, геморрагическая форма ЦХРД развивается уже в детском возрасте. Как правило, это монетовидные кро-воизлияния, связанные с формированием ЛТ. При врожденной высокой прогрессирующей близорукости у подростков и даже у детей можно ветре-тить и субретинальные НВМ. В целом на долю наиболее неблагоприятной геморрагической формы при врожденной близорукости приходится более 30 % всех ЦХРД, при рано приобре-тенной — 16,7 %, при возникшей в школьном возрасте — 6,7 % [Тарутта Е.П., 1993]. Врожденная прогрессирующая близорукость со времёнём становится осложненной в абсолют-ном большинстве случаев. Так, частота различных форм ЦХРД у взрослых па-циентов с продолжающимся прогрес-сированием близорукости при врожденной форме составила 86,4 %, тогда как при рано приобретенной и возникшей в школьном возрасте — соответственно 30,8 и 15,3 %.
ПВХРД при всех формах близорукости встречаются уже в детском возрасте. У детей с врожденной миопией они встречаются достоверно чаще (более 40 %), чем при рано приобретенной (25,7 %) и возникшей в школьном возрасте (23,8 %). С возрастом и прогрес-сированием миопии увеличивается число глаз с ПВХРД при сохранении безусловного лидерства врожденной близорукости: в группе взрослых паци-ентов частота ПВХРД при этой форме достигает 86 %. При этом в отличие от приобретенной миопии, для которой характерно более частое поражение периферии сетчатки, при врожденной близорукости у взрослых изменения, как правило, обнаруживаются и в центре, и на периферии глазного дна. Очевидно, это свидетельствуёт о гене-рализованном дистрофическом процессе в оболочках глаза.
По нашим данным, наиболее ранний возраст возникновения ПВХРД при врожденной и рано приобретенной миопии составил 7 лет, при возникшей в школьном возрасте — 9 лет. Наиболее ранними формами ПВХРД у детей при врожденной миопии явля-ются диффузная и очаговая хориоре-тинальная атрофия, витреоретиналь-ные сращения, при врожденной и приобретенной — плоский периферический ретиношизис, решетчатая дис-трофия, изолированные разрывы сетчатки.
153
N.E. Byer (1999) выделяет среди клинически важных регматогенных поражений форму ПВХРД под названием «кистозные ретинальные пучки». Их впервые описал и зарисовал в 1936 г. Фогт (Vogt), который установил их связь с тракционными разрывами сетчатки. Г.Л. Стариков указы вал, что их называли розетками стекловидного тела. По клинической картине эти из-менения соответствуют витреорети-нальным сращениям с тракцией, нередко называемым формирующимися тракционными разрывами. Автор ука-зывает, что кистозные ретинальные пучки (Cystis Retinal Tuft - CRT) представляют собой врожденные ано-малии развития периферии сетчатки, при которых плотные скопления гли-альной ткани формируются в маленькие отграниченные узелки или пучки на поверхности сетчатки, тесно связанные с прилежащим стекловидным телом и скрытые в криптах или стекло-видном теле. При возникновении вит-реоретинальной тракции они обнару-живаются и могут вызывать тракцион-ные разрывы. Считают, что 36 % пара-оральных тракционных разрывов про-исходят из CRT. В то же время отмеча-ют, что эти мелкие разрывы, клапан-ные и с крышечками, не являются причиной развития отслойки сетчатки.
Длительное динамическое наблюдение за группой детей с не осложненной в начале исследования миопией позво-лило обнаружить появление подобиых витреоретинальных сращений в 3 глазах у 2 пациентов с врожденной близоруко-стью в возрасте 9—10 лет. При тщательной регулярной (2 раза в год) офтальмоскопни, проводимой с 7—8-летнего возраста, эти изменения раньше не обнару-живались. В дальнейшем в течение по-следующих 2 лет после первого выявле-ния на месте этих сращений сформиро-вались разрывы сетчатки (во всех 3 слу-чаях с крышечкой).
Частота ПВХРД достоверно нарас-тает с возрастом, увеличением степени и скорости прогрессирования близору-кости и длительности течения заболе-вания.
Отмечена связь частоты и выражен-ности ПВХРД с увеличением размера и объема глазного яблока и уменьшением опорных свойств склеральной капсулы, что подтверждает участие биомеханического фактора в их генезе. В отличие от ЦХРД при всех формах миопии ПВХРД развиваются именно в детском возрасте, особенно активно — в период от 10 до 15 лет, когда их частота у больных с близорукостью увели-чивается в 3—4 раза [Тарутта Е.П., Саксонова Е.О., 1991]. В этот период у детей нередко наблюдается «скачок» рефракции [Авербах Г.И., 1989], со-провождающийся резким увеличением размеров глазного яблока, т.е. растяжением его оболочек. Возможно, оп-ределенную роль в этих процессах играёт относительный дисбаланс стеро-идных гормонов, особенно половых (тестостерона и 17(3-эстрадиола), вы-явленный у пациентов с миопией [Балакко-Габриэли К., 1990; Cur-tin B.J., 1985]. Дисбаланс стероидных гормонов, оказывающих влияние на метаболизм коллагена, может приво-дить к уменьшению опорных свойств склеральной капсулы, ее растяжению как в сагиттальном, так и в других на-правлениях и, таким образом, играть существенную роль в патогенезе осложненной миопии.
Более раннее возникновение ПВХРД по сравнению с ЦХРД может быть обусловлено тем, что прогресси-рование миопии на начальных этапах ее развития происходит за счет растя-жения экваториальных отделов склеры, и только позже в этот процесс во-влекается задний полюс глаза. Извест-но, что в норме постнатальные рост и увеличение размеров глаза происходят в основном за счет области экватора склеры [Tso M.O.M., Friedman Е., 1968]. Возможно, именно с этим связан факт обнаружения ПВХРД при всех видах рефракции. По мнению ряда исследователей, при миопии увеличение переднезадней оси осуществ-ляется с большим вовлечением экватора. При этом с очевидностью доказано не только удлинение, но и «расшире-
154
ние» миопического глаза, т.е. увеличение его размера происходит в основном в зоне экватора и наиболее актив-но — у детей и подростков при всех формах миопии [Николов В.Б., 1979; Аветисов Э.С. и др., 1988; Свирин А.В., 1991; Иомдина Е.Н., 2000].
Дополнительное подтверждение эти факты получили в работе С.Н. Епише-вой (2001). Автор измеряла оптическим способом диаметр склерального кольца на расстоянии 4 мм от лимба и установила, что при миопии, проте-кающей с растяжением не только заднего, но и переднего отдела склераль-ной капсулы, отмечались более выра-женные изменения и в центре, и на периферии глазного дна. Подтверждая эмметропизирующую роль увеличения диаметра склерального кольца и связанного с ним уплощения хрусталика, автор считаёт этот процесс при про-- грессирующей миопии не компенса-торным, а неблагоприятным в прогно-| стическом отношении, поскольку он [ нивелирует процесс увеличения ПЗО, I скрывает истинное прогрессирование | близорукости, после чего часто насту-пает феномен «скачка» рефракции.
Помимо дистрофических процессов в склеральной капсуле, в патогенезе I осложненной миопии играют роль ге-I модинамические, гидродинамические, I метаболические нарушения в оболоч-; ках глаза, генетический фон. Изуче-| нию этих факторов уже многие годы I уделяется самое пристальное внима-I ние, однако четкого ответа на вопрос, I почему в одних случаях течение мио-; пии приобрстает патологический ха-I рактер с развитием осложнении, а в | других — нет, до сих пор не получено, а следовательно, нет ответа и на дру-[ гой, еще более важный вопрос: станет I лисо времёнём осложненной близору-I кость у конкретного ребенка. Извест-| ные клинические наблюдения, пока-I зывающие, что чем раньше началась I миопия, тем дольше и быстрее ее про-I грессирование и хуже прогноз, безусловно, обращают внимание врача на определенную группу пациентов, но явно недостаточны. Далеко не всякая
рано приобретенная и даже врожденная миопия становится дегенератив-ной. В то же время развитие тяжелых осложнении в центре и на периферии глазного дна, со времёнём приводящих к инвалидности, отмечено и при миопии, возникшей в школьном возрасте [Тарутта Е.П., 1993; Аветисов Э.С, 1999; Шерго Осман, 2002]. Поэтому следует признать оправданным пристальное внимание отечественных оф-тальмологов к любой прогрессирую-щей близорукости, особенно у детей. Главной целью лечебных мероприятий справедливо считается не избавление от очков или повышение некорриги-рованной остроты зрения, а именно торможение и профилактика прогрес-сирования близорукости.
Дата добавления: 2020-12-12; просмотров: 164; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!