Строение карбоксильной группы
Карбоновые кислоты
Карбоновые кислоты - класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп COOH.
R ( COOH ) n
Классификация карбоновых кислот.
а) по характеру углеводородного радикала:
1) предельные (насыщенные) *HCOOH метановая, муравьиная кислота
*CH3COOH этановая, уксусная кислота
2) непредельные *СН2=СНСООН акриловая кислота
3) ароматические *С6Н5СООН – бензойная кислота
б) по числу карбоксильных групп в молекуле
 1) Одноосновные
1) Одноосновные
метановая, муравьиная кислота

этановая, уксусная кислота
| 2) Двухосновные HOOC – COOH щавелевая кислота | ||
|
3) Многоосновные
| ||
Предельные одноосновные карбоновые кислоты.
CnH2n+1COOH ( CnH2nO2 ) .
Гомологический ряд
| Формула | Название кислоты R-COOH | Название остатка RCOO- | |
| систематическое | тривиальное | ||
| HCOOH | метановая | муравьиная | формиат |
| CH3COOH | этановая | уксусная | ацетат |
| C2H5COOH | пропановая | пропионовая | пропионат |
| C3H7COOH | бутановая | масляная | бутират |
| C4H9COOH | пентановая | валерьяновая | пентаноат |
| C5H11COOH | гексановая | капроновая | гексаноат |
| C7 | гептановая | энантовая | гентаноат |
| C8 | каприловая | октаноат | |
| C9 | пеларгоновая | нонаноат | |
| C10 | каприновая | деканоат | |
| C15H31COOH | гексадекановая | пальмитиновая | пальмитат |
| C17H35COOH | октадекановая | стеариновая | стеарат |
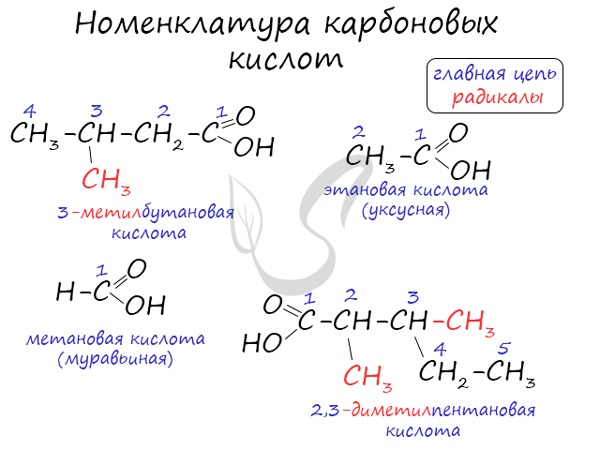
Номенклатура карбоновых кислот
|
|
|
Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота.
Чтобы указать положение заместителя (или радикала), нумерацию углеродной цепи начинают от атома углерода карбоксильной группы. Например, соединение с разветвленной углеродной цепью (CH3)2CH-CH2-COOH называется 3-метилбутановая кислота, СН3-С(СН3)2-СООН — 2,2-диметилпропановая кислота.
Для органических кислот широко используются также тривиальные названия, которые обычно отражают природный источник, где были впервые обнаружены эти соединения (см.тривиальные названия).
Изомерия карбоновых кислот
I . Структурная
а) изомерия углеродного скелета (начиная с C4)

б) межклассовая со сложными эфирами R- CO – O- R1 (начиная с C2)
Например: для С3Н6О2
CH3-CH2-COOH пропионовая кислота
СH3-CO-OCH3 метиловый эфир уксусной кислоты
II . Пространственная
а) Оптическая
Например:

Физические свойства предельных одноосновных кислот
Низшие члены этого ряда (С1 –С10) при обычных условиях представляют собой жидкости, обладающие характерным острым запахом, растворимые в воде. Муравьиная, уксусная и пропионовая кислоты смешиваются с водой неограниченно. С увеличением молекулярной массы растворимость кислот в воде уменьшается.
|
|
|
Высшие кислоты с числом С-атомов больше 11 –твёрдые вещества, нерастворимые в воде, без запаха.
Температуры кипения и плавления кислот значительно выше чем у соответствующих спиртов. С ростом молекулярной массы температура кипения и плавления растёт.
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.


Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы – карбонил >C=O и гидроксил -OH, взаимно влияющие друг на друга:

Для насыщенных монокарбоновых кислот характерна высокая химическая активность. Это определяется, главным образом, реакциями карбоксильной группы (разрыв связей O - H или C - O ), а также реакциями замещения H -атомов при α-С атоме.
Дата добавления: 2020-04-25; просмотров: 75; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
