II . Взаимодействие со сложными веществами.
1. Медь стоит в ряду напряжений правее водорода, поэтому не реагирует с разбавленными соляной и серной кислотами, но растворяется в кислотах – окислителях:
3Cu + 8HNO3(разб.) → 3Cu(NO3)2 + 2NO↑ + 2H2O
Cu + 4HNO3(конц.) → Cu(NO3)2 + 2NO2↑+ 2H2O
Cu + 2H2SO4(конц.) → CuSO4 + SO2↑+2H2O
2. Вытесняет из солей правее стоящие в ряду напряжений металлы:
Cu + Hg(NO3)2 → Cu(NO3)2 + Hg↓
3. Медь растворяется в водном растворе аммиака в присутствии кислорода воздуха с образованием гидроксида тетраамминмеди (II): 2Cu + 8NH3 + 2H2O + O2 = 2[Cu(NH3)4](OH)2.
4. Восстановительные свойства. Медь окисляется оксидом азота (IV) и хлоридом железа (III):
2Cu + NO2 = Cu2O + NO;
Cu + 2FeCl3 = CuCl2 + 2FeCl2.
Получение.
1. Восстановлением из оксидов углём или оксидом углерода (II): CuO + C 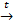 Cu + CO
Cu + CO
CuO + CO 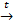 Cu + CO2
Cu + CO2
2. При электролизе растворов солей меди: 2CuSO4 + 2H2O → 2 Cu + O 2 + 2H2SO4
3. Из сульфидных руд: а) обжигают 2Cu2S + 3O2  2Cu2O + 2SO2
2Cu2O + 2SO2
б) сплавляют оксид с сульфидом: 2Cu2O + Cu2S → 6Cu + SO2
Применение.
Изготовление проводов и различных сплавов – бронзы, латуни, дюралюминия.
Соединения одновалентной меди
Оксид меди( I ) С u 2 O
Физические свойства: твердое вещество красного цвета, нерастворимое в воде. В природе встречается в виде минерала куприта.
|
|
|
Химические свойства: Сu2O – имеет слабовыраженные амфотерные свойства с преобладанием основных.
1. Взаимодействует с растворами щелочей с образованием гидроксокомплексов:
Cu2O + 2NaOH + H2O = 2Na[Cu(OH)2].
2. В водных растворах аммиака образует гидроксид диамминмеди (I):
Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH.
3. С соляной кислотой взаимодействует с образованием дихлорокупрата (I) водорода:
Cu2O + 4HCl = 2H[CuCl2] + H2O.
4. С бромоводородом и йодоводородом образует соли меди (I):
Cu2O + 2HBr = 2CuBr + H2O;
Cu2O + 2HI = 2CuI + H2O.
5. В разбавленной серной кислоте диспропорционирует, образуя сульфат меди (II) и металлическую медь: Сu2O + H2SO4 → CuSO4 + H2O + Cu↓
6. При нагревании восстанавливается водородом, угарным газом и активными металлами:
Сu2O + Н2 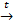 2Сu + H2O
2Сu + H2O
Cu2O + CO = 2Cu + CO2;
|
|
|
Cu2O + Mg = 2Cu + MgO.
7. При сильном нагревании на воздухе превращается в СuO: 2Сu2O + О2 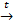 4СuO
4СuO
8. При более сильном нагревании разлагается на простые вещества: Сu2O 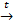 2Cu + O2↑
2Cu + O2↑
Получение.
1. Получают восстановлением соединений меди (II), например, глюкозой в щелочной среде:
2CuSO4 + C6H12O6 + 5NaOH → Cu2O↓ + 2Na2SO4 + C6H11O7Na + 3H2O
2. При разложении гидроксида меди(I): 2CuOH  Сu2O + H2O
Сu2O + H2O
3. При нагревании до 1100°С оксида меди (II): 4CuO = 2Cu2O + O2
Гидроксид меди( I ) CuOH
Физические свойства: неустойчивое, плохо растворимое в воде вещество желтого цвета, в свободном состоянии не выделен.
Химические свойства: CuOH – слабое основание.
1. Нестойкое соединение, легко разлагается: 2CuOH  Сu2O + H2O
Сu2O + H2O
2. Взаимодействует с кислотами: CuOH + HCl → CuCl + H2O
3. На воздухе легко окисляется до Cu(OH)2 : 4CuOH + О2 + 2H2O → 4 Cu(OH)2
Получение.
1. Действием щелочи на соли меди(I): CuCl + NaOH → CuOH↓ + NaCl
Дата добавления: 2019-02-22; просмотров: 322; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
