Хімічні реактиви, прилади та посуд
Реактиви:
· Насичений розчин (NН4)2S04.
· 20 % розчин аміачної води.
· 75 % розчин сірчаної кислоти.
· 0,5 мол/дм3 розчин сірчаної кислоти.
· 0.5 мол/дм3 розчин NaОН.
· Метилоранж.
Прилади і матеріали:
· Нейтралізатор на 250 см3. 
· Поглинальна склянка (2 шт.).
· Термометр на 100 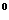 С.
С.
· Мірна колба на 100 см3
· Бюкс.
· Піпетка на 10 см3.
· Колба Ерленмейєра на 250 см3.
· Колба Бунзена, лійка Бюхнера.
· Фільтрувальний папір.
Опис лабораторної установки
Нейтралізацію розчину сірчаної кислоти проводять сумішшю аміака з повітрям. Як нейтралізатор (1) застосовується конічна колба закрита пробкою з трьома отворами в які вставлені термометр і дві трубки для вводу і виводу суміші аміку з повітрям. Через поглинальну склянку (2), де знаходиться розчин аміаку, відсисається повітря, яке насичається аміаком і надходить у нейтралізатор (1). Далі повітря з залишками аміаку донейтралізуються у склянці (3), де розташован розчин 1М Н2SO4. До відводу склянки (3) приєднан водоструминний насос яким відсмоктують повітря.
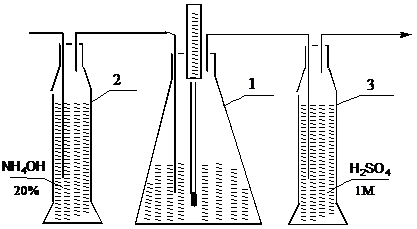
1 – нейтралізатор; 2 - поглинальна склянка; 3 – склянка донейтралізатор
Рисунок9.1 - Схема лабораторної установки
Послідовність виконання роботи
У поглинальну склянку 2 наливають 100-200 см3 20%-ного розчину аміаку. Готують суміш насиченого розчину сульфату амонію і 75%-ної сірчаної кислоти з таким розрахунком, щоб зміст Н2SO4 у суміші склав приблизно 25%, що відповідає пусковим умовам у заводському процесі. Для приготування суміші в порцелянову склянку ємністю 0,5 дм3 наливають 100 см3 насиченого розчину сульфату амонію і додають обережно, при помішуванні 35 см3 75%-ної сірчаної кислоти. З отриманої суміші відбирають пробу (3-5 см3) для визначення кислотності вихідного розчину, суміш що залишилася завантажують у нейтралізатор 1. У склянку 3 наливають 100-200 см3 0.1М Н2SO4 . До склянки 3 приєднують водоструминний насос і ведуть дослід до одержання осаду сульфату амонію. Отриманий осад (NH4)2SO4 відфільтровують на водоструминному насосі, промивають маточним розчином, залишають сушитися.
|
|
|
Опрацювання результатів
Визначення змісту летучого аміаку в аміачній воді:
Зміст летучого аміаку визначають до і після досліду, а потім розраховують кількість аміаку, витраченого на одержання сульфату амонію.
Визначення роблять прямим титруванням. Відбирають бюреткою 10см3 аміачної води, поміщають у мірну колбу на 100 см3 у яку заздалегідь наливають до половини об’єму дистильовану воду, потім доводять рівень до мітки і добре збовтують. Відібравши піпеткою 10 см3 розчину в колбу, де вже знаходиться 25-30 см3 дистильованої води, додають 1-2 краплі метилоранжу і титрують розчином Н2SO4
|
|
|
Процентний вміст аміаку в аміачній воді розраховують по формулі:
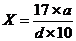 , (9.3)
, (9.3)
де: Х - вміст аміаку в аміачній воді, %:
а - кількість кислоти, що пішла на титрування, см3;
а 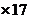 - зміст NH3 у грамах у 1 дм3 досліджуваного води;
- зміст NH3 у грамах у 1 дм3 досліджуваного води;
d - питома вага досліджуваної аміачної води при 20 °С.
Дата добавления: 2018-08-06; просмотров: 285; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
