Фториды ксенона: получение, строение молекул и химические свойства.
Фториды ксенона
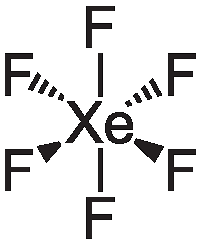
Xe + PtF6 = Xe[PtF6]
Xe + F2 = (XeF2;XeF4;XeF6) в зависимости от соотношений, температуры и давления
XeF6 + BF3 = XeF6*BF3
XeF2 + 2SbF5 = Xe[SbF6]2
XeF6 + CsF = Cs[XeF7]
Гидролиз:
2XeF2 + 2H2O = O2 +2Xe +4HF
XeF4 + 2H2O = O2 +Xe +4HF
XeF6 + H2O = XeoF4 + 2 HF
XeOF4 + H2O = XeO2F2 + 2HF
XeO2F2 + H2O = XeO3 + 2HF
Р-ции присоединения:
XeF2 + 2SbF5 = Xe[SbF6]2 XeF6 + CsF = Cs[XeF7]
Р-ции диспропорционирования:
3XeF4 =(H2o)= 2XeF6 + Xe 3XeF6 =(t)= XeF2 + 2XeF8 (полный гидролиз)
Получающийся при полном гидролизе XeF6 кристаллический XeO3 чрезвычайно легко и мощно взрывается.
Получение ксенатов:
XeO3 + KOH = KHXeO4
XeO3 + 3Ba(OH)2 = Ba3XeO6 + 3H2O
Перксенаты:
2KHXeO4 + 2KOH = K4XeO6 + Xe +O2 + 2H2O
Общая характеристика и химические свойства меди, серебра, золота.
Природные источники и получение:
Медные соединения преимущественно представлены сульфидами : Cu2S-халькозин, CuFeS2-халькопирит,так же представляет интерес для переработки Cu2(OH)2CO3-малахит.
2Cu2S + 3O2= 2Cu2O + 2SO2 2Cu2O + Cu2S= 6Cu + SO2
Серебро также встречается в виде сульфидов,например, Ag2S-аргентит.Ag выделяют из неочищенных Cu,Pb и других металлов,в рудах которых содержится его примеси.
Золото в основном представлено в природе в самородном виде.Кроме механического способа отделения золота от песка, основанного на большой разности плотности этого металла и SiO2, Au получают амальгамированием или цианидным способом(метод П.Р.Багратиона):
4Au + 8KCN + O2 + 2H2O = 4K[Au(CN)2] + 4KOH
2K[Au(CN)2] + Zn = K2[Zn(CN)4] +2Au
Химические свойства:
В атомах элементов Сu, Ag, Au происходит «провал» s-электрона, приводящий к полному заполнению электронами d-орбиталей. Благодаря наличию одного s-электрона во внешнем слое для этих элементов характерна степень окисления +1.Кроме того возможны ст.ок. +2 +3 для меди,+2 для серебра, +3 +5 для золота.Эти металлы обладают наивысшей тепло- и электропроводностью, ковки и пластичны.Не реагируют с водой и не вытесняют водород из растворов минеральных кислот,т.к. электродные потенциалы этих металлов имеют положительные значения.Пассивны при комнатной температуре, наибольшей активностью отличается медь.
|
|
|
Cu + 4HNO3(конц) = Cu(NO3)2 + 2NO2 +2H2O
3Cu + 8HNO3(разб) =3Cu(NO3)2 + 2NO + 4H2O
Cu + 2H2SO4(конц) = CuSO4 + SO2 + 2H2O
Ag + 2HNO3(конц) =AgNO3 + NO2 + H2O
2Ag + 2H2SO4(конц) =t= Ag2SO4 + SO2 + 2H2O
3Ag + 4HNO3(разб) = 3AgNO3 + NO + 2H2O
Au же нерастворимо в них, лучшим кислотным растворителем для Au является царская водка:
Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
Так же возможно:
2Au + 2HCl + 3Cl2 = 2H[AuCl4]
2Au + 6H2SeO4(конц) = Au2(SeO4)3 + 3H2SeO3 + 3H2O
2Ag(Cu) + H2S(г) = Ag2S(Cu2S) + H2
Соединения:
Черный CuO:
2Cu + O2 =t= 2CuO
2Cu(NO3)2 =t= 2Cuo + 4 NO2 + O2
Cu2(OH)2CO3 =t= 2CuO + CO2 + H2O
Красный Cu2O:
4CuSO4 + 8NaOH + N2H4 = N2 + 2Cu2O + 4Na2SO4 + 6H2O
Оба оксида проявляют основные свойства,у CuO отмечается слабая амфотерность:
CuO + 2NaOH =спл= Na2CuO2 + H2O
Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH
CuO + 4NH3 + H2O = 2[Cu(NH3)4](OH)2
2AgNO3 + 2NaOH = Ag2O + 2NaNO3 + H2O
|
|
|
При обработке озоном образуется черный AgO,сильный окислитель
При приливании растворов щелочей к солям меди +2 осаждается Сu(OH)2- голубой осадок:
Сu(OH)2 + 2NaOH = Na2Cu2O + 2H2O
Cu(OH)2 =t= CuO + H2O
Au(OH)3 – золотисто-желтый:
AuCl3 + 3KOH = Au(OH)3 + 3KCl
Au(OH)3 =50-100С= AuO(OH) + H2O
2AuO(OH) =150C= Au2O3 + H2O
Au(OH)3 + KOH = K[Au(OH)4]
Au(OH)3 + 4HCl = H[AuCl4] + 3H2O
Au2O3 =>150C= Au + Au2O + O2
Cu + CuCl2 + 2HCl = 2H[CuCl2]
CuCl + NaCl(изб) = Na[CuCl2]
CuCl2 + 2NH3(изб) = [Cu(NH3)2]Cl
2CuSO4 + KI = 2K2SO4 + 2CuI +I2
CuSO4 + 4KCN(изб) =K2[Cu(CN)4] + K2SO4
2CuSO4 + 4KCN = 2CuCN + 2K2SO4 + (CN)2
Соли меди +2 сильно гидролизованы
2CuSO4 + 2K2CO3 + H2O = Cu2(OH)2CO3 + 2K2SO4 + CO2
Соли серебра +1 практически не гидролизованы,растворимые соли серебра единичны.
AgF-AgCl-AgBr-AgI растворимость уменьшается
AgCl + NaCl(изб) = Na[AgCl2]
AgCl + 2NH3(изб) = [Ag(NH3)2]Cl
AgBr + 2NH3(изб) = [Ag(NH3)2]Br
AgI уже не растворяется в водном растворе аммиака
AgГ + 2Na2S2O3(изб) = Na3[Ag(S2O3)2] + NaГ
2AgF2 =t=2AgF + 2
4AgF2 + 2H2O = 4AgF +4 HF + O2
H[AuCl4] – золотохлористоводородная к-та
2H[AuCl4] + 3SnCl2 = 3SnCl4 +2Au+2HCl
2Au + 5KrF2=HF(ж)=2AuF5 + 5Kr
2Au + 5KrF2 + 2KF = HF(ж)= 2K[AuF6] + 5 Kr
Общая характеристика и химические свойства элементов подгруппы цинка.
Соли цинка, кадмия и ртути, их гидролиз. Амидные соединения ртути. Соединeния Hg22+: получение и свойства.
Общая характеристика подгруппы цинка, их химические свойства (Zn,Cd,Hg).
В соединениях в основном проявляют степень окисления +2,электроны характеризуются d10-конфигурацией. Исключение проявляют производные иона Hg22+, который формально проявляет степень окисления +1. Для комплексных соединений более характерно КЧ4, однако для кадмия характерно образование соединений с КЧ6. Для ртути характерно образование связей Hg-Hg, образование связей с другими металлами (Hg6[Rh(PM3)3]4, [Os3(CO)11Hg]3).
|
|
|
Получение: Цинк добывают из сульфидных руд:
2ZnS + 3O2 = 2ZnO + 3SO2
2ZnO + C = 2Zn + CO2
Кадмий получают из побочных продуктов переработки цинковых, свинцово-цинковых и медно-цинковых руд. Эти продукты (содержащие 0,2-7% Кадмия) обрабатывают разбавленной серной кислотой, которая растворяет оксиды Кадмия и цинка. Из раствора осаждают Кадмий цинковой пылью; губчатый остаток (смесь Кадмия и цинка) растворяют в разбавленной серной кислоте и выделяют Кадмий электролизом этого раствора. Электролитический Кадмий переплавляют под слоем едкого натра и отливают в палочки; чистота металла - не менее 99,98%.
Ртуть добывают относительно прямым способом:
HgS + O2 = Hg + SO2.
Химические свойства: Цинк и кадмий довольно похожи, а ртуть несколько отличается. Цинк и кадмий при нагревании взаимодействуют с кислородом, серой, фосфором и галогенами; ртуть не взаимодействует с фосфором. Ни один из металлов не реагирует с водородом, углеродом и азотом.
|
|
|
Сплавы ртути с другими металлами – амальгамы, являются мягкими восстановителями:
2NaHg + 2H2O = 2Hg + 2NaOH + H2
Цинк – более сильный восстановитель, чем кадмий:
Zn 0 + Cd2+ = Zn2+ + Cd0
С разбавленными кислотами:
Zn + H2SO4(разб) = ZnSO4 + H2
С кислотами-окислителями:
Zn + 4HNO3(конц,гор)=Zn(NO3)2 + 2NO2+2H2O
4Zn + 10HNO3(разб,гор)=4Zn(NO3)2 + N2O + 5H2O
Ртуть не взаимодействует с разбавленными кислотами, но с концентрированными:
Hg+4HNO3(конц)=Hg(NO3)2 +2NO2 + 2H2O
Hg+2H2SO4(конц,гор)=HgSO4 + SO2 + 2 H2O
Разбавленная азотная образует динитрат ртути:
6Hg+8HNO3 = 3Hg2(NO3)2 + 2NO + 4H2O
Цинк – единственный представитель группы, который растворяется в водн. р-рах щелочей с образованием комплексов:
Zn+2OH- + 2H2O = [Zn(OH)4]2- + H2
Zn + 4NH3*H2O=[Zn(NH3)4](OH)2 + 2H2O + H2.
Соли цинка, кадмия и ртути, их гидролиз
Сульфиды цинка, кадмия и ртути малорастворимы. Сфалерит ZnS – главный источник цинка. Легко растворяется в кислотах с выделением сероводорода
ZnS + 2H3O+ = Zn2+ + H2S + 2H2O
Сульфид кадмия более устойчив, выпадает в осадок даже в кислой среде, устойчив к действию растворов щелочей и большинства кислот. Сульфид кадмия получают:
CdSO4 + BaS = CdS + BaSO4 (камподон – смесь сульфата бария и сульфида кадмия)
Сульфид ртути подвергается действию только концетрированных HBr и HCl или царской водки или царской водки:
3HgS + 8HNO3 + 6 HCl = 3HgCl2 + 3H2SO4 + 8NO + 4H2O
Галогениды – известны все галогениды элементов этой подгруппы, а так же 4 галогенида диртути.
2HgCl2+[SnCl3]- + Cl- = Hg2Cl2 + [SnCl6]2-
Для цинка и кадмия наиболее характерны тетраэдрические комплексы.
Zn(OH)2 + 4NH3*H2O = [Zn(NH3)4](OH)2 + 4H2O, для кадмия и октаэдрические:
Cd(OH)2+6NH3*H2O = [Cd(NH3)6](OH)2 + 6H2O.
Соли ртути в водной среде осаждаются в виде основных солей:
Hg(NO3) + H2O = Hg(OH)(NO3) + HNO3
При поджигании Hg(SCN)2 –«фараоновы змеи»
2Hg(SCN)2 = 2Hgs + C3N2 + CS2+N2
Реактив Несслера – крайне чувствительный реагент на аммиак:
2K2[HgI4] + 3KOH + NH3 = Hg2NI*H2O + 7KI + 2H2O – иодидная соль основания Миллона ([Hg2N(OH)*(H2O)2).
Ртуть образовывает прямые связи с азотом:
HgCl2 + 2NH3 =(HgNH2)Cl + NH4Cl
При избытке NH4+:
HgCl2 + 2NH3 =[Hg(NH3)2)Cl 2].
Соединения Hg22+:
Получение: взаимодействием хлорида ртути(II) и металлической ртути при высокой температуре
HgCl2 + Hg = Hg2Cl2
взаимодействием хлорида ртути(II) с цианидом ртути(II):
HgCl2+Hg(CN)2 = Hg2Cl2 + C2N2
Свойства: катион диртути в водном растворе диспропорционирует
Hg22+ = Hg + Hg2+
Hg22++2OH- = HgO + Hg + H2O
Hg22+ + S2- = HgS + Hg
Большинство солей нерастворимы. ОВР с сильными окислителями и восстановителями
Hg2(NO3)2 + 4 HNO3 = 2Hg(NO3)2 + 2NO + 2H2O
Hg2Cl2 + [SnCl3]- + Cl- = 2Hg + [SnCl6]2-
Гидролиз солей:
ZnSO4 + 2H2O = Zn(OH)2 + H2SO4
Cd(CN)2 + 2H2O = Cd(OH)2 + HCN
От солей цинка к солям ртути гидролиз ослабевает, соли ртути очень слабо диссоциированы.
Т.к. Hg(OH)2 не существует, то при гидролизе:
2Hg(NO3)2 + H2O = Hg2O(NO3)2 + 2HNO3
Аммонийные соединения ртути Только для ртути известны амидные соединения, содержащие связь Hg—N устойчивые в водной среде (другие металлы образуют подобные соединения лишь в неводных растворах).
Для Hg (II):
HgCl2 + 2NH4OH→[HgNH2]Cl2↓ + NH4Cl + 2H2
Для Hg (I)
Hg 2Cl2 + 2NH3→[HgNH2]Cl↓ + NH4Cl + Hg↓
Дата добавления: 2018-08-06; просмотров: 967; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
