Тема 3. Хімічна кінетика та хімічна рівновага
Хімічна кінетика – це наука, що вивчає швидкість хімічних реакцій та механізм їх протікання.
Швидкість хімічної реакції - це зміна кількості речовини, що утворюється або витрачається в ході реакції в одиницю часу в одиниці простору системи.
Для реакції в гетерогенній системі за одиницю простору беруть площу зіткнення реагуючих речовин, а в гомогенній системі – об’єм:
в гетерогенній системі -  , моль/(с·м2),
, моль/(с·м2),
а в гомогенній системі –  , моль/(c·дм3)
, моль/(c·дм3)
Приклади гетерогенної та гомогенної реакцій:
Zn(тв.) +2HCl(р) = ZnCl2(р) + H2↑
SnCl2(вод) + FeCl3 (вод) = SnCl4 (вод) + FeCl2(вод).
Розглянемо, що таке  .
.  .
.
Тобто, це відношення є зміна концентрації якоїсь речовини.
Тоді для гомогенної реакції формулу можна переписати як:
 .
.
Це середня швидкість реакції на відрізку часу  τ.
τ.
Середня швидкість реакції - це зміна концентрації одного з продуктів реакції (або однієї з вихідних речовин) за певний інтервал часу.
Знак “-“ або “+” ставиться в залежності від того, зміна концентрації якого з реагентів використовується у вираженні для швидкості реакції. Так, вихідні речовини витрачаються, і для них DC<0, а продукти реакції – накопичуються, їх концентрація зростає DC>0. Швидкість не може бути негативною величиною і тому у формулі стоїть знак “мінус”, якщо вимірювання ведеться за початковими речовинами, які витрачаються в ході реакції.
|
|
|
Чим менше інтервал часу Δτ і зміна концентрації ∆C, тим ближче середня швидкість до істинної. Коли Δτ наближається до нуля, то попередня формула має вигляд похідної dC за dt, тому що

 .
.
Істинна швидкість реакції – це перша похідна від концентрації за часом:
 .
.
Наприклад, для реакції 2 NO (г) + O2 (г) ® 2 NO2 (г) співвідношення між швидкостями, що виражаються через концентрації реагентів, має вигляд:

Фактори, що впливають на швидкість реакції
Швидкість реакції залежить від природи реагуючих речовин, концентрації реагентів, температури, присутності каталізаторів, а для газів - і від тиску, який пов'язаний з молярною концентрацією рівнянням Клапейрона-Менделєєва:
p=CRT.
Залежність швидкості реакції від молярної концентрації виражається законом діючих мас(або основним законом кінетики): швидкість хімічної реакції пропорційна добутку константи швидкості та концентрацій реагуючих речовин у деяких ступенях

Так, для реакції А+В = Р швидкість дорівнює υ = k∙СA∙СB, а для реакції 2А + В = Р υ = k∙С2A∙СB, бо цю реакцію можна представити як А+А+В = Р
|
|
|
і швидкість пропорційна концентрації усіх компонентів:
υ = k∙СA∙СA∙СB= k∙СA2∙ СB .
Тоді швидкість взаємодії нітрогена(II) оксиду з киснем має вираз:
 ,
,
або запис може бути таким, де концентрацію речовин позначають квадратними дужками:

де n, m – порядок реакції за відповідним компонентом (2-ий порядок за NO)
(n+m) – сумарний порядок реакції
k - константа швидкості хімічної реакції.
Рівняння, що пов’язує швидкість хімічної реакції з концентрацією реагуючих речовин, називають кінетичним рівнянням реакції.
Основний закон хімічної кінетики не враховує реагуючі речовини, що знаходяться в твердому стані. Для гетерогенних реакцій взаємодія відбувається тільки на поверхні твердих речовин, що залишається незмінною, і концентрація твердих речовин вважається сталою величиною.
Наприклад, для горіння вугілля: С+О2 → СО2 реакція відбувається між молекулами кисню і твердою речовиною тільки на поверхні поділу фаз (твердої і газоподібної). Це означає, що концентрація твердої фази не впливає на швидкість реакції. В даному випадку швидкість реакції пропорційна тільки концентрації кисню.
|
|
|

Константа швидкості хімічної реакції - швидкістьреакції при концентраціях речовин, що дорівнюють 1 моль/дм3.
Константа k залежить від температури, від природи реагуючих речовин, але не залежить від їх концентрації. Загальний порядок наведеної реакції 2 NO (г) + O2 (г) ® 2 NO2 (г) дорівнює трьом (1+2=3). Значення n, m можна визначити тільки експериментально, іноді вони співпадають з коефіцієнтами в рівнянні реакції. Далі кінетичні рівняння не мають сенсу, бо дуже мала ймовірність того, що зіткнуться разом 4 або 5 молекул. У більшості випадків порядок реакції не дорівнює сумі стехіометричних коефіцієнтів у рівнянні реакції, а визначається її механізмом, тобто елементарними проміжними стадіями і їхньою послідовністю. Наприклад, реакція, що розглянута вище, протікає через дві елементарні стадії:
 NO+O2 NO3 і NO3+ NO ® 2NO2
NO+O2 NO3 і NO3+ NO ® 2NO2
У той час як порядок характеризує реакцію в цілому, поняття молекулярність реакції відноситься до її окремих стадій. Вона дорівнює числу молекул, що беруть участь в елементарному акті хімічного перетворення. У більшості реакцій молекулярність дорівнює двом, тому що ймовірність одночасного зіткнення трьох, а тим більше чотирьох молекул дуже мала.
|
|
|
При цьому рівняння показують залежності швидкості: пряму- від концентрації або тиску й опосередковану через константу швидкості - від природи реагуючих речовин, температури і каталізатора (якщо він є), відповідно до рівняння Арреніуса:
 ,
,
де k - константа швидкості; А - передекспоненціальний множник; Еа - енергія активації.
Енергія активації– це та мінімальна енергія, яку потрібно додатково надати реагентам, щоб відбулася реакція.
Для того, щоб відбувалася взаємодія між молекулами, вони повинні зіткнутися. В результаті зіткнення утворюється активований перехідний комплекс з максимальною потенційною енергією.
Наприклад:
А-В + С = [А··· В ··· С] = А + В-С
активований
комплекс
Але не всі зіткнення є ефективними, що призводять до утворення продуктів. Ефективними будуть тільки ті зіткнення, при яких молекули мають достатню енергію для подолання енергетичного бар’єру. Частотний фактор А в рівнянні Арреніуса – кількість зіткнень молекул, якраз і показує ймовірність (частоту) того, що система з енергією активації Еа перетвориться на продукти, а не повернеться в вихідний стан.
Більш проста залежність швидкості реакції від температури випливає з емпіричного правила Вант-Гоффа:
при підвищенні температури на кожні 10°С швидкість більшості реакцій збільшується в 2-4 рази:

де g - температурний коефіцієнт швидкості, що має значення від 2 до 4.
Наявність у рівнянні Арреніуса енергії активації дозволяє регулювати швидкість реакції за допомогою каталізаторів. На діаграмі ендотермічної реакції видно, що енергія активації може зменшитися при наявності в системі каталізатора.
Каталізатори - це речовини, що змінюють швидкість реакції в результаті участі в проміжній хімічній взаємодії з компонентами реакції, але, що відновлюють після кожного циклу проміжної взаємодії свій хімічний склад. При гомогенному каталізі взаємодіючі речовини і каталізатор складають однофазну систему, а при гетерогенному - двофазну, причому проміжна сполука утворюється на поверхні поділу фаз. Наприклад:
NO+NO2
 2SO2+O2 ® 2SO3 - гомогенний каталіз
2SO2+O2 ® 2SO3 - гомогенний каталіз
Pt або V2O5
2SO2+O2 ® 2SO3 - гетерогенний каталіз.
Питання хімічної рівноваги варто розглядати виходячи з того, що всі хімічні реакції поділяються на оборотні і практично необоротні. Більшість хімічних реакцій оборотні, тобто вони протікають одночасно в двох протилежних напрямках і характеризуються швидкостями як прямої, так і зворотної реакцій. Коли швидкості цих реакцій стають рівними, настає стан хімічної рівноваги, при якому концентрації речовин залишаються незмінними і називаються рівноважними.
У момент настання рівноваги пряма і зворотна реакції не припиняються, а продовжують протікати з рівними швидкостями, тобто рівновага є динамічною. Для реакції, що описується в загальному виді рівнянням:
 аА+bВ cС+dD ;
аА+bВ cС+dD ;
 ; - швидкість прямої реакції
; - швидкість прямої реакції
 - швидкість зворотної реакції
- швидкість зворотної реакції
у стані рівноваги виконується співвідношення:  тобто
тобто

 або
або

(якщо А, B, C, D газоподібні речовини),
де k+ і k-- константи швидкості прямої та зворотної реакцій;
Kр - константа рівноваги, С- молярні концентрації речовин,
[А], [В], [С], [D] – рівноважні молярні концентрації речовин.
Наприклад, при 3500С для оборотної реакції:
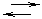 H2 + I2 2HI
H2 + I2 2HI
настає стан хімічної рівноваги і швидкості прямої та зворотної реакцій стають рівними.
υ1 = k1[H2] [I2]; υ2 = k2[HI]2.
Тоді вираз константи рівноваги при постійній температурі буде мати вигляд:

Константа рівновагипоказує, у скільки разів константа швидкості прямої реакції більше швидкості зворотної реакції і є мірою протікання процесу. Математичне вираження константи рівноваги являє собою інше формулювання закону дії мас.
Якщо К>>1, константа швидкості прямої реакції набагато більше ніж зворотної і в системі більше знаходиться продуктів реакції, ніж реагентів;
а при К<<1 – в системі більше знаходиться вихідних речовин, ніж продуктів реакції.
Константа рівноваги не залежить від концентрації, парціальних тисків для реакцій у газовій фазі і каталізатора, але залежить від природи реагуючих речовин і температури. Використання каталізаторів не змінює константу рівноваги, а лише скорочує час, необхідний для досягнення стану рівноваги.
При зміні зовнішніх умов (концентрація, тиск, температура) система виходить зі стану рівноваги в тому випадку, якщо швидкості прямої і зворотної реакцій під зовнішнім впливом змінюються в неоднаковому ступені. Рівновага зміщується в бік тієї реакції, швидкість якої в нерівноважних умовах буде більше.
Вплив зовнішніх факторів на рівноважну систему можна передбачити, користуючись принципом Ле-Шательє: якщо на систему, що знаходиться в рівновазі, діють зовнішні фактори, то рівновага зміститься в такому напрямку, де дія цих факторів буде послаблена.
Дійсно, при введенні в систему одного з реагентів, рівновага зміщується в бік його витрати, тобто в прямому напрямку. При підвищенні тиску – в бік меншого числа моль газів (тобто, де в системі менший тиск), при підвищенні температури – в бік ендотермічної реакції, де температура в системі падає.
У випадку гетерогенних систем у вираз для швидкості і константи рівноваги входять параметри газів і речовин у розчинах і не входять параметри твердих речовин.
Наприклад, для реакції утворення амоніаку:
N2 +3H2 = 2NH3; ∆H = - 46 кДж/моль.
Збільшення концентрації азоту та водню зміщує равновагу праворуч. Збільшення концентрації амоніаку ліворуч. Оскільки реакція екзотермічна, йде з підвищенням температури в системі, то зовнішнє підвищення температури змістить рівновагу ліворуч, у бік ендотермічної реакції.
Зміна тиску.
З рівняння видно, що з 4 молей газів (1моль N2 і 3 моль H2) утворюється 2 моль газу, тобто тиск у системі буде падати. Підвищення зовнішнього тиску спричиняє зміщення рівноваги праворуч, де кількість молей газів менша, а зниження зовнішнього тиску веде до зміщення рівноваги убік зворотної реакції.
Дата добавления: 2018-08-06; просмотров: 107; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
