Закон сохранения массы веществ.
Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции.
Этот закон является одним из основных стехиометрических законов химии, все расчеты по химическим реакциям производятся на его основе. Именно с открытием этого закона связывают возникновение современной химии как точной науки.
Этот закон объясняется тем, что при химических реакциях общее количество атомов не изменяется, а происходит лишь их перегруппировка.
Закон сохранения массы веществ применяется при составлении уравнений химических реакций.
Химическое уравнение– это условная запись химической реакции посредством химических формул и коэффициентов.
Исходные вещества, принимающие участие в химических реакциях называются реагентами.
Новые вещества, образующиеся в результате химической реакции называются продуктами.
| продукт |
| реагенты |
Алгоритм составления уравнения химической реакции.
1) Запишите схему реакции, т.е. формулы реагирующих и образующихся веществ:
Ba(OH)2 + H3PO4 → Ba3(PO4)2 + H2O
2) Начинайте уравнивать схему реакции с формулы соли (если она имеется). При этом помните, что несколько сложных ионов в составе основания или соли обозначаются скобками, а их число - индексами за скобками:
3Ba(OH)2 + 2H3PO4 → Ba3(PO4)2 + H2O
3) Водород уравняйте в предпоследнюю очередь:
3Ba(OH)2 + 2H3PO4 → Ba3(PO4)2 + 6H2O
|
|
|
4) Кислород уравняйте последним - это индикатор верной расстановки коэффициентов.
3Ba(OH)2 + 2H3PO4 = Ba3(PO4)2 + 6H2O
Типы химических реакций.
Химические реакцииилихимические явления – это процессы, в результате которых из одних веществ образуются другие.
Условия химических реакций:
• Выделение газа;
• Образование осадка;
• Выделение (поглощение) тепла и света;
• Появление или изменение запаха;
• Изменение цвета.
Типы химических реакций:
Реакции соединения.

2Аl+ 3I2 = 2 All3 NH3 + HCl = NH4Cl
Реакции, в которых из нескольких простых или сложных веществ образуется одно более сложное вещество, наз.реакциями соединения.
Реакции разложения.
| t |
| Эл.ток |

2Н2О → 2Н2 + О2 (NH4)2Cr2O7 → Cr2O3 + N2 + 4H2O
Реакции, в которых из одного сложного вещества получается два или несколько простых или сложных веществ, наз.реакциями разложения.
Реакции замещения.
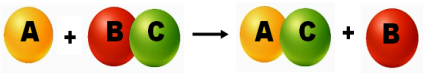
SnCl2 + Zn = ZnCl2 + Sn H2SO4 + Zn = ZnSO4 + H2↑
Реакции, протекающие между простыми и сложными веществами, при которых атомы простого вещества замещают атомы одного из элементов в сложном веществе, наз.реакциями замещения.
|
|
|
Реакции обмена.

Pb(NO3)2 +2KI = PbI2↓+2KNO3 2 NaOH + H2SO4 = Na2SO4 + 2H2O
Реакции, происходящие между сложными веществами, в результате которых они меняются своими составными частями, наз. реакциями обмена.
Дата добавления: 2018-06-01; просмотров: 305; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
