Опыт 2. Получение малорастворимых сульфидов
В первую пробирку внести 2 - 3 капли раствора сульфата марганца(II), во вторую пробирку - 2 - 3 капли раствора нитрата свинца(II). В каждый раствор добавить, по 2 - 3 капли сульфида аммония. Наблюдать выпадение осадков сульфида марганца(II) и сульфида свинца(II). К полученным осадкам прибавить по 2 - 3 капли 2н. раствора азотной кислоты.
- отметить, какие изменения происходят в пробирках. Указать цвет осадков
- Составить уравнения реакций получения сульфидов марганца(II) и свинца(II) в молекулярном и ионном виде.
MnSO4 + (NH4)2S →
Pb(NO3)2 + (NH4)2S →
- Указать, какой сульфид растворился……………
- Ответить, возможно, ли его образование в кислой среде…………..
- Составить уравнение реакции растворения MnS в кислоте в молекулярной и ионной форме
MnS + HNO3 →
- Пользуясь значениями (ПРMnS = 1,1 10-13) и констант диссоциации сероводородной кислоты рассчитать константу равновесия для процесса растворения и сульфида марганца(II) в кислоте
K = ПРMnS/ (K1H2S K2H2S) =
- Пользуясь значениями (ПРPbS, = 8,7 10-29) и констант диссоциации сероводородной кислоты рассчитать константу равновесия для процесса растворения и сульфида свинца(II) в кислоте
K = ПРPbS/ (K1H2S K2H2S) =
- Сделать вывод о направлении протекания указанных реакций.
В две другие пробирки с растворами солей марганца(II) и свинца(II) добавить по 3 - 4 капли сероводородной воды.
- отметить, какие изменения происходят в пробирках.
|
|
|
- Указать, какой сульфид образовался……………
- Составить уравнения реакций получения сульфида свинца(II) в молекулярном и ионном виде.
Pb(NO3)2 + H2S →
- Объяснить различные результаты действия H2S и (NН4)2S на соль марганца(II) и образование осадка PbS в обоих случаях.
Образование черного осадка PbS может служить реакцией обнаружения иона Pb2+ или сероводорода.
Опыт 3. Получение диоксида серы и его растворение в воде
В колбу поместить кристаллический сульфит натрия (Na2SO3), добавить 6-8 капель 4 н. раствора серной кислоты и быстро закрыть пробкой с отводной трубкой. Выделяющийся газ пропустить в пробирку с дистиллированной водой в течение 2-3 мин. Если выделение газа идет недостаточно энергично, пробирку осторожно подогреть. Проверить универсальным лакмусом рН раствора.
- отметить, какие изменения происходят в пробирках.
- выделяется газ…………….
- Окраска индикатора …………………, рН = ………..
- окраска индикатора указывает на………………… свойства водного раствора SO2
- Составить уравнение реакции получения оксида серы в молекулярном и ионном виде:
Na2SO3 + H2SO4 ®
- Составить уравнение реакции растворения оксида серы в воде в молекулярном и ионном виде:
|
|
|
SO2 + H2O ®
- Написать уравнения диссоциации сернистой кислоты по 1-ой и по 2-ой ступени
1 ст. H2SO3 → …..…… + ……
2 ст. HSO3- → …..…… + ……
- Составьте выражения для констант диссоциации по 1-ой и по 2-ой ступени.
K1 = K2 =
- Выписать значения констант диссоциации из таблицы.
K1 = 1,6 10-2 K2 = 6,31 10-8
- Сделать вывод о свойствах сернистой кислоты.
Сохранить раствор SO2 для следующего опыта.
Опыт 4. Окислительные и восстановительные свойства соединений серы (IV)
а) Окислительные и восстановительные свойства SO2.
В две пробирки, одна из которых с сероводородной (а), другая с йодной водой (б) (по 3-5 капель), добавить по несколько капель водного раствора SO2.
- Отметить происходящие изменения в растворах.
- Составить уравнение реакции диоксида серы с сероводородной водой
H2S + SO2 ®
- Указать окислитель………………….., восстановитель ………………….
- Составить уравнение реакции диоксида серы с йодной водой
I2 + SO2 + H2O ®
- Указать окислитель………………….., восстановитель ………………….
|
|
|
- указать, какие свойства проявляет диоксид серы.
Опыт 5. Дегидратирующие свойства серной кислоты
а) «Черная колонна» (демонстрационный).
В стаканчик объемом 100 мл поместить 10-15 гр сахарозы (С12Н22О11) или глюкозы (С6Н12О6), поместить стеклянную палочку длиной приблизительно 30 см. Прилить по палочке 10 мл 4н.серной кислоты, энергично перемешать палочкой, оставить палочку в стакане вертикально.
- Отметить происходящие изменения
- Составить уравнение реакции обугливания
С12Н22О11 + Н2SО4(конц) ® 12C + Н2SО4 11H2O
- Объяснить образование газа с резким запахом.
- Составить уравнение реакции.
С + H2SO4(конц) ®
- Вывод
Опыт 6. Взаимодействие серной кислоты с металлами
(см. лабораторные работы №5 – 10)
Опыт 7. Различная растворимость сульфита и сульфата бария в кислоте
В двух пробирках получить обменной реакцией сульфит и сульфат бария, для чего взять по 3-4 капли растворов соответствующих солей Na2SO3 или Na2SO4 и BaCl2. Наблюдать образование осадков в обеих пробирках. Сравнить растворимость сульфита и сульфата бария в кислоте, добавив в обе пробирки по 1-2 капли 2 н. соляной кислоты.
- Отметить происходящие изменения в пробирках
|
|
|
- Составить уравнение реакции получения сульфата бария в молекулярной и ионной форме
BaCl2 + Na2SO4 →
- Составить уравнение реакции получения сульфита бария в молекулярной и ионной форме
BaCl2 + Na2SO3 →
- Составить уравнение реакции растворения сульфита бария в кислоте в молекулярной и ионной форме
BaSO3 + HCl →
-Ответить, можно ли этой реакцией различить ионы SO 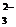 и SO
и SO 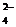 .
.
Дата добавления: 2018-05-31; просмотров: 693; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
