Основные понятия термодинамики: система, фаза, виды систем (открытые, закрытые, изолированные системы), параметры состояния систем, виды процессов.
ХИМИЯ 2 КУРС
Дайте понятие предмета, задач аналитической химии, ее назначение в подготовке технологов общественного питания.

Растворы электролитов. Степень диссоциации. Константа диссоциации. Независимость этой величины от концентрации. Сильные и слабые электролиты.


Диссоциация воды. Ионное произведение воды. Понятие рН. Определение среды растворов.

Обратимые реакции. Хим. Равновесие. Константа равновесия. Смещение хим равновесия. Принцип Ле-Шателье




Эмульсия, способы получения, значение. Эмульгаторы.

Пены: понятие, строение и устойчивость. Роль пенообразователей. Получение и разрушение пен.

Методы количественного анализа. Гравиметрический метод анализа.
Методы количественного анализа – химический (калориметрический, гравиметрический, титриметрический), физико-химический (спектральный), физический (нефелометрический).
Гравиметрический метод анализа – это совокупность методов количественного анализа на выделения и определения вещества. Методы:
1. Отгонка вещества в виде летучего соединения (Например: определение влаги хлебобулочных изделий)
2.Осаждение в виде мало растворимого соединения (Например: определение железа в воде)
Методы количественного анализа. Титриметрический анализ.
Методы количественного анализа – химический (калориметрический, гравиметрический, титриметрический), физико-химический (спектральный), физический (нефелометрический).
|
|
|
Титриметрический анализ- это определение количественного содержания компонентов в исследуемом веществе основанном на точном измерении объемом реагирующих веществ.
Сухой метод – растирание, исследуемое вещество помещается в ступку и растирают с твердым реагентом, смотрят на изменение окраски.
Пирохимические методы: окрашенные перлы – растворение в расплаве некоторых металлов с образованием цветного стекла. Окрашенное пламя – горение пламени некоторых солей, некоторых металлов, восстанавливаются в атомах металлов, пары которых окрашивают пламя в разные цвета.
Мокрый способ – химические реакции в растворах электролитов.
Качественный анализ. Методы качественного анализа. Требования к аналитической химии.

Общая характеристика растворов. Способы выражения концентрации растворов. Сущность процесса растворения.
Раствором называют гомогеннее системы состоящие из 2-х или более компонентов.
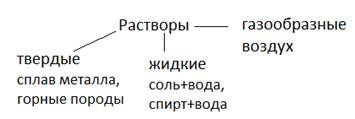
Жидкие р-ры – состоят из растворителя и растворенного вещества, то вещество которое в растворе находится в том же агрегатном состоянии что и было до растворения.

Концентрация раствора – называется количество растворенного вещества содержащиеся в определенном количестве раствора.
|
|
|
Процесс растворения – это физико-химический процесс.
1. Разрушение структуры растворяемого вещества распределение его частиц между молекулами растворителя – это физический процесс.
2. Взаимодействие частиц растворенного вещества с молекулами растворителя – это химический процесс.
Основные понятия термодинамики: система, фаза, виды систем (открытые, закрытые, изолированные системы), параметры состояния систем, виды процессов.
Термодинамическая система – тело или группа тел, находящихся во взаимодействии, мысленно или реально обособленные от окружающей среды.
Гомогенная система – система, внутри которой нет поверхностей, разделяющих отличающиеся по свойствам части системы (фазы).
Гетерогенная система – система, внутри которой присутствуют поверхности, разделяющие отличающиеся по свойствам части системы.
Фаза - совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделённая от других частей системы видимыми поверхностями раздела.
Изолированная система - система, которая не обменивается с окружающей средой ни веществом, ни энергией.
Закрытая система – система, которая обменивается с окружающей средой энергией, но не обменивается веществом.
Открытая система – система, которая обменивается с окружающей средой и веществом, и энергией.
|
|
|



Дата добавления: 2018-06-27; просмотров: 545; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
