Сорбция ионов меди (II) на ионообменной смоле
Выполнение опыта
Сорбция ионов меди (II) на катионите
В стакан №1 налейте 40 мл раствора сульфата меди (II) с концентрацией 0,05 М. Объем раствора отмерьте мерным цилиндром или воспользуйтесь специальной меткой на стакане, которая соответствует объему в 40 мл. Отмерьте мерной ложечкой катионит КУ-2 ( 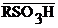 – сульфокислота) и перенесите его в стакан с 40 мл раствора СuSO4.Включите секундомер как только смола будет перенесена в стакан с раствором СuSO4 и непрерывно перемешивайте раствор стеклянной палочкой в течение заданного преподавателем времени. Перемешивание обеспечивает равномерную сорбцию катионитом ионов меди (II) из раствора.
– сульфокислота) и перенесите его в стакан с 40 мл раствора СuSO4.Включите секундомер как только смола будет перенесена в стакан с раствором СuSO4 и непрерывно перемешивайте раствор стеклянной палочкой в течение заданного преподавателем времени. Перемешивание обеспечивает равномерную сорбцию катионитом ионов меди (II) из раствора.
СuSO4 + 2 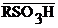 ® H2SO4 + ® H2SO4 + 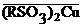
|
Далее аккуратно слейте с катионита раствор в стакан № 2.
В полученном растворе определите концентрацию ионов меди (II)комплексонометрическим титрованием с мурексидом.
Определение концентрации ионов меди (II) комплексонометрическим титрованием с мурексидом
Отберите пипеткой 10 мл раствора меди (II) из стакана № 2 и перенесите его в коническую колбу для титрования. В эту же колбу добавьте из бюретки 5 мл ацетатного буферного раствора и 1/2 мерной фарфоровой ложки индикатора – мурексида. Смесь перемешайте и оттитруйте раствором трилона Б концентрацией 0,05 М до изменения окраски из желто-оранжевой в сиренево-малиновую в точке стехиометричности. Измерьте объем израсходованного на титрование раствора трилона Б (Трилон Б – динатриевая соль этилендиаминтетрауксусной кислоты ЭДТА, C10H14O8N2Na2·2H2O, условная формула Na2H2Y). В реакции участвуют ионы – H2Y2-:
|
|
|
Сu2+ + H2Y2- = CuY2- + 2H+
Титрование повторяют до получения не менее двух сходящихся результатов (±0,1 мл).
Оформление опыта
Результаты титрования запишите в таблицу № 2.1
Запишите значения объёмов трилона Б и определите средний результат.
Рассчитайте массу m1 ионов меди (II) до сорбции, используя исходную концентрацию ионов меди (II). Объем исходного раствора сульфата меди, 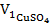 = 40 мл.
= 40 мл.
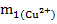 =
= 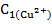 ∙
∙ 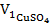 ∙
∙ 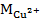 ,г
,г
Рассчитайте концентрацию C2 ионов меди (II) после сорбции, используя закон стехиометрии:
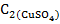 ∙
∙ 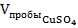 = Стрилон Б ∙Vтрилон Б,
= Стрилон Б ∙Vтрилон Б,
где 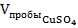 – объем пробы, взятый на титрование, 10 мл;
– объем пробы, взятый на титрование, 10 мл;
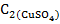 =
=  , моль/л
, моль/л
Рассчитайте массу m2 ионов меди (II) в растворе после сорбции (объем раствора после сорбции практически не меняется, так как используется набухшая ионообменная смола (катионит).
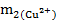 =
=  ∙
∙ 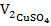 ∙
∙ 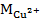 , г,
, г,
где: 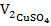 - объем раствора после сорбции равный:
- объем раствора после сорбции равный: 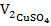 =
= 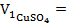 40 мл.
40 мл.
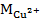 – молярная масса ионов меди.
– молярная масса ионов меди.
Рассчитайте массу сорбированной меди m3
Результаты занесите в таблицу 2.1.
Таблица 2.1
| Результаты титрования: | |
| V1трилона Б = … мл V2трилона Б = … мл Vсртрилона Б= … мл | 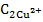 ∙ ∙  = Стрилон Б ∙Vтрилон Б = Стрилон Б ∙Vтрилон Б
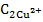 = = 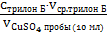
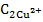 = … моль/л = … моль/л
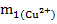 = = 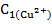 ∙ ∙ 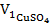 ∙ ∙ 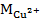 ,г ,г
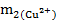 = =  ∙ ∙ 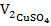 ∙ ∙  г
m3 – масса сорбированных катионов меди(II)
m3 = m1 –m2 г
m3 – масса сорбированных катионов меди(II)
m3 = m1 –m2
|
|
|
|
Рассчитайте коэффициент распределения ионов меди (II)между жидкой (электролит) и твердой (катионит) фазой по формуле:
Dтв/ж = m3/m2
Результаты опыта занесите в таблицу 2.2, используя результаты студентов группы.
Таблица 2.2
| Время контакта мин. | τ1 | τ2 | τ3 | τ4 |
 мл
мл
| 40 | 40 | 40 | 40 |
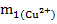 мг
мг
| ||||
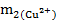 мг
мг
| ||||
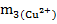 мг
мг
| ||||
| Dтв/ж |
По результатам опыта сделайте вывод о зависимости коэффициента распределения Dтв/ж от времени контакта раствора с катионитом.
Дата добавления: 2018-05-13; просмотров: 578; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
