Вычислить энергию Гиббса реакции при заданной температуре
| № | Уравнение реакции | Т, °С |
| 31. | 2CO (г) + SO2 (г) = S2 (г) + 2CO2 (г) | 850 |
| 32. | 2NaHCO3 (тв.) = Na2CO3 (тв.) + H2O (г) + CO2 (г) | 900 |
| 33. | 2NO2 (г) + О3 (г) = О2 (г) + N2O5 (г) | 800 |
| 34. | 4H2S (г) + 2SO2 (г) = 3S2 (г) + 4H2O (г) | 850 |
| 35. | 4HCl (г) + O2(г) = 2H2O(г) + 2Cl2(г) | 700 |
| 36. | 4СО (г) + 2SO2 (г) = S2 (г) + 4CO2 (г) | 850 |
| 37. | CH4 (г) + 2H2S (г) = CS2 (г) + 4H2 (г) | 850 |
| 38. | CH4 (г) + 2O2 (г) = CO2 (г) + 2H2O (г) | 850 |
| 39. | CH4 (г) + СO2 (г) = 2CO (г) + 2H2 (г) | 850 |
| 40. | CuS (тв) + O2 (г) = Cu (т) + SO2 (г) | 800 |
| 41. | CuSO4 (тв) = CuO (тв) + SO3 (г) | 1000 |
| 42. | СuСО3 (тв) = CuO (тв) + СО2 (г); для CuCO3 (тв): ΔfHo298 = -596 кДж/моль, So298 = 88 Дж/(моль·K), а = 92 Дж/(моль·K), b = 39·10-3 Дж/(моль·K), c’ = -18·105 Дж/(моль·K) | 1000 |
| 43. | Fe2O3 (тв) + 3CO (г) = 2Fe (α) + 3CO2 (г) | 700 |
| 44. | Fe2O3 (тв) + C(графит) = Fe (α) + CO2 (г) | 1500 |
| 45. | MgСO3 (т) = MgO (т) + СO2 (г) | 800 |
| 46. | Na2SO4 (α) + 2C(графит) = Na2S (тв) + 2CO2 (г) | 800 |
| 47. | PbCO3 (тв) + H2S (г) = PbS (тв) + H2O (г) + CO2 (г). | 500 |
| 48. | SiO2(кварц-α) + 4HF(г) = SiF4 (г) + 2H2O (г) | 800 |
| 49. | CaCO3 (кальцит) = CaO (тв) + CO2 (г) | 800 |
| 50. | Al2O3 (корунд) + Na2CO3 (α) = 2NaAlO2 (тв) + CO2 (г) | 450 |
| 51. | TiO2 (рутил) + CCl4 (г) = TiCl4 (г) + CO2 (г) | 700 |
| 52. | 2Fe(OH)3(тв) = Fе2O3(тв) + 3H2O(г); для Fe(OH)3(тв): ΔfHo298=-823 кДж/моль, So298=-105 Дж/(моль·K), a = 85,51 Дж/(моль·K), b = 123,24·10−3 Дж/(моль·K), c’ = −15,12·105 Дж/(моль·K), | 900 |
| 53. | 2PbS (тв) + 3O2 (г) = 2PbO (тв, желтый) + 2SO2 (г) | 500 |
| 54. | Ni(OH)2 (тв) = NiO (тв) + H2O (г); для Ni(OH)2 (тв): ΔfHo298 = -547,1 кДж/моль, So298 = 88 Дж/(моль·K), а = 88 Дж/(моль·K), b = 93·10-3 Дж/(моль·K), с’ = 13·105 Дж/(моль·K) | 1000 |
| 55. | Cu(OH)2 (тв) = CuO (тв) + H2O (г); для Cu(OH)2 (тв): ΔfHo298 = -443,09 кДж/моль, So298 =81 Дж/(моль·K), а = 87 Дж/(моль·K), b = 23,3·10-3 Дж/(моль·K), с’ = -5,4·105 Дж/(моль·K) | 1000 |
| 56. | 4CuS (тв) = 2Cu2S (тв) + S2 (г) | 1200 |
| 57. | Cu2O (тв) + FeS (α) = Cu2S (тв) + FeO (тв) | 1200 |
| 58. | 6FeO (тв) + 4O2 (г) = 2Fe3O4 (тв) | 1400 |
| 59. | 3CaSO4 (тв) + CaS (тв) = 4CaO (тв) + 4SO2 (г) | 1000 |
| 60. | CaSO4 (тв) + 4CO (г) = CaS (тв) + 4CO2 (г) | 1000 |
Расчет константы равновесия при заданной температуре
|
|
|
Краткие теоретические сведения
Химическая термодинамика позволяет определить константу равновесия при какой-либо температуре, если известны константы равновесия при другой температуре и тепловой эффект реакции с применением интегральной формы уравнения изобары химической реакции

Уравнение изобары применимо для узкого температурного интервала и широко применяется для оценки констант гидролиза или диссоциации при нагревании растворов, а также для расчета изменения произведения растворимости в зависимости от температуры раствора.
Для расчета константы равновесия при заданной температуре в достаточно широком температурном интервале применяют метод Темкина-Шварцмана или метод приведенных энергий Гиббса. По методу Темкина-Шварцмана вычисляют энергию Гиббса при заданной температуре по уравнению

В этой формуле М0, М1, М-2 – заранее рассчитанные численные значения, являющиеся частью зависимости теплоемкости от температуры.
|
|
|
После расчета энергии Гиббса вычисляют константу равновесия по формуле
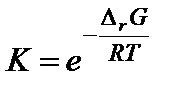 .
.
Поэтому следует обратить внимание на размерность!!! Энергия Гиббса должна быть выражена в Дж/моль!
По методу приведенных энергий Гиббса вычисляют константу равновесия по формуле

Значения  (энтальпии при абсолютном нуле) и
(энтальпии при абсолютном нуле) и  (приведенной энергии Гиббса) приводятся в справочной литературе.
(приведенной энергии Гиббса) приводятся в справочной литературе.
Примеры решения задач
Применение уравнения изобары
Пример 4. Вычислить значение константы гидролиза карбоната натрия по первой ступени при 25 и 90°С.
Решение. 1. Составить ионное уравнение первой ступени гидролиза карбонат-иона

2. Составить таблицу справочных данных, необходимых для расчета:
| Компонент | 
| 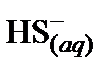
| 
| 
|
 , кДж/моль , кДж/моль
| –230,02 | –17,57 | –285,83 | 32,64 |
 , кДж/моль , кДж/моль
|
3. Вычислить изменение энергии Гиббса реакции гидролиза при 25°С

4. Вычислить значение константы гидролиза карбонат-иона по первой ступени при 25°С

5. Вычислить тепловой эффект реакции гидролиза

6. По уравнению изобары химической реакции вычислить константу гидролиза при 90°С
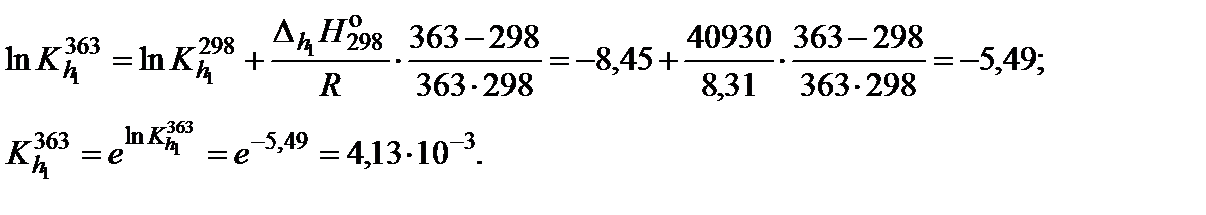
Метод Темкина-Шварцмана
Пример 5. Вычислить энергию Гиббса реакции 4NH3 (г) + 5O2 (г) = 6H2O (г) + 4NO (г) при 850 K.
|
|
|
Решение. 1. Составить таблицу справочных данных, необходимых для расчета:
| Компонент | NH3 (г) | O2 (г) | H2O (г) | NO (г) |
 , кДж/моль , кДж/моль
| −45,94 | 0 | −241,81 | 91,26 |
 , Дж·моль−1·K−1 , Дж·моль−1·K−1
| 192,66 | 205,04 | 188,72 | 210,64 |
| a, Дж·моль−1·K−1 | 29,80 | 31,46 | 30,00 | 29,58 |
| b·103, Дж·моль−1·K−1 | 25,48 | 3,39 | 10,71 | 3,85 |
| c’·10−5, Дж·моль−1·K−1 | −1,67 | −3,77 | 0,33 | −0,59 |
2. Составить уравнение для расчета теплового эффекта реакции при 298 K и произвести необходимые вычисления:

3. Составить уравнение для расчета изменения энтропии реакции в соответствии с законом Гесса и произвести необходимые вычисления:
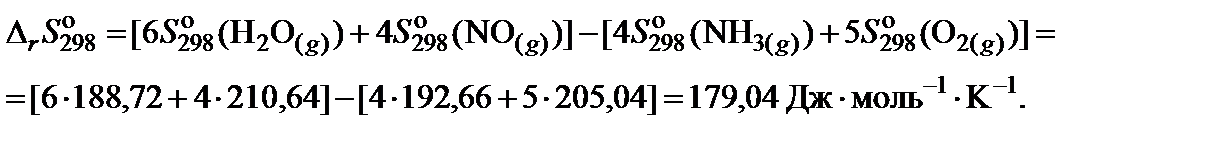
4. Пользуясь законом Гесса, найти изменение коэффициентов теплоемкости в ходе процесса:



5. В таблице 45 краткого справочника физико-химических величин находят значения интегралов М0, М1 и М‒2 при температуре 800 K и 900 K. Величины для 850 K находят как среднее арифметическое для значений температуры 800 и 900 K.
| T, K | M0 | M1∙10‒3 | M2∙10‒6 | M‒2∙105 |
| 800 | 0,3597 | 0,1574 | 0,0733 | 0,2213 |
| 900 | 0,4361 | 0,2012 | 0,1004 | 0,2521 |
| 850 | 0,3979 | 0,1793 | 0,2376 |
6. Подставить данные в расчетную формулу:
 :
:
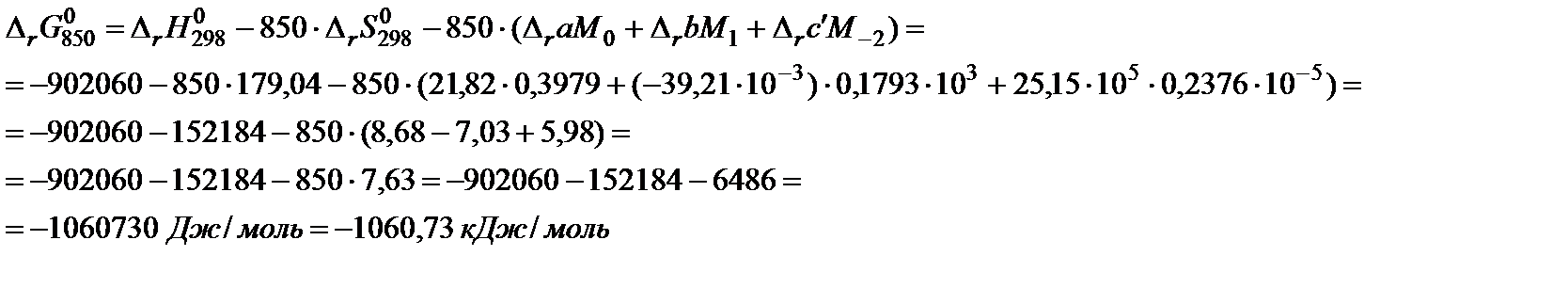
7. Вычислить константу равновесия по формуле:
|
|
|
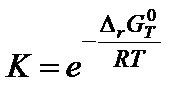 ;
; 
Дата добавления: 2018-05-09; просмотров: 6982; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
