Опыт 2. Электролиз водного раствора сульфата меди (II) с инертными электродами
Уфимский государственный нефтяной технический университет
Кафедра «Общая и аналитическая химия»
Дисциплина «Общая и неорганическая химия»
ОТЧЕТ
по лабораторной работе №4
На тему: «Электролиз водных растворов солей»
Выполнил
студент группы__________ ______________ Фамилия И.О.
(Подпись, дата)
Принял
доцент кафедры ОАХ ______________ Чалова О.Б.
(Подпись, дата)
Цель работы:
- научиться составлять уравнения электролиза водных растворов солей;
- изучить закономерности протекания электролиза водных растворов солей.
Краткая теория.
Электролиз –это …
Потенциал разложения – это….
Потенциал разложения определяется…
Перенапряжение зависит от…
Поляризация электродов – это
При электролизе водных растворов вода может восстанавливаться на ……………….
в соответствии с уравнениями:
(в кислой среде)
(в нейтральной и щелочной среде)
|
|
|
Окислительно-восстановительный потенциал водородного электрода зависит от…………. и может быть рассчитан по уравнению ……………
При электролизе водных растворов вода может окисляться на ……………….
в соответствии с уравнениями:
(в кислой среде)
(в нейтральной и щелочной среде)
Окислительно-восстановительный потенциал кислородного электрода зависит от………… и может быть рассчитан по уравнению ……………
При электролизе водного раствора соли первым осуществляется процесс, характеризующийся…………………………….значением ………………………………….
На катоде первым ………………………..окислитель с ……………………..значением …
На аноде первым ……………………..восстановитель с ……………………..значением …
При электролизе водного раствора соли Na2SO4протекают реакции
на катоде:
на аноде:
суммарное уравнение реакции
При электролизе водного раствора соли NiCl2протекают реакции
на катоде:
|
|
|
на аноде:
суммарные уравнения реакций
Опыт 1. Электролиз водного раствора иодида калия
В U-образную трубку налить раствор иодида калия. В оба колена добавить 4-5 капель фенолфталеина, опустить графитовые электроды, присоединить последние к блоку питания. Пропустить ток.
Отметить внешние изменения в растворе около электродов;
составить уравнение электрохимической диссоциации иодида калия в водном растворе:
KI →
в растворе KI ……………………….среда;
уравнение электролитической диссоциации воды:
к отрицательно заряженному электроду перемещаются ионы………………….
к положительно заряженному электроду перемещаются ионы…………………….
возможные окислители:
используя значения окислительно-восстановительных потенциалов, выбрать наиболее сильный окислитель:
 …………
…………  ; (pH=7)
; (pH=7)
возможные восстановители:
используя значения окислительно-восстановительных потенциалов, выбрать наиболее сильный восстановитель:
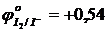 …………
…………  ; (pH=7);
; (pH=7);
составить уравнение катодного процесса восстановления окислителя,
катодная реакция:
составить уравнение анодного процесса окисления восстановителя,
анодная реакция:
составить суммарное уравнение электролиза водного раствора KI, объединив уравнения катодной и анодной реакций с учетом коэффициентов электронного баланса:
|
|
|
 (ионное уравнение);
(ионное уравнение);
 (молекулярное уравнение);
(молекулярное уравнение);
рассчитать минимальный потенциал разложения (без учета перенапряжения), необходимый для протекания электролиза иодида калия;
ответить, какие металлы не выделяются на катоде при электролизе водных растворов их солей.
Вывод:
Опыт 2. Электролиз водного раствора сульфата меди (II) с инертными электродами
Дата добавления: 2018-04-15; просмотров: 445; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
