Газовая постоянная. Универсальная газовая постоянная.
Равновесное состояние идеального газа описывается уравнением Клапейрона — Менделеева  , где р — давление, Па;
, где р — давление, Па;  — молярный объем газа, м3/моль;
— молярный объем газа, м3/моль;  — универсальная газовая постоянная, Дж/(мольК). Универсальная газовая постоянная численно равна работе 1 моля газа в изобарном процессе при повышении температуры на один Кельвин.
— универсальная газовая постоянная, Дж/(мольК). Универсальная газовая постоянная численно равна работе 1 моля газа в изобарном процессе при повышении температуры на один Кельвин.  является фундаментальной физической величиной и для всех газов имеет одно и то же значение. Из закона Авогадро следует, что молярные объемы любых газов при равных температурах и давлениях одинаковы. При нормальных физических условиях
является фундаментальной физической величиной и для всех газов имеет одно и то же значение. Из закона Авогадро следует, что молярные объемы любых газов при равных температурах и давлениях одинаковы. При нормальных физических условиях  =22,4143
=22,4143  . Тогда
. Тогда  Дж/(мольК).
Дж/(мольК).
После деления левой и правой частей уравнения  на молярную массу
на молярную массу 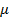 получим уравнение состояния идеального газа в виде рv = RТ, где R — газовая постоянная, зависящая от природы газа и принимающая для различных газов определенные значения, Дж/(кгК).
получим уравнение состояния идеального газа в виде рv = RТ, где R — газовая постоянная, зависящая от природы газа и принимающая для различных газов определенные значения, Дж/(кгК).
Дата добавления: 2015-12-17; просмотров: 55; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
