Гомология алкенов и изомерия алкенов.
26.10.2021
Химия 21
Тема: Строение молекул этилена
Урок посвящён непредельным углеводородам, их номенклатуре, физическим и химическим свойствам, а также роли в жизни человека. В ходе урока учащиеся познакомятся с представителями данного класса органических веществ.
Глоссарий
Алкены – непредельные углеводороды ряда этилена, имеющие одну двойную углерод-углеродную связь
Гибридизация – процесс взаимодействия разных, но близких по энергии электронных орбиталей, приводящий к их выравниванию по форме и энергии.
Гомология – явление сходства по составу, строению, химическим свойствам и принадлежности к тому же классу одного вещества с другим веществом, но различающиеся дуг от друга на одну или несколько групп СН2. Группу СН2 называют гомологической разностью.
Горение – быстро протекающий процесс окисления вещества, сопровождающийся большим выделением тепла и ярким свечением.
Полимеризация – реакция, при которой одинаковые молекулы соединяются между собой в более крупную молекулу
Изомерия – явление существования веществ, одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и вследствие этого по физическим и химическим свойствам. Такие вещества называются изомерами.
Формула структурная – изображение молекулы, в котором показан порядок связывания атомов между собой. Химические связи в таких формулах обозначаются черточками.
|
|
|
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Алкены – непредельные углеводороды, в молекулах которых между атомами углерода имеется одна двойная углерод-углеродная связь. Общая формула алкенов СnH2n, где n≥2.
Простейшим представителем алкенов является этен, или этилен С2Н4.
Структурная формула этилена:

(сокращенная: СН2=СН2).
Особенности пространственного и электронного строения алкенов на примере молекулы этилена
Рассмотрим особенности электронного и пространственного строения алкенов на примере молекулы этилена. Все атомы углерода в молекуле этилена находятся в состоянии sp2-гибридизации. Три гибридных орбитали участвуют в образовании трех достаточно прочных сигма связей (по две связи у каждого атома углерода с атомами водорода и одна общая между собой). Оставшаяся негибридная р-орбиталь образует менее прочную пи-связь между атомами углерода. Таким образом, в молекуле этилена присутствуют 5 сигма-связей и одна пи-связь, причем двойная связь между атомами углерода образована одной сигма и и одно пи-связями. Наличие пи-связей в молекулах алкенов делает невозможным вращение атомов углерода друг относительно друга (имеются ввиду те атомы, при которых находится двойная связь)
|
|
|
Каждый атом углерода в молекуле этилена имеет треугольное строение.
Номенклатура алкенов
Особенности номенклатуры алкенов заключаются в следующем:
1. Нумерация углеродной цепи начинается с того конца, где ближе расположена двойная связь
2. В конце названия изменяется суффикс -ан соответствующего предельного углеводорода на -ен или -илен, и, если это необходимо, указывается атом углерода, при котором находится двойная связь
|
|
|
Рассмотрим пример:

1. Нумерация главной цепи начинается слева направо, так как двойная связь ближе к левой части молекулы.
2. Называем радикал, расположенный у второго атома углерода: 2-метил
3. В главной цепи находится четыре атома углерода, следовательно, она соответствует предельному углеводороду – бутану.
4. Так как присутствует двойная связь, то суффикс – ан меняется на суффикс -ен и указывается положение двойной связи: бутен-1.
5. Соединяем суффикc с корнем и получаем название 2-матилбутен-1.
Гомология алкенов и изомерия алкенов.
Ближайшие гомологи этилена:
С3Н6 пропен (пропилен)
С4Н8 бутен (бутилен)
С5Н10 пентен (амилен)
Для алкенов характерны следующие виды изомерии:
1. Изомерия углеродного скелета
2. Изомерия положения кратной связи
3. Пространственная геометрическая изомерия
4. Межклассовая (с циклоалканами)
Рассмотрим каждый вид изомерии на примере вещества состава С4Н8:
При построении структурной формулы данного вещества возможно расположение двойной связи как между первым и вторым атомами углерода, так и между вторым и третьим, тогда возможно получить две структурные формулы

Данный вид изомерии называется изомерией положения кратных связей.
|
|
|
Для данного вещества возможно построить единственный разветвлённый изомер – изомер углеродного скелета – 2-метилпропен:

Межклассовый изомер бутена – циклобутан:

Также для бутена-2 возможно существование геометрических изомеров, это связано с тем, что метильная группа СН3- может располагаться относительно плоскости двойной связи в двух разных положениях, что приводит к образованию цис- (если эти группы расположены по одну линию связи) и транс-изомеров (если метильные группы расположены по разные линии связи):
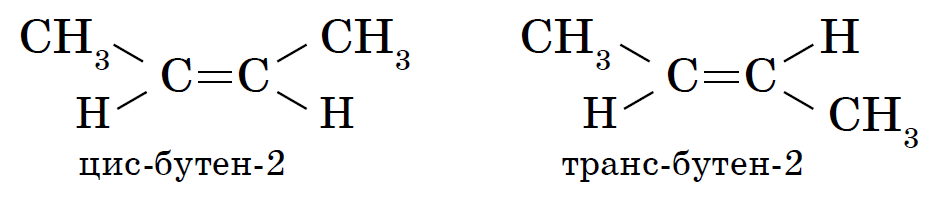
Физические свойства алкенов
Этилен – бесцветный газ, почти без запаха, легче воздуха, плохо растворим в воде. Пропен и бутен – также газы. От пентена до октадецена – жидкости. Остальные – твердые вещества. Все агрегатные состояния указаны при нормальных условиях.
Способы получения алкенов
1. Внутримолекулярная дегидратация спиртов:
Данный способ является основным способом получения этилена в лабораторных условиях. Реакция протекает при температуре выше 140 градусов и в присутствии концентрированной серной кислоты, выполняющей роль катализатора. При дегидратации этанола получают этилен, а при дегидратации пропанола – пропилен:
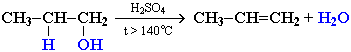
2. Дегидрирование предельных углеводородов.
Данная реакция протекает при нагревании в присутствии катализаторов: никеля, платины, оксида хрома (III). При этом получают соответствующие алкены:

Химические свойства алкенов
Химические свойства алкенов обусловлены наличием в их молекулах двойных углерод-углеродных связей. Дело в том, что пи-связь, как было сказано ранее, является менее устойчивой, чем сигма связь. Поэтому при атаке её каким-либо реагентом она легко разрывается. Это объясняет основные химические свойства алкенов: они способны вступать в реакции присоединения и окисления.
Реакции присоединения
| Гидрирование – присоединение водорода | Протекает при нагревании в присутствии катализаторов: платина, никель, оксид хрома (III). Продуктом реакции всегда является алкан. | |
| Галогенирование – присоединение галогенов | Реакция протекает при обычных условиях. Продукт реакции – дигалогеналкан (1,2 - дибромэтан) | Признак реакции – обесцвечивание раствора брома, поэтому данную реакцию используют как качественную на двойную связь. |
| Гидрогалогенирование – присоединение галогенводородов | Продукт реакции – галогеналкан (хлорэтан) | |
| Гидратация – присоединение воды | Продукт реакции - спирт |
Реакция полимеризации
| Полимеризация – реакция, при которой одинаковые молекулы соединяются в более крупные молекулы. | Условия реакции – высокая температура и давление Продукт реакции – полимер (полиэтилен) | Продукты реакции полимеризации используются для производства пластмасс и синтетических волокон |
Окисление
Дата добавления: 2022-01-22; просмотров: 26; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
