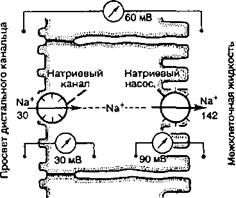
Схема 11.1. Регуляция водо- и электролитовыделительной функции почки
Клубочковая фильтрация
Мысль о фильтрации воды и растворенных веществ как первом этапе мочеобразования была высказана в 1842 г. немецким физиологом К. Людвигом. В 20-х годах XX столетия американскому физиологу А. Ричардсу в прямом эксперименте удалось подтвердить это предположение — с помощью микроманипулятора он пунктировал микропипеткой капсулу клубочка и извлек из нее жидкость, действительно оказавшуюся ультрафильтратом плазмы крови.
Ультрафильтрация воды и низкомолекулярных компонентов из плазмы крови происходит через клубочковый фильтр. Этот фильтрационный барьер почти непроницаем для высокомолекулярных веществ. Процесс ультрафильтрации обусловлен разностью между гидростатическим давлением крови, гидростатическим давлением в капсуле клубочка и онкотическим давлением белков плазмы крови. Общая поверхность капилляров клубочка больше общей поверхности тела человека и достигает 1,5 м2 на 100 г массы почки.
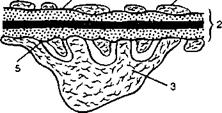
Фильтрующая мембрана (фильтрационный барьер), через которую проходит жидкость из просвета капилляра в полость капсулы клубочка, состоит из трех слоев: эндотелиальных клеток капилляров, базальной мембраны и эпителиальных клеток висцерального (внутреннего) листка капсулы — подоцитов (рис. 11.2).
Клетки эндотелия, кроме области ядра, очень истончены, толщина цитоплазмы боковых частей клетки менее 50 нм; в цитоплазме имеются круглые или овальные отверстия (поры) размером 50—100 нм, которые занимают до 30 % поверхности клетки. При нормальном кровотоке наиболее крупные белковые молекулы образуют барьерный слой на поверхности пор эндотелия и затрудняют движение через них альбуминов, ограничивая тем самым прохождение форменных элементов крови и белков через эндотелий. Другие компоненты плазмы крови и вода могут свободно проходить через эндотелий и достигать базальной мембраны.
|
|
|
Базальная мембрана — важнейшая составная часть фильтрующей мембраны клубочка. У человека толщина базальной мембраны 250—400 нм. Эта
| |||
| |||
Рис. 11.2. Строение фильтрующей мембраны клубочка.
1 — эндотелий; 2 — базальная мембрана; 3 — подоцит; 4 — отверстие в эндотелии; 5 — шелевая мембрана подоцита.
мембрана состоит из трех слоев — центрального и двух периферических. Поры в базальной мембране препятствуют прохождению молекул диаметром больше 6 нм.
Наконец, важную роль в качестве барьера для фильтруемых веществ играют щелевые мембраны между «ножками» подоцитов. Эти эпителиальные клетки обращены в просвет капсулы почечного клубочка и имеют отростки — «ножки», которыми прикрепляются к базальной мембране. Базальная мембрана и щелевые мембраны между этими «ножками» ограничивают фильтрацию веществ, диаметр молекул которых больше 6,4 нм (т.е. не проходят вещества, радиус молекулы которых превышает 3,2 нм). Поэтому в просвет нефрона свободно проникает инулин (радиус молекулы 1,48 нм, мол. м. около 5200), может фильтроваться лишь 22 % яичного альбумина (радиус мол. 2,85 нм, мол. м. 43 500), 3 % гемоглобина (радиус мол. 3,25 нм, мол. м. 68 000) и меньше 1 % сывороточного альбумина (радиус мол. 3,55 нм, мол. м. 69 000).
|
|
|
Прохождению белков через клубочковый фильтр препятствуют отрицательно заряженные молекулы — полианионы, входящие в состав вещества базальной мембраны, и сиалогликопротеиды в выстилке, лежащей на поверхности подоцитов и между их «ножками». Ограничение для фильтрации белков, имеющих отрицательный заряд, обусловлено размером пор клубочкового фильтра и их электронегативностью. Таким образом, состав клубочкового фильтрата зависит от свойств эпителиального барьера и базальной мембраны. Естественно, размер и свойства пор фильтрационного барьера вариабельны, поэтому в обычных условиях в ультрафильтрате обнаруживают лишь следы белковых фракций, характерных для плазмы крови. Прохождение достаточно крупных молекул через поры зависит не только от их размера, но и конфигурации молекулы, ее заряда и пространственного соответствия форме поры.
|
|
|
Величина клубочковой фильтрации зависит от разности между гидростатическим давлением крови (около 70 мм рт. ст. в капиллярах клубочка), онкотическим давлением белков плазмы крови (около 30 мм рт. ст.) и гидростатическим давлением в капсуле клубочка (около 20 мм рт. ст.). Эффективное фильтрационное давление, т.е. давление, которое определяет клубочковую фильтрацию, составляет примерно 20 мм рт. ст. [70 мм рт. ст. — (30 мм рт. ст. + 20 мм рт. ст.) = 20 мм рт. ст.]. Фильтрация происходит только в том случае, если давление крови в капиллярах клубочков превышает сумму онкотического давления белков в плазме и величину давления жидкости в капсуле клубочка.
Ультрафильтрат практически не содержит белков; он подобен плазме по общей концентрации осмотически активных веществ, глюкозы, мочевины, мочевой кислоты, креатинина и др. Небольшое различие концентрации ряда ионов по обеим сторонам клубочковой мембраны обусловлено 496
равновесием Доннана — наличием в плазме крови анионов, не диффундирующих через мембрану и удерживающих часть катионов. Следовательно, для расчета количества фильтруемых веществ в клубочках необходимо учитывать, какая их часть может проходить из плазмы крови в просвет нефрона через гломерулярный фильтр.
|
|
|
Для внесения поправки на связывание некоторых ионов белками плазмы крови вводится понятие об ультрафилыпруемой фракции (f) — той части вещества в плазме от общего его количества в плазме крови, которая не связана с белком и свободно проходит через клубочковый фильтр. Ультра- фильтруемая фракция для кальция составляет 60 %, магния — 75 %. Эти величины свидетельствуют о том, что около 40 % кальция и 25 % магния плазмы связаны с белком и не фильтруются в клубочках. Однако в профильтровавшейся жидкости кальций (и магний) также представлен двумя фракциями: одна из них — ионизированный кальций (магний), другая — кальций (магний), связанный с низкомолекулярными соединениями, проходящими через клубочковый фильтр.
В ультрафильтрате обнаруживают следы белка. Различие размера пор в клубочках даже у здорового человека обусловливает проникновение небольшого количества обычно измененных белков; из нормальной мочи удалось выделить в следовых количествах белковые фракции, характерные для плазмы крови.
Измерение скорости клубочковой фильтрации. Для расчета объема жидкости, фильтруемой в 1 мин в почечных клубочках (скорость клубочковой фильтрации), и ряда других показателей процесса мочеобразования используют методы и формулы, основанные на принципе очищения (клиренс). Для измерения величины клубочковой фильтрации используют физиологически инертные вещества, не токсичные и не связывающиеся с белком в плазме крови, свободно проникающие через поры мембраны клубочкового фильтра из просвета капилляров вместе с безбелко- вой частью плазмы. Следовательно, концентрация этих веществ в клубочковой жидкости будет такой же, как в плазме крови. Эти вещества не должны реабсорбироваться и секретироваться в почечных канальцах, поэтому с мочой будет выделяться все количество данного вещества, поступившего в просвет нефрона с ультрафильтратом в клубочках. К веществам, используемым для измерения скорости клубочковой фильтрации, относятся полимер фруктозы инулин, маннитол, полиэтиленгликоль-400, креатинин.
Рассмотрим принцип очищения на примере измерения объема клубочковой фильтрации с помощью инулина. Количество профильтровавшегося в клубочках инулина (In) равно произведению объема фильтрата (С(П) на концентрацию в нем инулина (она равна его концентрации в плазме крови, Р|п). Выделившееся за то же время с мочой количество инулина равно произведению объема экскретированной мочи (V) на концентрацию в ней инулина (U]n).
Так как инулин не реабсорбируется и не секретируется, то количество профильтровавшегося инулина (С(п Р|П) равно количеству выделившегося (V Р!п), откуда:
С1п = V UIn /Р|л.
Эта формула является основной для расчета скорости клубочковой фильтрации. При использовании других веществ для измерения скорости клубочковой фильтрации инулин в формуле заменяют на анализируемое вещество и рассчитывают скорость клубочковой фильтрации данного вещества, например креатинина. Скорость фильтрации жидкости вычисляют в мл/мин; для сопоставления величины клубочковой фильтрации у людей различных массы тела и роста ее относят к стандартной площади поверхности тела человека (1,73 м2). В норме у мужчин в обеих почках скорость клубочковой фильтрации на 1,73 м2 составляет около 125 мл/мин, у женщин — приблизительно 110 мл/мин.
Измеренная с помощью инулина величина фильтрации в клубочках, называемая также коэффициентом очищения от инулина (инулиновый клиренс), показывает, какой объем плазмы крови освобожден от инулина за это время. Для измерения очищения от инулина необходимо непрерывно вводить в вену раствор инулина, чтобы в течение всего исследования поддерживать постоянной его концентрацию в крови. Очевидно, что это весьма сложно и в клинике не всегда осуществимо, поэтому чаще используют креатинин — естественный компонент плазмы, по очищению от которого можно было бы судить о скорости клубочковой фильтрации, хотя с его помощью скорость клубочковой фильтрации измеряется менее точно, чем при инфузии инулина. При некоторых физиологических, и особенно патологических, состояниях креатинин может реабсорбироваться и секретироваться, поэтому очищение от креатинина не отражает истинной величины клубочковой фильтрации.
У здорового человека вода попадает в просвет нефрона в результате фильтрации в клубочках, реабсорбируется в канальцах, и вследствие этого концентрация инулина растет. Концентрационный показатель инулина Uin/P.n указывает, во сколько раз уменьшается объем фильтрата при его прохождении по канальцам. Эта величина имеет важное значение для суждения об особенностях обработки любого вещества в канальцах, для ответа на вопрос о том, подвергается ли вещество реабсорбции или секретируется клетками канальцев. Если концентрационный показатель данного вещества X Ux/Px меньше, чем одновременно измеренная величина Uin/Pin, то это указывает на реабсорбцию вещества X в канальцах. Если Ux/Px больше, чем U]n/Pin, то это указывает на его секрецию. Отношение концентрационных показателей вещества X и инулина Ux/Px U[n/P]n носит название экскретируемой фракции (EF).
Канальцевая реабсорбция
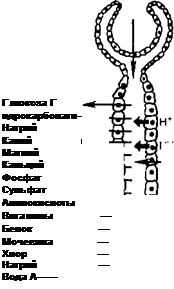
Начальный этап мочеобразования, приводящий к фильтрации всех низкомолекулярных компонентов плазмы крови, неизбежно должен сочетаться с существованием в почке систем, реабсорбирующих все ценные для организма вещества. В обычных условиях в почке человека за сутки образуется до 180 л фильтрата, а выделяется 1,0—1,5 л мочи, остальная жидкость всасывается в канальцах. Роль клеток различных сегментов нефрона в реабсорбции неодинакова. Проведенные на животных опыты с извлечением микропипеткой жидкости из различных участков нефрона позволили выяснить особенности реабсорбции различных веществ в разных частях почечных канальцев (рис. 11.3). В проксимальном сегменте нефрона практически полностью реабсорбируются аминокислоты, глюкоза, витамины, белки, микроэлементы, значительное количество ионов Na+, С1_, НСОз В последующих отделах нефрона всасываются преимущественно электролиты и вода.
Реабсорбция натрия и хлора представляет собой наиболее значительный по объему и энергетическим тратам процесс. В проксимальном канальце в результате реабсорбции большинства профильтровавшихся веществ и
 |
| ||||
| ||||
 | |||
 | |||
| ||||||
| ||||||
| ||||||
 |
| ||||||||||||||
 | ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
 |
Рис. 11.3. Локализация реабсорбции и секреции веществ в почечных канальцах. Направление стрелок указывает на фильтрацию, реабсорбцию и секрецию веществ.
воды объем первичной мочи уменьшается, и в начальный отдел петли нефрона поступает около % профильтровавшейся в клубочках жидкости. Из всего количества натрия, поступившего в нефрон при фильтрации, в петле нефрона всасывается до 25 %, в дистальном извитом канальце — около 9 % и менее 1 % реабсорбируется в собирательных трубках или экскретируется с мочой.
Реабсорбция в дистальном сегменте характеризуется тем, что клетки переносят меньшее, чем в проксимальном канальце, количество ионов, но против большего градиента концентрации. Этот сегмент нефрона и собирательные трубки играют важнейшую роль в регуляции объема выделяемой мочи и концентрации в ней осмотически активных веществ (осмоти
ческая концентрация)[I]. В конечной моче концентрация натрия может снижаться до 1 ммоль/л по сравнению со 140 ммоль/л в плазме крови. В дистальном канальце калий не только реабсорбируется, но и секретируется при его избытке в организме.
В проксимальном отделе нефрона реабсорбция натрия, калия, хлора_и других веществ происходит через высокопроницаемую для воды мембрану стенки канальца. Напротив; в толстом восходящем отделе петли нефрона, дистальных извитых канальцах и собирательных трубках реабсорбция ионов и воды происходит через малопроницаемую для воды стенку канальца; проницаемость мембраны для воды в отдельных участках нефрона и собирательных трубках может регулироваться, а величина проницаемости изменяется в зависимости от функционального состояния организма (факультативная реабсорбция). Под влиянием импульсов, поступающих по эфферентным нервам, и при действии биологически активных веществ реабсорбция натрия и хлора регулируется в проксимальном отделе нефрона. Это особенно отчетливо проявляется в случае увеличения объема крови и внеклеточной жидкости, когда уменьшение реабсорбции в проксимальном канальце способствует усилению экскреции ионов и воды и тем самым — восстановлению водносолевого равновесия. В проксимальном канальце всегда сохраняется изоосмия. Стенка канальца проницаема для воды, и объем реабсорбируемой воды определяется количеством реабсорбируемых осмотически активных веществ, за которыми вода движется по осмотическому градиенту. В конечных частях дистального сегмента нефрона и собирательных трубках проницаемость стенки канальца для воды регулируется вазопрессином.
Факультативная реабсорбция воды зависит от осмотической проницаемости канальцевой стенки, величины осмотического градиента и скорости движения жидкости по канальцу.
Для характеристики всасывания различных веществ в почечных канальцах существенное значение имеет представление о пороге выведения. Непороговые вещества выделяются при любой их концентрации в плазме крови (и соответственно в ультрафильтрате). Такими веществами являются инулин, маннитол. Порог выведения практически всех физиологически важных, ценных для организма веществ различен. Так, выделение глюкозы с мочой (глюкозурия) наступает тогда, когда ее концентрация в клубочковом фильтрате (и в плазме крови) превышает 10 ммоль/л. Физиологический смысл этого явления будет раскрыт при описании механизма реабсорбции.
Механизмы канальцевой реабсорбции. Обратное всасывание различных веществ в канальцах обеспечивается активным и пассивным транспортом. Если вещество реабсорбируется против электрохимического и концентрационного градиентов, процесс называется активным транспортом. Различают два вида активного транспорта — первично-активный и вторично-активный. Первично-активным транспорт называется в том случае, когда происходит перенос вещества против электрохимического градиента за счет энергии клеточного метаболизма. Примером служит транспорт ионов Na+, который происходит при участии фермента №+-К.+-АТФазы, использующей энергию АТФ. Вторично-активным называется перенос вещества против концентрационного градиента, но без затраты энергии клетки непосредственно на этот процесс; так реабсорбируются глюкоза, аминокислоты. Из просвета канальца эти органические вещества поступают в клетки проксимального канальца с помощью специального переносчика, который обязательно должен присоединить ион Na+ Этот комплекс (переносчик + органическое вещество + Na+) способствует перемещению вещества через мембрану щеточной каемки и его поступлению внутрь клетки. Движущей силой переноса этих веществ через апикальную плазматическую мембрану служит меньшая по сравнению с просветом канальца концентрация натрия в цитоплазме клетки. Градиент концентрации натрия обусловлен непрестанным активным выведением натрия из клетки во внеклеточную жидкость с помощью №+-К+-АТФазы, локализованной в латеральных и базальной мембранах клетки.
Реабсорбция воды, хлора и некоторых других ионов, мочевины осуществляется с помощью пассивного транспорта — по электрохимическому, концентрационному или осмотическому градиенту. Примером пассивного транспорта является реабсорбция в дистальном извитом канальце хлора по электрохимическому градиенту, создаваемому активным транспортом натрия. По осмотическому градиенту транспортируется вода, причем скорость ее всасывания зависит от осмотической проницаемости стенки канальца и разности концентрации осмотически активных веществ по обеим сторонам его стенки. В содержимом проксимального канальца вследствие всасывания воды и растворенных в ней веществ растет концентрация мочевины, небольшое количество которой по концентрационному градиенту реабсорбируется в кровь.
Достижения в области молекулярной биологии позволили установить строение молекул ионных и водных каналов (аквапорины), рецепторов, гормонов и тем самым проникнуть в сущность некоторых клеточных механизмов, обеспечивающих транспорт веществ через стенку канальца. Различны свойства клеток разных отделов нефрона, неодинаковы свойства цитоплазматической мембраны в одной и той же клетке. Апикальная мембрана клетки, обращенная в просвет канальца, имеет иные характеристики, чем ее базальная и боковые мембраны, омываемые межклеточной жидкостью и соприкасающиеся с кровеносным капилляром. Вследствие этого апикальная и базальная плазматические мембраны участвуют в транспорте веществ по-разному; специфично и действие биологически активных веществ на ту и другую мембраны.
Клеточный механизм реабсорбции ионов рассмотрим на примере Na+. В проксимальном канальце нефрона всасывание Na+ в кровь происходит в результате, ряда процессов, один из которых — активный транспорт Na+ из просвета канальца, другой — пассивная реабсорбция Na+ вслед за активно транспортируемыми в кровь как ионами гидрокарбоната, так и С1_ При введении одного микроэлектрода в просвет канальцев, а второго — в око- локанальцевую жидкость было выявлено, что разность потенциалов между наружной и внутренней поверхностью стенки проксимального канальца оказалась очень небольшой — около 1,3 мВ; в области дистального канальца она может достигать 60 мВ (рис. 11.4). Просвет обоих канальцев электроотрицателен, а в крови (следовательно, и во внеклеточной жидкости) концентрация Na+ выше, чем в жидкости, находящейся в просвете этих канальцев, поэтому реабсорбция Na+ осуществляется активно против градиента электрохимического потенциала. При этом из просвета канальца Na+ входит в клетку по натриевому каналу или при участии переносчика. Внутренняя часть клетки заряжена отрицательно, и положительно заряженный Na+ поступает в клетку по градиенту потенциала, движется в сторону базальной плазматической мембраны, через которую натриевым
|
|
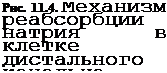 |
насосом выводится в межклеточную жидкость; градиент потенциала на этой мембране достигает 70—90 мВ.
Имеются вещества, которые могут влиять на отдельные элементы системы реабсорбции Na+ Так, натриевый канал в мембране клетки дистального канальца и собирательной трубки блокируется амилоридом и триам- тереном, в результате чего Na+ не может войти в канал. В клетках имеется несколько типов ионных насосов. Один из них представляет собой №+-К+-АТФазу. Этот фермент находится в базальной и латеральных мембранах клетки и обеспечивает транспорт Na+ из клетки в кровь и поступление из крови в клетку К+ Фермент угнетается сердечными гликозидами, например строфантином, уабаином. В реабсорбции гидрокарбоната важная роль принадлежит ферменту карбоангидразе, ингибитором которого является ацетазоламид — он прекращает реабсорбцию гидрокарбоната, который экскретируется с мочой.
Фильтоуемая глюкоза практически полностью реабсорбируется клетками проксимального канальца, и в норме за сутки с мочой выделяется незначительное (не более 130 мг) ее количество. Процесс обратного всасывания глюкозы осуществляется против высокого концентрационного градиента и является вторично-активным. В апикальной (люминальная) мембране клетки гйЮкоза соединяется с переносчиком, который должен присоединить также Na+, после чего комплекс транспортируется через апикальную мембрану, т.е. в цитоплазму поступают глюкоза и Na+ Апикальная мембрана отличается высокой селективностью и односторонней проницаемостью и не пропускает ни глюкозу, ни Na+ обратно из клетки в просвет канальца. Эти вещества движутся к основанию клетки по градиенту концентрации. Перенос глюкозы из клетки в кровь через базальную плазматическую мембрану носит характер облегченной диффузии, a Na+, как уже отмечалось выше, удаляется натриевым насосом, находящимся в этой мембране.
Аминокислоты почти полностью реабсорбируются клетками проксимального канальца. Имеется не менее 4 систем транспорта аминокислот из просвета канальца в кровь, осуществляющих реабсорбцию нейтральных, двуосновных, дикарбоксильных аминокислот. Каждая из этих систем обеспечивает всасывание ряда аминокислот одной группы. Так, система реабсорбции двуосновных аминокислот участвует во всасывании лизина, аргинина, орнитина и, возможно, цистина. При введении в кровь избытка одной из этих аминокислот начинается усиленная экскреция почкой аминокислот 502
только данной группы. Системы транспорта отдельных групп аминокислот контролируются раздельными генетическими механизмами. Описаны наследственные заболевания, одним из проявлений которых служит увеличенная экскреция определенных групп аминокислот (аминоацидурия).
Выделение с мочой слабых кислот и оснований зависит от их клубочковой фильтрации, процесса реабсорбции или секреции. Процесс выведения этих веществ во многом определяется «неионной диффузией», влияние которой особенно сказывается в дистальных канальцах и собирательных трубках. Слабые кислоты и основания могут существовать в зависимости от pH среды в двух формах — неионизированной и ионизированной. Клеточные мембраны более проницаемы для неионизированных веществ. Многие слабые кислоты с большей скоростью экскретируются с щелочной мочой, а слабые основания, напротив, — с кислой. Степень ионизации оснований увеличивается в кислой среде, но уменьшается в основной. В неионизированном состоянии эти вещества через липиды мембран проникают в клетки, а затем в плазму крови, т.е. они реабсорбируются. Если значение pH канальцевой жидкости сдвинуто в кислую сторону, то основания ионизируются, плохо всасываются и экскретируются с мочой. Никотин — слабое основание, при pH 8,1 ионизируется 50 %, в 3—4 раза быстрее экскретируется с кислой (pH около 5), чем с основной (pH 7,8) мочой. Процесс «неионной диффузии» влияет на выделение почками слабых оснований и кислот, барбитуратов и других лекарственных веществ.
Небольшое количество профильтровавшегося в клубочках белка реабсорбируется клетками проксимальных канальцев. Выделение белков с мочой в норме составляет не более 20—75 мг/сут, а при заболеваниях почек оно может возрастать до 50 г/сут. Увеличение выделения белков с мочой (протеинурия) может быть обусловлено нарушением их реабсорбции либо увеличением фильтрации.
В отличие от реабсорбции электролитов, глюкозы и аминокислот, которые, проникнув через апикальную мембрану, в неизмененном виде достигают базальной плазматической мембраны и транспортируются в кровь, реабсорбция белка обеспечивается принципиально иным механизмом. Белок попадает в клетку с помощью пиноцитоза. Молекулы профильтровавшегося белка адсорбируются на поверхности апикальной мембраны клетки, при этом мембрана участвует в образовании пиноцитозной вакуоли. Эта вакуоль движется в сторону базальной части клетки. В околоядерной области, где локализован пластинчатый комплекс (аппарат Гольджи), вакуоли могут сливаться с лизосомами, обладающими высокой активностью ряда ферментов. В лизосомах захваченные белки расщепляются и образовавшиеся аминокислоты, дипептиды удаляются в кровь через базальную плазматическую мембрану. Однако не все белки подвергаются гидролизу в процессе транспорта и часть их переносится в кровь в неизмененном виде.
Определение величины реабсорбции в канальцах почки. Обратное всасывание веществ, или, иными словами, их транспорт (Т) из просвета канальцев в тканевую (межклеточную) жидкость и в кровь, при реабсорбции R (TR) определяется по разности между количеством вещества X (F ₽х fx), профильтровавшегося в клубочках, и количеством вещества, выделенного с мочой (Ux V).
Tr = F Рх fx-Ux v,
где F — объем клубочковой фильтрации, fx — фракция вещества X, не связанная с белками в плазме по отношению к его общей концентрации в плазме крови, В — концентрация вещества в плазме крови, V — концентрация вещества в моче.
По приведенной формуле рассчитывают абсолютное количество реабсорбируемого вещества. При вычислении относительной реабсорбции (% R) определяют долю вещества, подвергшуюся обратному всасыванию по отношению к количеству вещества, профильтровавшегося в клубочках:
% R = (I — EFX) 100.
Для оценки реабсорбционной способности клеток проксимальных канальцев важное значение имеет определение максимальной величины транспорта глюкозы (Ттс). Эту величину измеряют при полном насыщении глюкозой системы ее канальцевого транспорта. Для этого вводят в кровь раствор глюкозы и тем самым повышают ее концентрацию в клубочковом фильтрате до тех пор, пока значительное количество глюкозы не начнет выделяться с мочой:
TmG = F Pg-Ug V,
где F — клубочковая фильтрация, Pg — концентрация глюкозы в плазме крови, a L)g — концентрация глюкозы в моче; Тт — максимальный канальцевый транспорт изучаемого вещества. Величина TmG характеризует полную загрузку системы транспорта глюкозы; у мужчин эта величина равна 375 мг/мин, а у женщин — 303 мг/мин при расчете на 1,73 м2 поверхности тела.
Канальцевая секреция
В выделении продуктов обмена и чужеродных веществ имеет значение их секреция из крови в просвет канальца против концентрационного и электрохимического градиентов. Этот дополнительный механизм выделения ряда веществ, помимо их фильтрации в клубочках, позволяет быстро экскретировать некоторые органические кислоты и основания, а также некоторые ионы, например К+ Секреция органических кислот (феноловый красный, ПАГ, диодраст, пенициллин) и органических оснований (холин) происходит в проксимальном сегменте нефрона и обусловлена функционированием специальных систем транспорта. Калий секретируется в конечных частях дистального сегмента и собирательных трубках. Рассмотрим механизм процесса секреции органических кислот на примере выделения почкой ПАГ. При введении ПАГ в кровь человека ее выделение с мочой зависит от фильтрации в клубочках и секреции клетками канальцев. Когда секреция ПАГ достигает максимального уровня (Ттпрдн), она становится постоянной и не зависит от содержания ПАГ в плазме крови. Механизм секреции органических кислот включает ряд этапов. В базальной плазматической мембране имеется Ма+-К+-АТФаза, которая удаляет из клетки ионы Na+ и способствует поступлению в клетку ионов К+ Более низкая концентрация в цитоплазме ионов Na+ позволяет поступать внутрь клетки ионам Na+ по градиенту концентрации при участии натриевых котранспортеров. Один из типов такого котранспортера способствует поступлению через базальную плазматическую мембрану а-кетоглутарата и Na+ В этой же мембране имеется анионный обменник, который удаляет из цитоплазмы а-кетоглутарат в обмен на поступающий из межклеточной жидкости в клетку парааминогиппурат, диодраст или некоторые иные органические кислоты. Это вещество движется по клетке в сторону люминальной мембраны и через нее проходит в просвет канальца по механизму облегченной диффузии. Угнетение дыхания цианидами, разобщение дыхания и окислительного фосфорилирования в присутствии динитрофенола снижают и прекращают секрецию. Уровень секреции зависит от числа переносчиков в мембране. Секреция ПАГ возрастает пропорционально увеличению концентрации ПАГ в крови до тех пор, пока все молекулы переносчика не насыщаются ПАГ. Максимальная скорость транспорта ПАГ достигается в тот момент, когда количество ПАГ, доступное для транспорта, становится равным количеству молекул переносчика, которые могут образовывать комплекс с ПАГ.
Поступившая в клетку ПАГ движется по цитоплазме к апикальной мембране и с помощью имеющегося в ней специального механизма выделяется в просвет канальца. Способность клеток почки к секреции органических кислот и оснований носит адаптивный характер. Если в течение нескольких дней часто инъецировать ПАГ (или пенициллин), то интенсивность секреции возрастает. Это обусловлено тем, что в клетках проксимальных канальцев при участии систем белкового синтеза вырабатываются вещества, являющиеся необходимыми компонентами процесса переноса через мембрану органических веществ.
Подобно секреции органических кислот, секреция органических оснований (например, холин) происходит в проксимальном сегменте нефрона и характеризуется Тт. Системы секреции органических кислот и оснований функционируют независимо друг от друга, при угнетении секреции органических кислот секреция оснований не нарушается.
Транспорт в нефроне К+ характеризуется тем, что К+ не только подвергается обратному всасыванию, но и секретируется клетками эпителия конечных отделов нефрона и собирательных трубок. При реабсорбции из просвета канальца К+ поступает в эпителиальную клетку, где концентрация К+ во много раз выше, чем в канальцевой жидкости, и К+ диффундирует из клетки через базальную плазматическую мембрану в тканевую интерстициальную жидкость, а затем уносится кровью. При секреции К+ поступает в клетку в обмен на Na+ через эту же мембрану с помощью натрий-калиевого насоса, который удаляет Na+ из клетки; тем самым поддерживается высокая внутриклеточная концентрация К+ При избытке К+ в организме система регуляции стимулирует его секрецию клетками канальцев. Возрастает проницаемость для К+ мембраны клетки, обращенной в просвет канальца, появляются «каналы», по которым К+ по градиенту концентрации может выходить из клетки. Скорость секреции К+ зависит от градиента электрохимического потенциала на этой мембране клетки: чем больше электроотрицательность апикальной мембраны, тем выше уровень секреции. При введении в кровь и поступлении в просвет канальца слабо реабсорбируемых анионов, например сульфатов, увеличивается секреция К+ Таким образом секреция К+ зависит от его внутриклеточной концентрации, проницаемости для К+ апикальной мембраны клетки и градиента электрохимического потенциала этой мембраны. При дефиците К+ в организме клетки конечных отделов нефрона и собирательных трубок прекращают секрецию К+ и только реабсорбируют его из канальцевой жидкости. В этом случае К+ из просвета канальца транспортируется через апикальную плазматическую мембрану внутрь клетки, движется по цитоплазме в сторону основания клетки и через базальную плазматическую мембрану поступает в тканевую жидкость, а затем в кровь. Приведенные данные указывают на высокую пластичность клеток этих отделов канальцев, способных под влиянием регуляторных факторов перестраивать свою деятельность, изменяя направление транспорта К+, осуществляя то его реабсорбцию, то секрецию.
Определение величины канальцевой секреции. Секреторную функцию проксимальных канальцев измеряют с помощью веществ, которые выделяются из организма главным образом посредством канальцевой секреции. В кровь вводят ПАГ (или диодраст) вместе с инулином, который служит для измерения клубочковой фильтрации. Величина транспорта (Т) органического вещества (Т5рдц) при секреции (S) его из крови в просвет канальца определяется по разности между количеством этого вещества, выделенным почкой (UpAH V), и количеством попавшего в мочу вследствие фильтрации в (Cjn Ррдн):
TSPAH = UpAH V — С1п РрАН’
Приведенная формула характеризует величину секреции вещества почкой при любом уровне загрузки секреторной системы. В то же время мерой работы секреторного аппарата почки служит его максимальная загрузка.
При условии полного насыщения секреторного аппарата ПАГ определяется величина максимального канальцевого транспорта ПАГ (Тгпрдц), которая является мерой количества функционирующих клеток проксимальных канальцев. У человека Тгпрдн составляет 80 мг/мин на 1,73 м2 поверхности тела.
11.2.4. Определение величины почечного плазмо- и кровотока
Непрямые методы измерения величины почечного кровотока основаны на оценке способности клеток почечных канальцев к секреции — практически полному извлечению из околоканальцевой жидкости (и соответственно из плазмы крови) ряда органических кислот и их секреции в просвет канальца. С этой целью используют ПАГ или диодраст, которые секретируются клетками почечных канальцев столь эффективно, что при невысокой их концентрации в артериальной крови она полностью очищается от этих веществ при однократном прохождении через почку. Используя те же обозначения, можно рассчитать очищение от ПАГ по формуле:
СрАН ~ V Пран / Г РАН*
Это позволяет измерить величину эффективного почечного плазмотока, т.е. то количество плазмы, которое протекает по сосудам коркового вещества почки и омывает клетки проксимального сегмента нефрона. Так как эритроциты не содержат ПАГ, для расчета величины эффективного почечного кровотока (ERBF) необходимо ввести в формулу величину, учитывающую соотношение между эритроцитами и плазмой крови (показатель гематокрита — Ht):
ERBF = CpAH/(l - Ht).
Выше шла речь об эффективном плазмотоке и кровотоке. Для определения общего кровотока и плазмотока через почки необходимо знать, сколько ПАГ остается в оттекающей из почки крови. Так как считается, что ПАГ полностью извлекается из крови, протекающей по корковому веществу почки, то наличие в почечной вене небольшого количества ПАГ обусловлено тем, что часть крови минует корковое вещество почки и поступает в сосуды мозгового вещества. Доля кровотока через мозговое вещество почки составляет около 9 %, а кровоток во внутреннем мозговом веществе (сосочек) равен лишь 1 % от общего почечного кровотока.
У мужчин эффективный почечный плазмоток составляет около 655 мл/мин (на 1,73 м2 площади поверхности тела), общий плазмоток равен 720 мл/мин, а общий кровоток через почки — 1300 мл/мин. Чтобы определить, сколько жидкости из плазмы крови подвергается клубочковой фильтрации, рассчитывают фильтрационную фракцию (FF):
FF = С|П / Срдн-
Фильтрационная фракция составляет около 0,2, т.е. равна почти 20 % от объема плазмы, протекающей через почку.
11.2.5. Синтез веществ в почках
В почках образуются некоторые вещества, выделяемые в мочу (например, гиппуровая кислота, аммиак) или поступающие в кровь (ренин, простагландины, глюкоза, синтезируемая в почке, и др.). Гиппуровая кислота образуется в клетках канальцев из бензойной кислоты и гликокола. В опытах на изолированной почке было показано, что при введении в артерию раствора бензойной кислоты и гликокола в моче появляется гиппуровая кислота. В клетках канальцев при дезаминировании аминокислот, главным образом глутамина, из аминогрупп образуется аммиак. Он поступает преимущественно в мочу, частично проникает и через базальную плазматическую мембрану в кровь, и в почечной вене аммиака больше, чем в почечной артерии.
11.2.6. Осмотическое разведение и концентрирование мочи
Способностью к осмотическому разведению мочи, т. е. способностью к выделению мочи с меньшей концентрацией осмотически активных веществ, а следовательно, с меньшим осмотическим давлением, чем плазма крови, обладают почки млекопитающих, птиц, рептилий, амфибий, пресноводных рыб и круглоротых. В то же время способностью к образованию мочи с большей концентрацией осмотически активных веществ, т. е. с большей осмотической концентрацией, чем кровь, обладают лишь почки теплокровных животных. Многие исследователи пытались разгадать физиологический механизм этого процесса, но лишь в начале 50-х годов XX века была обоснована гипотеза, согласно которой образование осмотически концентрированной мочи обусловлено деятельностью поворотнопротивоточной множительной системы в почке.
Принцип противоточного обмена достаточно широко распространен в природе и используется в технике. Механизм работы такой системы рассмотрим на примере кровеносных сосудов в конечностях арктических животных. Во избежание больших потерь тепла кровь в параллельно расположенных артериях и венах конечностей течет таким образом, что теплая
Вена Q ir 15° 13° 11° 9° 7° 5° 3° 1° А Артерия (рУ 17° 15° 13" 11° 9° 7° 5°
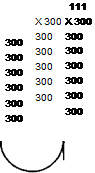 | |||||
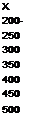 | |||||
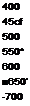 | |||||
|
 | ||||||
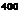 | ||||||
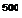 | ||||||
 | ||||||
 | ||||||
| ||||
| ||||
 |
артериальная кровь согревает охлажденную венозную кровь, движущуюся к сердцу (рис. 11.5, А). В стопу притекает артериальная кровь низкой температуры, что резко уменьшает теплоотдачу. Здесь такая система функционирует только как противоточный обменник; в почке же она обладает множительным эффектом, т. е. увеличением эффекта, достигаемого в каждом из отдельных сегментов системы. Для лучшего понимания ее работы рассмотрим систему, состоящую из трех параллельно расположенных трубок (рис. 11.5, Б). Трубки I и II дугообразно соединены на одном из концов. Стенка, общая для обеих трубок, обладает способностью переносить ионы, но не пропускать воду. Когда в такую систему через вход I наливают раствор концентрации 300 мосмоль/л (рис. 11.5, Б, а) и он не течет, то через некоторое время в результате транспорта ионов в трубке I раствор станет гипотоническим, а в трубке II — гипертоническим. В том случае, когда жидкость течет по трубкам непрерывно, начинается концентрирование осмотически активных веществ (рис. 11.5, Б, б). Перепад их концентраций на каждом уровне трубки вследствие одиночного эффекта транспорта ионов нс превышает 200 мосмоль/л, однако по длине трубки происходит умножение одиночных эффектов, и система начинает работать как противоточная множительная. Так как по ходу движения жидкости из нее извлекаются не только ионы, но и некоторое количество воды, концентрация раствора все более повышается по мере приближения к изгибу петли. В отличие от трубок I и II в трубке III регулируется проницаемость стенок для воды: когда стенка становится водопроницаемой — начинает пропускать воду, объем жидкости в ней уменьшается. При этом вода идет в сторону большей осмотической концентрации в жидкость возле трубки, а соли остаются внутри трубки. В результате этого растет концентрация ионов в трубке III и уменьшается объем содержащейся в ней жидкости. Концентрация в ней веществ будет зависеть от ряда условий, в том числе от работы противоточной множительной системы трубок I и II. Как будет ясно из последующего изложения, работа почечных канальцев в процессе осмотического концентрирования мочи похожа на описанную модель.
В зависимости от состояния водного баланса организма почки выделяют гипотоническую (осмотическое разведение) или, напротив, осмотически концентрированную (осмотическое концентрирование) мочу. В про- 508
|
|
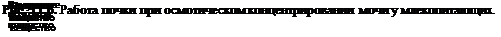 |
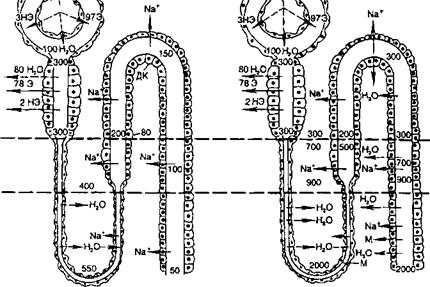
А — состояние водного диуреза; Б — состояние антидиуреза; Э — электролиты; НЭ — неэлектролиты; ДК — дистальный сегмент нефрона; М — мочевина. Цифры у просвета клубочка обозначают в процентах долю Э и НЭ в воде (HjO) ультрафильтрата и реабсорбцию этих веществ (цифры у обозначений Э и НЭ в корковом веществе). Цифры в просвете канальца и вне нефрона без специальных буквенных обозначений указывают на осмоляльность жидкости в соответствующем месте почки.
цессе осмотического концентрирования мочи в почке принимают участие все отделы канальцев, сосуды мозгового вещества, интерстициальная ткань, которые функционируют как поворотно-противоточная множительная система. Из 100 мл фильтрата, образовавшегося в клубочках, около 60—70 мл реабсорбируется к концу проксимального сегмента. Концентрация осмотически активных веществ в оставшейся в канальцах жидкости такая же, как и в ультрафильтрате плазмы крови, хотя состав жидкости отличается от состава ультрафильтрата вследствие реабсорбции ряда веществ вместе с водой в проксимальном канальце (рис. 11.6). Далее канальцевая жидкость переходит из коркового вещества почки в мозговое, перемещаясь по петле нефрона до вершины мозгового вещества (где каналец изгибается на 180°), переходит в восходящий отдел петли и движется в направлении от мозгового к корковому веществу почки.
Функциональное значение различных отделов петли нефрона неоднозначно. Поступающая из проксимального канальца в тонкий нисходящий отдел петли нефрона жидкость попадает в зону почки, в интерстициальной ткани которой концентрация осмотически активных веществ выше, чем в корковом веществе почки. Это повышение осмоляльной концентрации в наружной зоне мозгового вещества обусловлено деятельностью толстого восходящего отдела петли нефрона. Его стенка непроницаема для воды, а клетки транспортируют Cl~, Na+ в интерстициальную ткань. Стенка нисходящего отдела петли проницаема для воды. Вода всасывается из просвета канальца в окружающую интерстициальную ткань по осмотическому градиенту, а осмотически активные вещества остаются в просвете канальца. Концентрация осмотически активных веществ в жидкости, поступающей из восходящего отдела петли в начальные отделы дистального извитого канальца, составляет уже около 200 мосмоль/кг Н2О, т. е. она ниже, чем в ультрафильтрате. Поступление С1" и Na+ в интерстициальную ткань мозгового вещества увеличивает концентрацию осмотически активных веществ (осмоляльная концентрация) межклеточной жидкости в этой зоне почки. На такую же величину растет и осмоляльная концентрация жидкости, находящейся в просвете нисходящего отдела петли. Это обусловлено тем, что через водопроницаемую стенку нисходящего отдела петли нефрона в интерстициальную ткань по осмотическому градиенту переходит вода, в то же время осмотически активные вещества остаются в просвете этого канальца.
Чем дальше от коркового вещества по длиннику почечного сосочка находится жидкость в нисходящем колене петли, тем выше ее осмоляльная концентрация. Таким образом, в каждых соседних участках нисходящего отдела петли имеется лишь небольшое нарастание осмотического давления, но вдоль мозгового вещества почки осмоляльная концентрация жидкости в просвете канальца и в интерстициальной ткани постепенно растет от 300 до 1450 мосмоль/кг ЩО.
На вершине мозгового вещества почки осмоляльная концентрация жидкости в петле нефрона возрастает в несколько раз, а ее объем уменьшается. При дальнейшем движении жидкости по восходящему отделу петли нефрона, особенно в толстом восходящем отделе петли, продолжается реабсорбция С1~ и Na+, вода же остается в просвете канальца. В начальные отделы дистального извитого канальца всегда — и при водном диурезе, и при антидиурезе — поступает гипотоническая жидкость, концентрация осмотически активных веществ в которой менее 200 мосмоль/кг Н2О.
При уменьшении мочеотделения (антидиурез), вызванном инъекцией АДГ или секрецией АДГ нейрогипофизом при дефиците воды в организме, увеличивается проницаемость стенки конечных частей дистального сегмента (связующий каналец) и собирательных трубок для воды. Из гипотонической жидкости, находящейся в связующем канальце и собирательной трубке коркового вещества почки, вода реабсорбируется по осмотическому градиенту, осмоляльная концентрация жидкости в этом отделе увеличивается до 300 мосмоль/кг Н2О, т. е. становится изоосмотичной крови в системном кровотоке и межклеточной жидкости коркового вещества почки. Концентрирование мочи продолжается в собирательных трубках; они проходят параллельно канальцам петли нефрона через мозговое вещество почки. Как отмечалось выше, в мозговом веществе почки постепенно возрастает осмоляльная концентрация жидкости и из мочи, находящейся в собирательных трубках, реабсорбируется вода; концентрация осмотически активных веществ в жидкости просвета канальца выравнивается с таковой в интерстициальной жидкости на вершине мозгового вещества. В условиях дефицита воды в организме усиливается секреция АДГ, что увеличивает проницаемость стенок конечных частей дистального сегмента и собирательных трубок для воды.
В отличие от наружной зоны мозгового вещества почки, где повышение осмолярной концентрации основано главным образом на транспорте Na+ и С1~, во внутреннем мозговом веществе почки это повышение обусловлено участием ряда веществ, среди которых важнейшее значение имеет мочевина — для нее стенки проксимального канальца проницаемы. В проксимальном канальце реабсорбируется до 50 % профильтровавшейся мочевины, однако в начале дистального канальца количество мочевины несколько больше, чем количество мочевины, поступившей с фильтратом. Оказалось, что имеется система внутрипочечного кругооборота мочевины, которая участвует в осмотическом концентрировании мочи. При антидиурезе АДГ увеличивает проницаемость собирательных трубок мозгового вещества почки не только для воды, но и для мочевины. В просвете собирательных трубок вследствие реабсорбции воды повышается концентрация мочевины. Когда проницаемость канальцевой стенки для мочевины увеличивается, она диффундирует в мозговое вещество почки. Мочевина проникает в просвет прямого сосуда и тонкого отдела петли нефрона. Поднимаясь по направлению к корковому веществу почки по прямому сосуду, мочевина непрерывно участвует в противоточном обмене, диффундирует в нисходящий отдел прямого сосуда и нисходящую часть петли нефрона. Постоянное поступление во внутреннее мозговое вещество мочевины, Na+ и С1", реабсорбируемых клетками тонкого восходящего отдела петли нефрона и собирательных трубок, удержание этих веществ благодаря деятельности противоточной системы прямых сосудов и петель нефрона обеспечивают повышение концентрации осмотически активных веществ во внеклеточной жидкости во внутреннем мозговом веществе почки. Вслед за увеличением осмоляльной концентрации окружающей собирательную трубку интерстициальной жидкости возрастает реабсорбция воды из нее и повышается эффективность осморегулирующей функции почки. Эти данные об изменении проницаемости канальцевой стенки для мочевины позволяют понять, почему очищение от мочевины уменьшается при снижении мочеотделения.
Прямые сосуды мозгового вещества почки, подобно канальцам петли нефрона, образуют противоточную систему. Благодаря такому расположению прямых сосудов обеспечивается эффективное кровоснабжение мозгового вещества почки, но не происходит вымывания из крови осмотически активных веществ, поскольку при прохождении крови по прямым сосудам наблюдаются такие же изменения ее осмотической концентрации, как и в тонком нисходящем отделе петли нефрона. При движении крови по направлению к вершине мозгового вещества концентрация осмотически активных веществ в ней постепенно возрастает, а во время обратного движения крови к корковому веществу соли и другие вещества, диффундирующие через сосудистую стенку, переходят в интерстициальную ткань. Тем самым сохраняется градиент концентрации осмотически активных веществ внутри почки и прямые сосуды функционируют как противоточная система. Скорость движения крови по прямым сосудам определяет количество удаляемых из мозгового вещества солей и мочевины и отток реабсорбируемой воды.
В случае водного диуреза функции почек отличаются от описанной ранее картины. Проксимальная реабсорбция не изменяется, в дистальный сегмент нефрона поступает такое же количество жидкости, как и при антидиурезе. Осмоляльность мозгового вещества почки при водном диурезе в 3 раза меньше, чем на максимуме антидиуреза, а осмотическая концентрация жидкости, поступающей в дистальный сегмент нефрона, такая же — приблизительно 200 мосмоль/кг HjO. При водном диурезе стенка конечных отделов почечных канальцев остается водопроницаемой, а из протекающей мочи клетки продолжают реабсорбировать Na+. В итоге выделяется
гипотоническая моча, концентрация осмотически активных веществ в которой может снижаться до 50 мосмоль/кг HjO. Проницаемость канальцев для мочевины низкая, поэтому мочевина экскретируется с мочой, не накапливаясь в мозговом веществе почки.
Таким образом, деятельность петли нефрона, конечных частей дистального сегмента и собирательных трубок обеспечивает способность почек вырабатывать большие объему разведенной (гипотоническая) мочи — до 900 мл/ч, а при дефиците воды экскретировать всего 10—12 мл/ч мочи, в
4,5 раза более осмотически концентрированной, чем кровь. Способность почки осмотически концентрировать мочу исключительно развита у некоторых пустынных грызунов, что позволяет им длительное время обходиться без воды.
11.2.7. Гомеостатические функции почек
Для поддержания почками постоянства объема и состава внутренней среды, и прежде всего крови, существуют специальные системы рефлекторной регуляции, включающие специфические рецепторы, афферентные пути и нервные центры, где происходит переработка информации. Команды к почке поступают по эфферентным нервам или гуморальным путем.
В целом перестройка работы почки, ее приспособление к непрестанно изменяющимся условиям определяются преимущественно влиянием на гломерулярный и канальцевый аппарат аргинин-вазопрессина [антидиуре- тический гормон (АДГ)], альдостерона, паратирина и ряда других гормонов.
Роль почек в осмо- и волюморегуляции. Почки являются основным органом осморегуляции. Они обеспечивают выделение избытка воды из организма в виде гипотонической мочи при увеличенном содержании воды (гипергидратация) или экономят воду и экскретируют мочу, гипертоническую по отношению к крови, при обезвоживании организма (дегидратация).
После питья воды или при ее избытке в организме снижается концентрация растворенных осмотически активных веществ в крови и падает ее осмоляльность. Это уменьшает активность центральных осморецепторов, расположенных в области супраоптического ядра гипоталамуса, а также периферических осморецепторов, имеющихся в печени, почке и других органах, что приводит к снижению секреции АДГ нейрогипофизом и увеличению выделения воды почкой. Центральные осморецепторы открыл английский физиолог Верней, а представление об осморегулирующем рефлексе и периферических осморецепторах разработал А. Г Гинецинский.
При обезвоживании организма или введении в сосудистое русло гипертонического раствора NaCl увеличивается концентрация осмотически активных веществ в плазме крови, возбуждаются осморецепторы, усиливается секреция АДГ, возрастает всасывание воды в канальцах, уменьшается мочеотделение и выделяется осмотически концентрированная моча (схема 11.1). В эксперименте было показано, что, помимо осморецепторов, секрецию АДГ стимулируют натрийрецепторы. При введении в область III желудочка мозга гипертонического раствора NaCl наблюдался антидиурез, если же вводить в то же место гипертонический раствор сахарозы, то мочеотделение не уменьшается.
Осморецепторы высокочувствительны к сдвигам концентрации осмотически активных веществ в плазме крови. При увеличении концентрации в 512
Схема 11.1. Регуляция водо- и электролитовыделительной функции почки
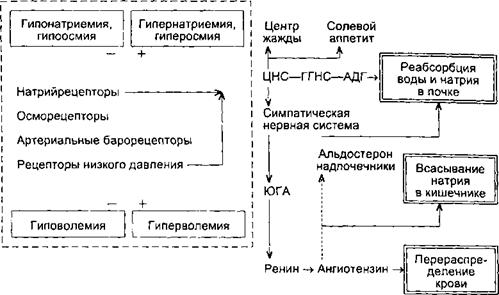
плазме осмотически активных веществ на 1 % (около 3 мосмоль/кг HjO) концентрация аргинин-вазопрессина в плазме крови у человека возрастает на 1 пг/мл[II] Повышение концентрации осмотически активных веществ в плазме на 1 мосмоль/кг ЩО вызывает благодаря выделению АДГ увеличение осмотической концентрации мочи почти на 100 мосмоль/кг HjO, а переход от состояния водного диуреза до максимального осмотического концентрирования мочи требует десятикратного возрастания активности АДГ в крови — с 0,5 до 5 пг/мл.
Помимо осмо- и натрийрецепторов, уровень секреции АДГ определяет активность волюморецепторов, воспринимающих изменение объема внутрисосудистой и внеклеточной жидкости. Ведущее значение в регуляции секреции АДГ имеют рецепторы, которые реагируют на изменение напряжения сосудистой стенки в области низкого давления. Прежде всего это рецепторы левого предсердия, импульсы от которых передаются в ЦНС по афферентным волокнам блуждающего нерва. При увеличении кровенаполнения левого предсердия активируются волюморецепторы и угнетается секреция АДГ, что вызывает усиление мочеотделения. Поскольку активация волюморецепторов в отличие от осморецепторов обусловлена увеличением объема жидкости, т. е. возросшим содержанием в организме воды и солей натрия, возбуждение волюморецепторов приводит к увеличению экскреции почкой не только воды, но и натрия. Эти процессы связаны с секрецией натрийуретического гормона, уменьшением секреции ренина, ангиотензина, альдостерона, при этом снижается тонус симпатической нервной системы, в результате уменьшается реабсорбция натрия и возрастают натрийурез и мочеотделение. В конечном счете восстанавливается объем крови и внеклеточной жидкости.
Роль почек в регуляции ионного состава крови. Почки являются эффекторным органом системы ионного гомеостаза. В организме существуют системы регуляции баланса каждого из ионов. Для некоторых ионов уже описаны специфические рецепторы, например натрийрецепторы. Рефлекторная регуляция транспорта ионов в почечных канальцах осуществляется как периферическими, так и центральными нервными механизмами.
Регуляция реабсорбции и секреции ионов в почечных канальцах осуществляется несколькими гормонами. Реабсорбция натрия возрастает в конечных частях дистального сегмента нефрона и собирательных трубках пбд влиянием гормона коркового вещества надпочечника альдостерона. Этот гормон выделяется в кровь при уменьшении концентрации натрия в плазме крови и уменьшении объема циркулирующей крови. В усилении выделения натрия почкой участвует натрийуретический гормон, одним из мест образования которого являются предсердия. При увеличении объема циркулирующей крови, повышении объема внеклеточной жидкости в организме усиливается секреция в кровь этого пептидного гормона.
Секрецию калия в дистальном сегменте и собирательных трубках усиливает альдостерон. Инсулин уменьшает выделение калия Алкалоз сопровождается усилением выделения калия, а при ацидозе калийурез уменьшается.
При уменьшении концентрации кальция в крови паращитовидные железы выделяют паратгормон, который способствует нормализации уровня кальция в крови, в частности благодаря увеличению его реабсорбции в почечных канальцах и высвобождению из кости. При гиперкальциемии, а также под влиянием гастрина (или подобного ему вещества), вырабатываемого в пищеварительном тракте в процессе всасывания кальция, стимулируется выделение в кровь парафолликулярными клетками щитовидной железы кальцитонина, который способствует уменьшению концентрации Са2+ в плазме крови благодаря увеличению экскреции этого иона почкой и переходу Са2+ в кость. В регуляции обмена Са2+ участвуют образующиеся в почке активные формы витамина D3, в частности 1,25(ОН)г-холекаль- циферол. В почечных канальцах регулируется уровень реабсорбции Mg2+ Cl-, SO^-, а также микроэлементов.
Роль почек в регуляции кислотно-основного состояния. Почки участвуют в поддержании постоянства концентрации Н+ в крови, экскретируя кислые продукты обмена. Активная реакция мочи у человека и животных может очень резко меняться в зависимости от состояния кислотно-основного состояния организма. Концентрация Н+ при ацидозе и алкалозе различается почти в 1000 раз, при ацидозе pH может снижаться до 4,5, при алкалозе — превышать 8,0. Это способствует участию почек в стабилизации pH плазмы крови на уровне 7,36. Механизм подкисления мочи основан на секреции клетками канальцев Н+ В апикальной плазматической мембране и цитоплазме клеток различных отделов нефрона находится фермент карбоангидраза (КА), катализирующий реакцию гидратации COj:
СО2 + Н2О о Н2СО3 о Н+ + HCOJ.
Секреция Н+ создает условия для реабсорбции вместе с гидрокарбонатом эквивалентного количества Na+ Наряду с натрий-калиевым насосом и электрогенным натриевым насосом, обусловливающим перенос Na+ с СГ, реабсорбция Na+ с гидрокарбонатом играет важную роль в поддержании натриевого баланса. Фильтрующийся из плазмы крови гидрокарбонат соединяется с секретированным клеткой Н+ и в просвете канальца пре
вращается в Н2СО3. Образование Н+ происходит следующим образом Внутри клетки вследствие гидратации СО2 образуется Н2СО3 и диссоциирует на Н+ и НСО3. В просвет канальца секретируется Н+, протоны связываются не только с НСОз, но и с такими соединениями, как двузамещенный фосфат (Na2HPO4), и некоторыми другими, в результате чего увеличивается экскреция титруемых кислот (ТА-) с мочой. Это способствует выделению кислот и восстановлению резерва оснований в плазме крови. Наконец, секретируемый Н+ может связываться в просвете канальца с NH3, образующимся в клетке при дезаминировании глутамина и ряда аминокислот и диффундирующим через мембрану в просвет канальца, в котором образуется ион аммония: NH3 + Н+ -> NH^ Этот процесс способствует сбережению в организме Na* и К+, которые реабсорбируются в канальцах. Таким образом, общая экскреция кислот почкой складывается из трех компонентов — титруемых кислот, аммония и гидрокарбоната.
При питании мясом образуется большое количество кислот и моча становится кислой, а при потреблении растительной пищи pH сдвигается в основную сторону. При интенсивной физической работе из мышц в кровь поступает значительное количество молочной и фосфорной кислот и почки увеличивают выделение «кислых» продуктов с мочой.
11.2.8. Экскреторная функция почек
Почки играют ведущую роль в выделении из крови нелетучих конечных продуктов обмена и чужеродных веществ, попавших во внутреннюю среду организма. В процессе метаболизма белков и нуклеиновых кислот образуются различные продукты азотистого обмена (у человека — мочевина, мочевая кислота, креатинин и др.). Катаболизм пуриновых оснований в организме человека останавливается на уровне образования мочевой кислоты, в клетках некоторых животных имеются ферменты, обеспечивающие распад пуриновых оснований до СО2 и аммиака. Мочевая кислота в почке человека фильтруется в клубочках, затем реабсорбируется в канальцах, часть мочевой кислоты секретируется клетками в просвет нефрона. Обычно экскретируемая фракция мочевой кислоты довольно низкая (9,8 %), что указывает на реабсорбцию значительного количества мочевой кислоты в канальцах. Интерес к изучению механизмов транспорта мочевой кислоты в почечных канальцах обусловлен резко возросшей частотой заболевания подагрой, при которой нарушен обмен мочевой кислоты.
Образующийся в течение суток креатинин, источником которого служит креатинфосфорная кислота, выделяется почками. Его суточная экскреция зависит не столько от потребления мяса с пищей, сколько от массы мышц тела. Креатинин, как и мочевина, свободно фильтруется в почечных клубочках, с мочой выводится весь профильтровавшийся креатинин, в то время как мочевина частично реабсорбируется в канальцах.
Помимо перечисленных, имеется много разнообразных веществ, постоянно удаляемых почкой из крови. О том, какие вещества удаляет или разрушает почка, можно судить при изучении состава крови у людей с удаленными почками. В их крови, помимо мочевины, креатинина, мочевой кислоты, накапливаются гормоны (глюкагон, паратирин, гастрин), ферменты (рибонуклеаза, ренин), производные индола, глюкуроновая кислота и др.
Существенно, что физиологически ценные вещества при их избытке в крови начинают экскретироваться почкой. Это относится как к неоргани-
ческим веществам, о которых шла речь выше при описании осмо-, волю- мо- и ионорегулирующей функции почек, так и к органическим веществам — глюкозе, аминокислотам. Повышенная экскреция этих веществ может в условиях патологии наблюдаться и при нормальной концентрации в крови, когда нарушена работа клеток, реабсорбирующих то или иное профильтровавшееся вещество из канальцевой жидкости в кровь.
11.2.9. Инкреторная функция почек
В почках вырабатывается несколько биологически активных веществ, позволяющих рассматривать ее как инкреторный орган. Гранулярные клетки юкстагломерулярного аппарата выделяют в кровь ренин при уменьшении АД в почке, снижении содержания натрия в организме, при переходе человека из горизонтального положения в вертикальное. Уровень выброса ренина из клеток в кровь изменяется и в зависимости от концентрации Na+ и С1_ в области плотного пятна дистального канальца, обеспечивая регуляцию электролитного и клубочково-канальцевого баланса. Ренин синтезируется в гранулярных клетках афферентной артериолы юкстагломерулярного аппарата и представляет собой протеолитический фермент. В плазме крови он отщепляет от ангиотензиногена, находящегося главным образом во фракции аз-глобулина, физиологически неактивный пептид, состоящий из 10 аминокислот, — ангиотензин I. В плазме крови под влиянием ангиотензинпревращающего фермента от ангиотензина I отщепляются 2 аминокислоты и он превращается в активное сосудосуживающее вещество ангиотензин II. Он повышает АД благодаря сужению артериальных сосудов, усиливает секрецию альдостерона, увеличивает чувство жажды, регулирует реабсорбцию натрия в дистальных отделах канальцев и собирательных трубках. Все перечисленные эффекты способствуют нормализации объема крови и АД.
В почке синтезируется активатор плазминогена — урокиназа. В мозговом веществе почки и клубочках образуются простагландины. Они участвуют, в частности, в регуляции почечного и общего кровотока, увеличивают выделение натрия с мочой, уменьшают чувствительность клеток канальцев к АДГ Клетки почки извлекают из плазмы крови образующийся в печени прогормон — витамин D3 и превращают его в физиологически активный гормон — активные формы витамина D3. Этот стероид стимулирует образование кальцийсвязывающего белка в кишечнике, способствует освобождению кальция из костей, регулирует его реабсорбцию в почечных канальцах. Почка является местом продукции эритропоэтина, стимулирующего эритропоэз в костном мозге. В почке вырабатывается брадикинин, являющийся сильным вазодилататором.
11.2.10. Метаболическая функция почек
Почки участвуют в обмене белков, липидов и углеводов. Не следует смешивать понятия «метаболизм почек», т. е. процесс обмена веществ в их паренхиме, благодаря которому осуществляются все формы деятельности почек, и «метаболическая функция почек». Данная функция обусловлена участием почек в обеспечении постоянства концентрации в крови ряда физиологически значимых органических веществ. В почечных клубочках фильтруются измененные белки, низкомолекулярные белки, пептиды. 516
Клетки проксимального отдела нефрона расщепляют их до аминокислот или дипептидов и транспортируют через базальную плазматическую мембрану в кровь. Это способствует восстановлению в организме фонда аминокислот, что важно при дефиците белков в рационе. При заболеваниях почек эта функция может нарушаться. Почки способны синтезировать глюкозу (глюконеогенез) При длительном голодании почки могут синтезировать до 50 % от общего количества глюкозы, образующейся в организме и поступающей в кровь. Почки являются местом синтеза фосфатидилинози- та — необходимого компонента плазматических мембран. Для энерготрат почки могут использовать глюкозу или свободные жирные кислоты. При низком уровне глюкозы в крови клетки почки в большей степени расходуют жирные кислоты, при гипергликемии преимущественно расщепляется глюкоза. Значение почек в липидном обмене состоит в том, что свободные жирные кислоты могут в клетках почек включаться в состав триацилгли- церина и фосфолипидов и в виде этих соединений поступать в кровь.
11.2.11. Принципы регуляции реабсорбции и секреции веществ в клетках почечных канальцев
Почки способны в широком диапазоне изменять интенсивность транспорта различных веществ- воды, электролитов и неэлектролитов. Это является непременным условием выполнения почкой ее основного назначения — стабилизации основных физических и химических показателей жидкостей внутренней среды. Широкий диапазон изменения скорости реабсорбции каждого из профильтровавшихся в просвет канальца веществ, необходимых для организма, требует существования соответствующих механизмов регуляции функций клеток. Действие гормонов и медиаторов, влияющих на транспорт ионов и воды, состоит в изменении функций (или числа) ионных или водных каналов, переносчиков, ионных насосов. Известно несколько вариантов биохимических механизмов, с помощью которых гормоны и медиаторы регулируют транспорт веществ клеткой нефрона. В одном случае происходит активирование генома и усиливается синтез специфических белков, ответственных за реализацию гормонального эффекта, в другом — изменение проницаемости и работы насосов происходит без непосредственного участия генома.
Сравнение особенностей действия альдостерона и вазопрессина позволяет раскрыть сущность обоих вариантов регуляторных влияний. Альдостерон увеличивает реабсорбцию Na+ в клетках почечных канальцев. Из внеклеточной жидкости альдостерон проникает через базальную плазматическую мембрану в цитоплазму клетки, соединяется с рецептором, и образовавшийся комплекс поступает в ядро (рис. 11.7). В ядре стимулируется ДНК-зависимый синтез тРНК и активируется образование белков, необходимых для увеличения транспорта Na+ Альдостерон стимулирует синтез компонентов натриевого насоса (Na+—К+-АТФазы), ферментов цикла трикарбоновых кислот и натриевых каналов, по которым Na+ входит в клетку через апикальную мембрану из просвета канальца. В обычных, физиологических условиях одним из факторов, ограничивающих реабсорбцию Na+, является проницаемость для Na+ апикальной плазматической мембраны. Возрастание числа натриевых каналов или времени их открытого состояния увеличивает вход Na+ в клетку, повышает содержание Na+ в ее цитоплазме и стимулирует активный перенос Na+ и клеточное дыхание.
 | |||||||||||
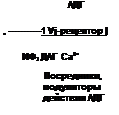 | |||||||||||
 | |||||||||||
 | |||||||||||
 | |||||||||||
 | |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
 | |||
 | |||
|
|
 | |||
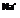 | |||
Рис. 11.7. Механизм действия альдостерона и вазопрессина на реабсорбцию натрия и воды. Объяснение в тексте.
Увеличение секреции К+ под влиянием альдостерона обусловлено возрастанием калиевой проницаемости апикальной мембраны и транспорта К+ из клетки в просвет канальца. Усиление синтеза Na+—К+-АТФазы при действии альдостерона обеспечивает усиленное поступление К+ в клетку из внеклеточной жидкости и благоприятствует секреции К+
Другой вариант механизма клеточного действия гормонов рассмотрим на примере АДГ (вазопрессин). Он взаимодействует со стороны внеклеточной жидкости с У2-рецептором, локализованным в базальной плазматической мембране клеток конечных частей дистального сегмента и собирательных трубок. При участии G-белков происходит активация фермента аденилатциклазы и из АТФ образуется 3’,5’-АМФ (цАМФ), который стимулирует протеинкиназу А и встраивание водных каналов (аквапорины) в апикальную мембрану. Это приводит к увеличению проницаемости для воды. В дальнейшем цАМФ разрушается фосфодиэстеразой и превращается в 5’-АМФ
11.2.12. Регуляция деятельности почек
Почка служит исполнительным органом в цепи различных рефлексов, обеспечивающих постоянство состава и объема жидкостей внутренней среды. В ЦНС поступает информация о состоянии внутренней среды, происходит интеграция сигналов и обеспечивается регуляция деятельности почек при участии эфферентных нервов или эндокринных желез, гормоны которых регулируют процесс мочеобразования. Работа почки, как и других органов, подчинена не только безусловнорефлекторному контролю, но и регулируется корой большого мозга, т. е. мочеобразование может меняться условнорефлекторным путем. Анурия, наступающая при болевом раздражении, может быть воспроизведена условнорефлекторным путем. Механизм болевой анурии основан на раздражении гипоталамических центров, стимулирующих секрецию вазопрессина нейрогипофизом. Наря- 518
ду с этим усиливаются активность симпатической части автономной нервной системы и секреция катехоламинов надпочечниками, что и вызывает резкое уменьшение мочеотделения вследствие снижения клубочковой фильтрации и увеличения канальцевой реабсорбции воды.
Не только уменьшение, но и увеличение диуреза может быть вызвано условнорефлекторным путем. Многократное введение воды в организм собаки в сочетании с действием условного раздражителя приводит к образованию условного рефлекса, сопровождающегося увеличением мочеотделения. Механизм условнорефлекторной полиурии в данном случае основан на том, что из коры большого мозга импульсы поступают в гипоталамус и уменьшается секреция АДГ Импульсы, поступающие по эфферентным нервам почки, регулируют гемодинамику и работу юкстагломерулярного аппарата почки, оказывают прямое влияние на реабсорбцию и секрецию ряда неэлектролитов и электролитов в канальцах. Импульсы, поступающие по адренергическим волокнам, стимулируют транспорт натрия, а по холинергическим — активируют реабсорбцию глюкозы и секрецию органических кислот. Механизм изменения мочеобразования при участии адренергических нервов обусловлен активацией аденилатциклазы и образованием цАМФ в клетках канальцев. Катехоламинчувствительная аденилатциклаза имеется в базолатеральных мембранах клеток дистальных извитых канальцев и начальных отделов собирательных трубок. Афферентные нервы почки играют существенную роль как информационное звено системы ионной регуляции, обеспечивают осуществление рено-ренальных рефлексов
11.2.13. Количество, состав и свойства мочи
Диурезом называют количество мочи, выделяемое человеком за определенное время. Эта величина у здорового человека колеблется в широких пределах в зависимости от состояния водного обмена. При обычном водном режиме за сутки выделяется 1—1,5 л мочи. Концентрация осмотически активных веществ в моче зависит от состояния водного обмена и составляет 50—1450 мосмоль/кг Н2О. После потребления значительного количества воды и при функциональной пробе с водной нагрузкой (испытуемый выпивает воду в объеме 20 мл на 1 кг массы тела) скорость мочеотделения достигает 15—20 мл/мин. В условиях высокой температуры окружающей среды вследствие возрастания потоотделения количество выделяемой мочи уменьшается. Ночью во время сна диурез меньше, чем днем.
Состав и свойства мочи. С мочой могут выделяться большинство веществ, имеющихся в плазме крови, а также некоторые соединения, синтезируемые в почке. С мочой выделяются электролиты, количество которых зависит от их потребления с пищей, а концентрация в моче — от уровня мочеотделения. Суточная экскреция Na+ составляет 40—220 ммоль, К+ — 25-125, СГ - 110-250, Са2+ - 1-4, Mg2+ - 1-5, SO2’ - 15-30 ммоль.
Почки служат главным органом экскреции конечных продуктов азотистого обмена. У человека при распаде белков образуется мочевина, составляющая до 90 % азота мочи; ее суточная экскреция достигает 25—35 г. С мочой выделяется 0,4—1,2 г азота аммиака, 0,2—0,7 г мочевой кислоты (при потреблении пищи, богатой пуринами, выделение возрастает до 2— 3 г). Креатин, образующийся в мышцах из фосфокреатина, переходит в креатинин; его выделяется около 1,5 г/сут. В небольшом количестве в мочу поступают некоторые производные продуктов гниения белков в кишечнике — индол, скатол, фенол, они в основном обезвреживаются в
печени, где образуются парные соединения с серной кислотой — индоксилсерная, скатоксилсерная и другие кислоты. Белки в нормальной моче выявляются в очень небольшом количестве (суточная экскреция не превышает 125 мг). Небольшая протеинурия наблюдается у здоровых людей после тяжелой физической нагрузки и исчезает после отдыха.
Глюкоза в моче в обычных условиях не выявляется. При избыточном потреблении сахара, когда концентрация глюкозы в плазме крови превышает 10 ммоль/л, при гипергликемии иного происхождения наблюдается глюкозурия — выделение глюкозы с мочой.
Цвет мочи зависит от величины диуреза и уровня экскреции пигментов. Цвет меняется от светло-желтого до оранжевого. Пигменты образуются из билирубина желчи в кишечнике, где билирубин превращается в уробилин и урохром, которые частично всасываются в кишечнике и затем выделяются почками. Часть пигментов мочи представляет собой окисленные в почке продукты распада гемоглобина.
С мочой выделяются различные биологически активные вещества и продукты их превращения, по которым в известной степени можно судить о функции некоторых желез внутренней секреции. В моче обнаружены производные гормонов коркового вещества надпочечников, эстрогены, АДГ, витамины (аскорбиновая кислота, тиамин), ферменты (амилаза, липаза, трансаминаза и др.). При патологии в моче обнаруживаются вещества, обычно в ней не выявляемые, — ацетон, желчные кислоты, гемоглобин и др.
11.2.14. Мочеиспускание
Образующаяся в почечных канальцах моча выделяется в почечную чашечку, а затем в фазе систолы почечной чашечки происходит опорожнение в почечную лоханку. Последняя постепенно заполняется мочой, и по достижении порога раздражения возникают импульсы от барорецепторов, сокращаются мышцы почечной лоханки, раскрывается просвет мочеточника, и моча благодаря сокращениям его стенки продвигается в мочевой пузырь. Объем мочи в пузыре постепенно увеличивается, его стенка растягивается, но вначале напряжение стенок не изменяется и давление в мочевом пузыре не растет. Когда объем мочи в пузыре достигает определенного предела, круто нарастает напряжение гладкомышечных стенок и повышается давление жидкости в его полости. Раздражение механорецепторов мочевого пузыря определяется растяжением его стенок, а не увеличением давления. Если поместить мочевой пузырь в капсулу, которая препятствовала бы его растяжению, то повышение давления внутри пузыря не вызовет рефлекторных реакций. Существенное значение имеет скорость наполнения пузыря: при быстром растяжении мочевого пузыря резко увеличивается импульсация в афферентных волокнах тазового нерва. После опорожнения пузыря напряжение стенки уменьшается и быстро снижается импульсация.
В процессе мочеиспускания моча выводится из мочевого пузыря в результате рефлекторного акта. Наступают сокращение гладкой мышцы стенки мочевого пузыря, расслабление внутреннего и наружного сфинктеров мочеиспускательного канала, сокращение мышц брюшной стенки и дна таза; в это же время происходит фиксация грудной стенки и диафрагмы. В результате моча, находившаяся в мочевом пузыре, выводится из него.
При раздражении механорецепторов мочевого пузыря импульсы по центростремительным нервам поступают в крестцовые отделы спинного 520
мозга, во II — IV сегментах которого находится рефлекторный центр мочеиспускания. Первые позывы к мочеиспусканию появляются у человека, когда объем содержимого пузыря достигает 150 мл, усиленный поток импульсов наступает при увеличении объема до 200—300 мл. Спинальный центр мочеиспускания находится под влиянием вышележащих отделов мозга, изменяющих порог возбуждения рефлекса мочеиспускания. Тормозящие влияния на этот рефлекс исходят из коры большого мозга и среднего мозга, возбуждающие — из заднего гипоталамуса и переднего отдела моста мозга.
Возбуждение центра мочеиспускания вызывает импульсацию в парасимпатических волокнах тазовых внутренностных нервов, при этом стимулируется сокращение мышцы мочевого пузыря, давление в нем возрастает до 20—60 см вод. ст., расслабляется внутренний сфинктер мочеиспускательного канала. Поток импульсов к наружному сфинктеру мочеиспускательного канала уменьшается, его мышца — единственная исчерченная в мочевыводящих путях, иннервируемая соматическим нервом — ветвью полового нерва, расслабляется, и начинается мочеиспускание.
Раздражение рецепторов при растяжении стенки пузыря рефлекторно по эфферентным волокнам тазовых внутренностных нервов вызывает сокращение мышцы мочевого пузыря и расслабление его внутреннего сфинктера. Растяжение пузыря и продвижение мочи по мочеиспускательному каналу ведет к изменению импульсации в половом нерве, и наступает расслабление наружного сфинктера. Движение мочи по мочеиспускательному каналу играет важную роль в акте мочеиспускания, оно рефлекторно по афферентным волокнам полового нерва стимулирует сокращение мочевого пузыря. Поступление мочи в задние отделы мочеиспускательного канала и его растяжение способствуют сокращению мышцы мочевого пузыря. Передача афферентных и эфферентных импульсов этого рефлекса осуществляется по подчревному нерву.
11.2.15. Последствия удаления почки и искусственная почка
После удаления одной почки у человека и животных в течение нескольких недель увеличивается масса оставшейся почки, наступает ее компенсаторная гипертрофия. Клубочковая фильтрация возрастает в оставшейся почке почти в 1,5 раза по сравнению с исходным уровнем, увеличивается реабсорбционная и секреторная способность нефронов. Одна почка успешно обеспечивает стабильность состава внутренней среды. После удаления обеих почек или их выключения у человека в течение нескольких дней развивается уремия, в крови возрастает концентрация продуктов азотистого обмена, содержание мочевины может увеличиваться в 20—30 раз, нарушаются кислотно-основное состояние и ионный состав крови, развиваются слабость, расстройство дыхания, и через несколько дней наступает смерть.
Для временного замещения некоторых функций почек во время острой и хронической почечной недостаточности,'а также постоянно у больных с удаленными почками используется аппарат «искусственная почка». Он представляет собой диализатор, в котором через поры полупроницаемой мембраны кровь очищается от шлаков, в результате чего нормализуется ее состав. Сконструированы десятки различных типов аппаратов искусственной почки — спиральный, улиточный, пластинчатый. В этих аппаратах используют пленки, радиус пор в которых около 3 нм. Через эти поры проходят (как и в почечном клубочке) низкомолекулярные компоненты плазмы, но не проникают белки. По одну сторону пленки непрерывно протекает кровь пациента, поступающая из артерии и после прохождения через аппарат вливаемая в его вену, по другую сторону находится раствор для диализа. Он по ионному составу и осмотической концентрации подобен плазме крови. Больного подключают к аппарату искусственная почка обычно 2—3 раза в неделю. С помощью этого метода удается поддерживать жизнь больных более 25 лет. Один сеанс гемодиализа длится несколько часов. Важную роль в проведении регулярных гемодиализов сыграло использование артериовенозных шунтов, которые вживляют в лучевую артерию и вену предплечья, в результате чего исчезает необходимость хирургических операций перед каждым сеансом гемодиализа. В клинике гемодиализ иногда сочетают с гемосорбцией, что дает возможность дополнительно удалить из крови ряд веществ, которые должна была бы экскретировать почка.
11.2.16. Возрастные особенности структуры и функции почек
У человека к моменту рождения нефроны в основном сформированы. У новорожденного почечный плазмоток и гломерулярная фильтрация в несколько раз ниже, чем у взрослого человека. Эти показатели достигают уровня взрослого при расчете на стандартную величину площади поверхности тела к концу первого — началу второго года жизни. В клетках проксимальных канальцев у новорожденных резко снижена способность к секреции органических кислот, которая постепенно нарастает в течение первых нескольких месяцев жизни. В почках новорожденных недостаточно эффективно осуществляется осмотическое концентрирование мочи, слабо действует АДГ, что обусловлено незрелостью многих элементов почек. Определенную роль в низком осмотическом концентрировании мочи у детей первых месяцев жизни играют и высокая степень утилизации белков, и обусловленная этим низкая концентрация мочевины в крови и моче, а следовательно, и в мозговом веществе почки.
Основные процессы, обеспечивающие мочеобразование, достигают уровня взрослого человека к началу второго года жизни и сохраняются до 45—50 лет, после чего происходит медленное снижение почечного плазмотока, гломерулярной фильтрации, канальцевой секреции, осмотического концентрирования мочи. Отмечается параллельное уменьшение кровоснабжения нефронов и функциональной способности их клеток.
[I] Концентрация осмотически активных веществ; син.: осмотическая концентрация, осмоляльная концентрация, осмоляльность.
[II] 1 пг (пикограмм) = Ю-12 г.
Дата добавления: 2021-07-19; просмотров: 71; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!