Обратите внимание, что в данных реакциях водород не выделяется, потому что здесь окислителем выступает не водород, а сера.
Химические свойства разбавленной и концентрированной серной кислоты отличаются.
Так разбавленная серная кислота проявляет все характерные свойства кислот. Она изменяет окраску индикаторов: лакмус в растворе кислоты красный, метиловый оранжевый тоже.

Серная кислота вступает во взаимодействие с металлами, стоящими в ряду напряжений металлов до водорода.

Разбавленная серная кислота реагирует с основными и амфотэрными оксидами с образованием соли и воды. Если поместить в пробирку немного чёрного порошка оксида меди (II) и прилить немного раствора серной кислоты, а затем содержимое нагреть на пламени спиртовки, то постепенно чёрный порошок оксида меди (II) начинает растворяться, а раствор меняет свою окраску на голубую.
В результате данной реакции образуется соль – сульфат меди (II) и вода.
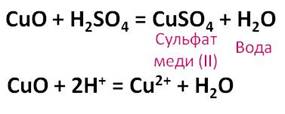
Разбавленная серная кислота вступает во взаимодействие с основаниями. Например, к раствору щёлочи добавим несколько капель фенолфталеина, раствор приобретает малиновую окраску. К этому раствору прильём разбавленную серную кислоту до исчезновения окраски. Таким образом, между щёлочью и кислотой прошла реакция нейтрализации, при этом образовалась соль – сульфат натрия и вода.

Разбавленная серная кислота реагирует не только с растворимыми основаниями – щелочами, но и с нерастворимыми. Получим нерастворимое основание – гидроксид меди (II). Для этого, в раствор медного купороса прильём щёлочи – гидроксид натрия, в результате чего образуется гидроксид меди (II) и соль – сульфат натрия.


Теперь, к этому осадку добавим раствор серной кислоты до его исчезновения. В результате данной реакции образуется соль – сульфат меди (II) и вода.


Кроме этого, разбавленная серная кислота реагирует с солями. Прильём к раствору сульфата калия раствор хлорида кальция. В результате образуется малорастворимое вещество белого цвета. Это сульфат кальция.

Концентрированная серная кислота также реагирует с металлами. Если металл стоит в ряду напряжений до водорода, то в результате реакции образуется газ сероводород и вода.
Например, в реакции с цинком образуется соль – сульфат цинка, газ – сероводород и вода. Цинк изменяет свою степень окисления с 0 до +2, а сера понижает с +6 до -2. Поэтому цинк выступает в роли восстановителя, а сера – в роли окислителя.
В реакции с металлами, стоящими после водорода образуется оксид серы (IV). Например, при взаимодействии меди с концентрированной серной кислотой, образуется соль – сульфат меди (II), оксид серы (IV) и вода. В этой реакции медь повышает свою степень окисления с 0 до +2, а сера понижает с +6 до +4. Поэтому медь восстановитель, а сера – окислитель.

Обратите внимание, что в данных реакциях водород не выделяется, потому что здесь окислителем выступает не водород, а сера.
Железо и алюминий пассивируются концентрированной серной кислотой, потому что покрываются защитной плёнкой, что позволяет перевозить её в стальных и алюминиевых цистернах.
Концентрированная серная кислота вытесняет кислоты из их солей. Например, если к твёрдому хлориду натрия добавить концентрированной серной кислоты, то образуется соль – гидросульфат натрия и хлороводород.


Серная кислота – это двухосновная кислота, поэтому она образует средние и кислые соли. Соли серной кислоты – сульфаты. Например, Na2SO4 – сульфат натрия, NaHSO4 – гидросульфат натрия.
Качественной реакцией на серную кислоту и её соли является ион бария. В результате взаимодействия сульфат-иона и иона бария образуется сульфат бария – осадок белого цвета.

Серная кислота находит широкое применение. Она используется при производстве взрывчатых веществ, минеральных удобрений, электролитической меди, моющих средств, эмалей и красок, искусственного шёлка, лекарств, пластмасс, при очистке нефтепрдуктов, в качестве электролита в аккумуляторах.


Среди солей серной кислоты наиболее распространена глауберова соль – Na2SO4 ∙ 10H2O, гипс – CaSO4 ∙ 2H2O, BaSO4 – сульфат бария и CuSO4 ∙ 5H2O – медный купорос, который используют для борьбы с вредителями и болезнями растений.
Дата добавления: 2020-12-22; просмотров: 67; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
