В случае равных моляльных концентраций наибольшее понижение температуры будет в растворе
Занятие № 3
Методические указания для студентов
ТЕМА: Растворы. Коллигативные свойства растворов.
ЦЕЛЬ: Изучить коллигативные свойства растворов и приобрести навыки криометрических измерений.
Теоретические вопросы:
1. Растворы, определение. Роль воды и растворов в жизнедеятельности. Физико-химические свойства воды, обуславливающие ее роль в качестве единственного биорастворителя. Строение воды, образование межмолекулярных водородных связей.
2. Концентрация растворов, способы ее выражения. Массовая доля, молярная концентрация, моляльная концентрация, молярная концентрация эквивалента, молярная доля и титр.
3. Зависимость растворимости вещества в воде от соотношения гидрофильных и гидрофобных свойств; влияние внешних условий на растворимость.
4. Понятие об идеальном растворе.
5. Закон Рауля и следствия из него: понижение температуры замерзания, повышение температуры кипения раствора.
6. Коллигативные свойства разбавленных растворов неэлектролитов.
7. Коллигативные свойства разбавленных растворов электролитов.
8. Осмос. Омотическое давление: закон Вант-Гоффа. Осмоляльность и осмолярность биологических жидкостей и перфузионных растворов.
9. Понятие о изоосмии. Роль осмоса в биологических системах. Плазмолиз, гемолиз.
10. Законы растворения газов в воде и биологических жидкостях.
Обучающие задачи:
1. Какой объем раствора серной кислоты с массовой долей 98 % (ρ = 1,81г/мл) необходимо взять для приготовления 500 мл раствора с молярной концентрацией кислоты 0,25 моль/л. (Кз=1,86 кг×К/моль)
|
|
|
Решение:

n (H2SO4) = C (H2SO4) × V (p-pa) = 0,25 моль/л×0,5л = 0,125моль
2. m (H2SO4) = n (H2SO4)×M (H2SO4)
M (H2SO4) = 2 + 32 + 64 = 98 г/моль
m (H2SO4) = 0,125моль×98 г/моль = 12,25 г

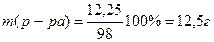

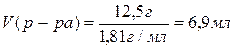
Ответ: V(р-ра) = 6,9 мл
2. Вычислите температуру замерзания раствора, содержащего 10г глюкозы в 180г воды (изотонический раствор).
Решение:
1. DTзам = K∙× b (C6H12O6)


Tзам раствора = Tзам. р-ля - DTзам.
Tзам. раствора = 273 - 0,57 = 272,430К или -0,570С
Ответ: -0,570С
3. Определите осмотическое давление при 370С в растворе с молярной концентрацией NaCl 0,16 моль/л. Будет ли этот раствор изотоничен плазме крови? Изотонический коэффициент NaCl равен 1,95.
Решение:
p = i×C (NaCl)∙×R×T R = 8,31 кПа×л/моль×К T = 273 + 37 = 310 K
p = 1,95 × 0,16моль/л × 8,31кПа×л/моль×К × 310К = 803,7 кПа
Осмотическое давление близко плазме крови, раствор изотоничен плазме крови.
Задачи для самостоятельного решения.
Упражнение 1. В каких системах можно наблюдать явление осмоса? Приведите примеры природных осмотических явлений.
Упражнение 2. Почему клубника, посыпанная сахаром, даёт сок?
|
|
|
Упражнение 3. Какую цель преследуют, посыпая снег на тротуаре солью?
Упражнение 4. Почему при аллергических реакциях, сопровождающихся отеками тканей, в организм вводят высококонцентрированные растворы хлорида кальция (10%) и глюкозы (20%) ?
Задача 1. Вычислить молярную, моляльную, моль-эквивалентную концентрации и молярную долю серной кислоты в 20% её растворе с плотностью 1,14 г/мл.
Ответ: С(Н2SO4)=2,33 моль/л; b(Н2SO4)=2,55моль/кг; С(1/2Н2SO4)=4,66 моль/л; χ(Н2SO4)=0,044
Задача 2. Этиловый спирт внутривенно иногда вводят при гангрене и абсцессе легкого в виде раствора с массовой долей 20%. Определите, будет ли при 370С данный раствор этилового спирта изотоничен плазме крови? Плотность раствора принять за 1 г/мл.
Ответ: 11200 кПа, раствор спирта –гипертонический.
Задача 3. Рассчитайте осмотическое давление при 310К водного раствора, содержащего в 0,1л дезоксирибозу массой 1,34г. Каким (гипо-, гипер- или изотоническим) является этот раствор по отношению к плазме крови?
Ответ: Посм= 258 кПа
Задача 4. Осмотическое давление плазмы крови равно 7,8×105Н/м2. Рассчитайте, сколько граммов хлорида натрия необходимо для приготовления 200мл раствора изотоничного плазме крови. Степень диссоциации хлорида натрия 95%.
|
|
|
Ответ:1,81г.
Задача 5. Опишите состояние эритроцитов при 310К в растворах сахарозы с массовой долей 8% (плотность 1,03 г/мл) и глюкозы с ω=2% (плотность 1,006 г/мл).
Ответ: гемолиз
Задача 6. Осмотическое давление крови в норме 780 кПа. Вычислите осмолярность крови при 310 К.
Ответ: Сосм = 0,303 осмоль/л
Задача 7. Рассчитайте кажущуюся степень электролитической диссоциации LiCl в растворе с молярной концентрацией эквивалента равной 0,1 моль/л, если раствор изотоничен с 0,19 моль/л раствором сахара С12Н22О11 при 00С.
Ответ: i = 1,89
Тестовые вопросы
1. Раствор, содержащий 4,6 г глицерина (М=92) в 100 г воды  , замерзает при темпратуре___ ° С
, замерзает при темпратуре___ ° С
1) -0,465 2) -0,372 3) 0,186 4) -0,93
2. Растворение твердых веществ в воде характеризуется:
1) DH<0, DS<0 3) DH<0, DS=0
2) DH<0, DS>0 4) DH=0, DS<0
Сольватирование частиц растворенного вещества является процессом ______
1) Эндотермическим 3) Экзотермическим
2) Физическим 4) Необратимым
Растворимость газов в жидкости повышается при___
1) понижении температуры 3) повышении температуры
2) понижении давления газа 4) введении в жидкость электролитов
|
|
|
Зависимость растворимости газа от концентрации электролита в растворе описывается законом____
1) Генри 3) Вант-Гоффа
2) Рауля 4) Сеченова
6. Осмотическое давление раствора глюкозы с молярной концентрацией 0,1 моль/л при 25 ° С равно _____ кПа.
1) 61,9 2) 51,6 3) 123,8 4) 247,6
7. Осмотическое давление раствора хлорида натрия с молярной концентрацией 0,1 моль/л (изотонический коэффициент 1,95) при 25 ° С равно _____ кПа.
1) 247,6 2) 482,9 3) 20,8 4) 40,5
8.Уравнение π=С RT является математическим выражением закона ___
1) Вант-Гоффа 3) Дальтона
2) Рауля 4) Сеченова
9. Осмолярная концентрация раствора глюкозы, если при температуре 25 ° С его осмотическое давление равно 247,6 кПа, составляет _____ моль/л.
1) 1,2 2) 0,12 3) 0,1 4) 12
Процесс перехода молекул растворителя через полупроницаемую мембрану из раствора с меньшей концентрацией в раствор с большей концентрацией называется___
1) электролитическая диссоциация 3) осмос
2) гидролиз 4) диффузия
11. Растворы хлорида натрия и глюкозы с одинаковой концентрацией имеют:
1) Одинаковое осмотической давление 3) Одинаковое давление пара над раствором
2) Разное осмотическое давление 4) Разный цвет
12. Водный раствор глюкозы с моляльной концентрацией 0,5 моль/кг замерзнет при температуре___ ° С. Криоскопическая постоянная воды равна 1,86.
1) – 0,93 2) 0,93 3) 0 4) – 3,72
13. Водный раствор глюкозы с моляльной концентрацией 1 моль/кг закипит при температуре ___ ° С. Эбулиоскопическая постоянная воды 0,516.
1) 0,516 2) 100,516 3) 273,516 4) 298,516
14. Растворы глицерина и глюкозы будут иметь одинаковое осмотическое давление при 25 ° С если у них ____.
1) Одинаковый объем 3) Разная концентрация
2) Одинаковая концентрация 4) Разный объем
В случае равных моляльных концентраций наибольшее понижение температуры будет в растворе
1) С6Н12О6 2) NaCl 3) KCl 4) CaCl2
Дата добавления: 2019-02-22; просмотров: 811; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
