Чем стабильнее анион, тем выше реакционная способность ацильного производного.
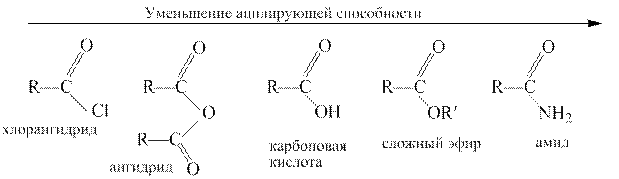
Наибольшей ацилирующей активностью обладают галогенангидриды и ангидриды, так как их ацильные остатки соединены с хорошо уходящими группами – галогенид-ионами и анионами карбоновых кислот. Сложные эфиры и амиды проявляют более низкую ацилирующую способность, потому что соответственно алкоксид- и амид-ионы не относятся к стабильным анионам и не являются хорошо уходящими группами. Такой подход к оценке ацилирующей способности показан ниже на примере сопоставления наиболее важных функциональных производных карбоновых кислот:
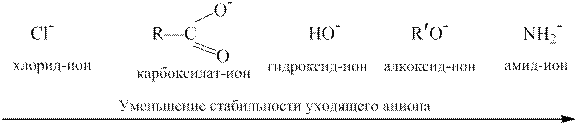
6.3. Галогенангидриды.
Галогенангидридами называются функциональные производные карбоновых кислот общей формулы RC ( O ) Hal .
Галогенангидриды представляют собой жидкости или твердые вещества с резким навязчивым запахом, сильно раздражают кожу и слизистые оболочки. Практическое значение имеют ацилхлориды и ацилбромиды.
Реакции ацилирования.
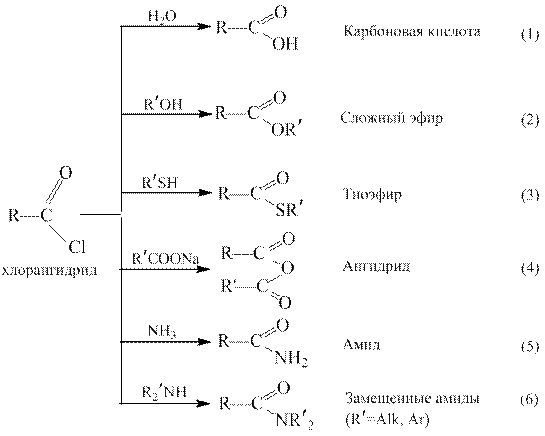
Галогенангидриды относятся к наиболее активным ацилирующим агентам, их используют для получения большинства других функциональных производных карбоновых кислот [реакции (2) – (6)].
Ацилгалогениды очень легко гидролизуются в карбоновые кислоты [реакция(1)], поэтому их хранят в условиях, исключающих доступ влаги воздуха.
С помощью галогенангидридов удается проацилировать такие соединения, которые не реагируют с другими ацилирующими агентами, например, третичные спирты и фенолы.
|
|
|
Восстановление.
Галогенангидриды восстанавливают комплексными гидридами металлов в первичные спирты:
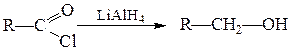
Гидрирование галогенангидридов на палладиевом катализаторе приводит к альдегидам:
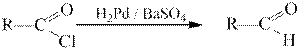
6.4. Ангидриды
Ангидридами называются функциональные производные карбоновых кислот общей формулы RC ( O ) OC ( O ) R /
Ангидриды можно рассматривать как продукты отщепления воды от карбоксильных групп двух молекул монокарбоновой кислоты или одной молекулы дикарбоновой кислоты. Существуют три основных типа ангидридов – симметричные, несимметричные, включающие остатки разных кислот, в том числе минеральных, и циклические ангидриды – производные дикарбоновых кислот:
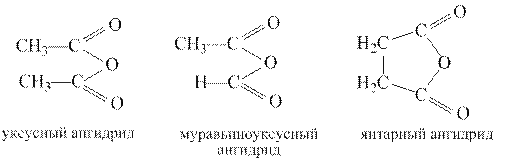
Ангидриды представляют собой жидкости или твердые вещества, низшие ангидриды имеют раздражающий запах, похожий на запах соответствующей кислоты.
Реакции ацилирования.
Реакции ацилирования протекают в условиях как кислотного, так и основного катализа или без катализатора. Ангидриды, как и галогенангидриды, способны ацилировать такие малоактивные нуклеофилы, как третичные и другие пространственно затрудненные спирты, алкилфенолы, низкоосновные ароматические амины.
|
|
|
Из симметричных ангидридов наибольшее значение имеет уксусный ангидрид.
Высокая ацилирующая способность ангидридов используется для получения большинства функциональных производных карбоновых кислот, как показано на примере уксусного ангидрида:
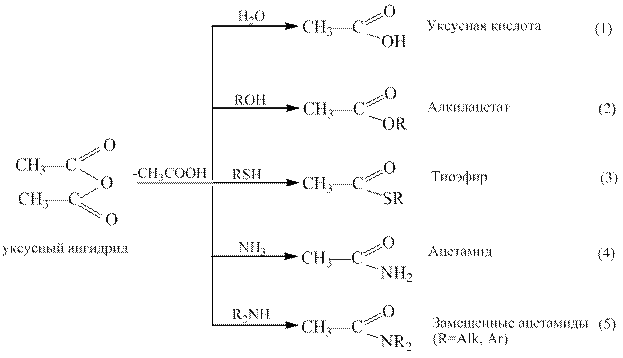
С помощью смешанных ангидридов в молекулу нуклеофила вводится остаток более слабой кислоты, потому что анион сильной кислоты является хорошо уходящей группой.
6.5. Сложные эфиры.
Сложными эфирами называются функциональные производные карбоновых кислот общей формулы RC ( O ) OR / .
Сложные эфиры низших спиртов и карбоновых кислот представляют собой летучие жидкости с приятным запахом, плохо растворимые в воде и хорошо – в большинстве органических растворителей. Запахи сложных эфиров напоминают запахи разных фруктов. Повышенную летучесть сложных эфиров используют в аналитических целях. Например, для масс-спектрометрического и газожидкостного хроматографического анализа низколетучие спирты и карбоновые кислоты переводят в более летучие сложные эфиры.
Гидролиз.
Важнейшей из реакций ацилирования является гидролиз сложных эфиров с образованием спирта и карбоновой кислоты:
|
|
|
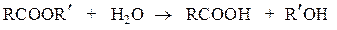
Реакция осуществляется как в кислой, так и в щелочной среде. Кислотно-катализируемый гидролиз сложных эфиров – реакция, обратная этерификации, протекает по тому же самому механизму, что и реакция этерификации:
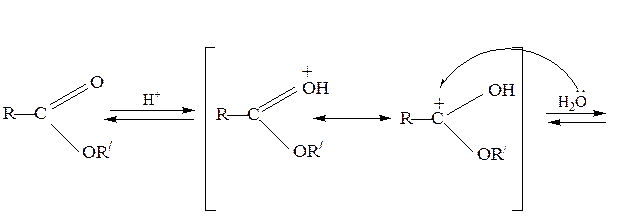
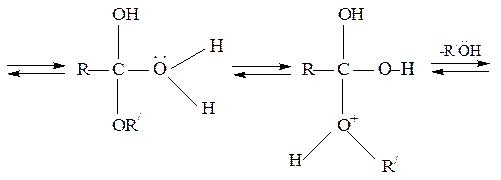
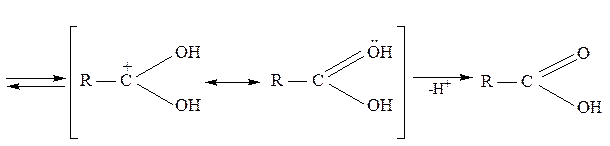
Нуклеофилом в этой реакции является вода. Смещение равновесия в сторону образования спирта и кислоты обеспечивается добавлением избытка воды.
Щелочной гидролиз необратим, в процессе реакции на моль эфира расходуется моль щелочи, т.е. щелочь в этой реакции выступает в качестве расходуемого реагента, а не катализатора:
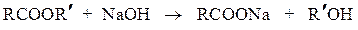
Гидролиз сложных эфиров в щелочной среде протекает по бимолекулярному ацильному механизму через стадию образования тетраэдрического интермедиата (I).
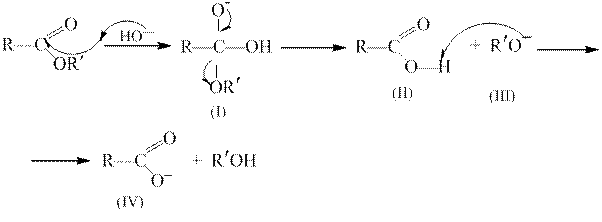
Необратимость щелочного гидролиза обеспечивается практически необратимым кислотно-основным взаимодействием карбоновой кислоты (II) и алкоксид-иона (III). Образовавшийся анион карбоновой кислоты (IV) сам является довольно сильным нуклеофилом и потому не подвергается нуклеофильной атаке.
Сложноэфирная конденсация.
|
|
|
При конденсации двух молекул сложного эфира в присутствии основного катализатора образуются эфиры β-оксокислот.
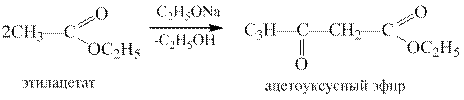
Эту реакцию рассматривают как нуклеофильное замещение у карбонильного атома углерода, т.е. как реакцию С-ацилирования.
Восстановление.
Сложные эфиры чаще восстанавливают в первичные спирты, реже в альдегиды или простые эфиры. Обычно для восстановления используют алюмогидрид лития:
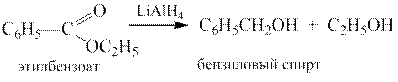
6.6. Амиды.
Амидами называются функциональные производные карбоновых кислот общей формулы R ─ C ( O )─ NH 2- n R ' n , где n =0-2.
В незамещенных амидах ацильный остаток соединен с незамещенной аминогруппой, а в N-замещенных амидах один из атомов водорода замещен одним алкильным или арильным радикалом, в N , N-дизамещенных – атомы водорода замещены двумя радикалами.
Амиды представляют собой кристаллические вещества с относительно высокими и четкими температурами плавления, что позволяет использовать некоторые из амидов в качестве производных для идентификации карбоновых кислот.
Кислотно-основные свойства.
Амиды обладают слабыми как кислотными, так и основными свойствами. Причиной пониженной основности аминогруппы в амидах является сопряжение неподеленной пары электронов атома азота с карбонильной группой. При взаимодействии с сильными кислотами амиды протонируются по атому кислорода как в разбавленных, так и в концентрированных растворах кислот. Такого рода взаимодействие лежит в основе кислотного катализа в реакциях гидролиза амидов:
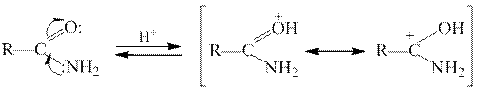
Незамещенные и N-замещенные амиды проявляют слабые NH-кислотные свойства, сравнимые с кислотностью спиртов (значения рКа большинства амидов находятся в пределах 15,1-19,0) и отщепляют протон только в реакциях с сильными основаниями.
Кислотно-основное взаимодействие лежит в основе образования амидами межмолекулярных ассоциатов, существованием которых объясняются высокие температуры плавления и кипения амидов. Возможно существование двух типов ассоциатов: линейных полимеров и циклических димеров.
Реакции ацилирования.
Вследствие наличия в сопряженной системе амидов сильной электронодонорной аминогруппы электрофильность карбонильного атома углерода, а следовательно, и реакционная способность амидов в реакциях ацилирования очень низкая. Низкая ацилирующая способность амидов объясняется также и тем, что амид-ион NH2- - плохо уходящая группа. Из числа реакций ацилирования практическое значение имеет гидролиз амидов, который можно проводить в кислой и щелочной средах. Амиды гидролизуются намного труднее, чем другие функциональные производные карбоновых кислот. Гидролиз амидов проводится в более жестких условиях по сравнению с гидролизом сложных эфиров.
Кислотный гидролиз амидов – необратимая реакция, приводящая к образованию карбоновой кислоты и аммониевой соли:
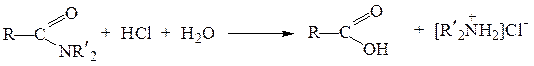
В большинстве случаев кислотный гидролиз амидов протекает по механизму бимолекулярного кислотного ацилирования, т.е. во многом похож на механизм кислотного гидролиза сложных эфиров. Необратимость реакции обусловлена тем, что аммиак или амин в кислой среде превращаются в ион аммония, не обладающий нуклеофильными свойствами.
Щелочной гидролиз тоже необратимая реакция; в результате её образуется соль карбоновой кислоты и аммиак или амин:
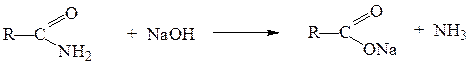
Щелочной гидролиз амидов, как и гидролиз сложных эфиров, протекает по тетраэдрическому механизму.
Дата добавления: 2019-02-12; просмотров: 107; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
