ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
ЦЕЛЬ. Экспериментальное определение универсальной газовой постоянной и постоянной Больцмана.
ОБОРУДОВАНИЕ. Лабораторный комплекс ЛКТ-1; баллон с резиновым шлангом и зажимом; весы с разновесами; соединительные силиконовые шланги.
КРАТКАЯ ТЕОРИЯ
Давление Р,оказываемое газом на стенки сосуда, обусловлено тем, что молекулы при своем хаотическом движении сталкиваются не только друг с другом, но и со стенками сосуда. Эти столкновения определяют силу, испытываемую стенкой со стороны газа. Средняя сила, действующая на единицу площади, и есть давление. Давление газа будет тем больше, чем больше концентрация молекул и скорость их теплового движения. Следовательно, такой макроскопический параметр газа, каким является давление, зависит от поведения отдельных молекул, т.е. от микроскопических параметров теплового движения. Количественная связь между давлением газа и микроскопическими параметрами молекул устанавливается в молекулярно-кинетической теории идеальных газов. Основное уравнение МКТ имеет вид:
 , (1)
, (1)
где n - число молекул в единице объема,
<v2> - среднее значение квадрата скорости молекул.
Одной из важных величин, характеризующих макросистему, является энергия U. В случае идеального газа, состоящего из N атомов, совершающих поступательное хаотическое движение,
 , (2)
, (2)
где <E> - средняя кинетическая энергия поступательного движения одной молекулы,
N – число молекул в атоме,
m о - масса одной молекулы.
Поскольку энергия есть величина аддитивная, U является функцией объема V . Заметим, что давление  . Действительно, с учетом (2) выражение (1) можно переписать:
. Действительно, с учетом (2) выражение (1) можно переписать:
 (3)
(3)
Средняя кинетическая энергия движения молекул определяет другой важный параметр состояния газа - температуру Т. Как известно, средняя энергия молекулы одноатомного идеального газа равна:
 (4)
(4)
где k - коэффициент пропорциональности, устанавливающий связь между температурой, выраженной в единицах энергии (джоули), и температурой, выраженной в градусах. Коэффициент k называется постоянной Больцмана. Подставим (4) в (3), находим:

откуда:  (5)
(5)
Мы получили уравнение классического идеального газа. Оно связывает давление, объем и температуру газа. Так как в уравнение (5) не входит никакой величины, характеризующей природу конкретного газа, то оно пригодно для любых классических идеальных газов (при выводе мы пренебрегли взаимодействием атомов, лишив тем самым газ его "индивидуальности").
Получим уравнение состояния для 1 моля идеального газа. В одном моле газа содержится атомов

Указанное число N А называют постоянной Авогадро. Тогда для 1 моля уравнение (5) примет вид:
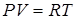 , (6)
, (6)
где R = NА. k - называют универсальной газовой постоянной. Она имеет размерность [Дж/моль·К].
Для произвольной массы газа уравнение (5) принимает вид:
 , (7)
, (7)
где m - масса взятого газа,
 - его молярная масса.
- его молярная масса.
В данной работе предлагается использовать уравнение (7) для экспериментального определения универсальной газовой постоянной.
МЕТОДИКА ЭКСПЕРИМЕНТА
В баллоне объемом V при комнатной температуре Т находится воздух массой m1. Давление воздуха - Р1, оно равно атмосферному (~ 105 Па). Состояние газа в баллоне описывается уравнением:
 . (8)
. (8)
Будем медленно накачивать воздух в баллон, увеличивая давление газа до Р2. В новом состоянии уравнение (7) будет иметь вид:
 , (9)
, (9)
где m2 - масса газа в баллоне в новом состоянии.
При медленном накачивании процесс протекает изотермически вследствие
теплообмена с окружающей средой. Таким образом, можно считать, что:
 . (10)
. (10)
Объем баллона также остается неизменным
 . (11)
. (11)
Решая совместно (8) и (9) с учетом (10) - (11), находим:
 (12)
(12)
Получим искомую рабочую формулу
 (13)
(13)
Определив экспериментально газовую постоянную R, можно вычислить постоянную Больцмана:
 (14)
(14)
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
Внимание: Перед выполнением работы ознакомьтесь с устройством лабораторного комплекса ЛКТ-1, принципом работы газогенератора и его измерительной системы (см. инструкцию).
1. При помощи силиконовых шлангов произведите соединение в газогенераторе, по схеме с манометром высокого давления (см. инструкцию).
2. Определите взвешиванием массу m1 баллона объемом V , внутри которого воздух при атмосферном давлении P1.
3. Подключите баллон объемом V1 = 2,05 л к компрессору с манометром M1. (Наденьте шланг баллона на штуцер над указателем [К]). Включите тумблер питания. Кран компрессора должен находиться в положении "закрыто".
4. Вращая ручку плавной регулировки, медленно повышайте давление воздуха. За изменением давления следите по манометру. Шкала манометра проградуирована в миллиметрах ртутного столба. Давление ∆P = 300 мм рт.ст. соответствует 40 кПа. Манометр показывает разницу между атмосферным давлением и давлением в баллоне - ∆P.
5. Доведите дополнительное давление до значения ∆P = 150 мм.рт.ст. Закройте кран на шланге баллона. Вновь произведите взвешивание баллона. Новое значение давления P2 = P1 + ∆P и массы m2 занесите в таблицу:
| m1 | m2 | V | T | P1 | 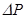
| P2 | R | 
|
6. Повторите пп.3-5, увеличивая ∆P до250-300 мм рт.ст. и производя измерения через каждые 50 мм рт.ст.
7. Произведите аналогичные измерения с баллонами другого объема (V2 = 1,55 л; V3 = 1,3 л).
8. Рассчитайте по формуле (13) универсальную газовую постоянную. Произведите статистическую обработку данных. Запишите результат в виде:
 .
.
Сравните полученный результат с табличными данными.
9. Используя экспериментальное значение R, вычислите по формуле
(14) постоянную Больцмана.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Сформулируйте основные положения молекулярно-кинетической
теории газов.
2. Выведите основное уравнение МКТ.
3. В чем заключается физический смысл давления и температуры газа с точки зрения молекулярно-кинетической теории?
4. Выведите формулу (7).
5. Какой физический смысл имеет постоянная Больцмана?
6. Как можно определить объем сосуда по изменению давления в нем за счет увеличения числа молекул газа?
7. Выведите рабочую формулу (13).
ЛИТЕРАТУРА
[1] §§ 7- 9, 59; [3] §§ 5,7-11; [5] 1.16; [6] §§ 85-86.
ЛАБОРАТОРНАЯ РАБОТА № 2-03
Дата добавления: 2019-02-12; просмотров: 1664; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
