Аддитивный подход расчета физико-химических свойств углеводородных газов
Аддитивный подход расчета физико-химических свойств углеводородных газов
Нефтяной газ при нормальных условиях содержит неполярные углеводороды – смесь углеводородов от С1 до С4: метан, этан, пропан, изо-бутан и н-бутан. С точки зрения физики к газам можно применять законы для идеальных систем.
То есть нефтяной газ – это идеальная система.
С точки зрения химии – идеальным называется газ силами взаимодействия между молекулами которого можно пренебречь.
С точки зрения термодинамики идеальным называется газ, для которого справедливы равенства:
(∂Е / ∂V)T = 0, z = P·V/Q·R·T = 1, (2.8)
где Е – внутренняя энергия парообразования, Дж/моль;
z – коэффициент, характеризующий степень отклонения реального газа от закона идеального газа.
С точки зрения математики – это аддитивная система. Следовательно, для оценки свойств нефтяного газа (при нормальных или стандартных условиях) применимы аддитивные методы расчётов физико-химических и технологических параметров (Псмеси):
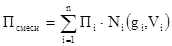 , (2.9)
, (2.9)
где Ni – мольная доля;
gi – весовая доля;
Vi – объёмная доля;
Пi – параметр i-го углеводорода или неуглеводородного компонента.
Аддитивный подход к расчёту физико-химических и технологических параметров означает, что каждый компонент газа в смеси ведет себя так, как если бы он в данной смеси был один.
Для идеальных газов давление смеси газа равно сумме парциальных давлений компонентов (закон Дальтона):
|
|
|
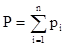 , (2.10)
, (2.10)
где Р – давление смеси газов;
рi – парциальное давление i-го компонента в смеси,
или
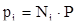 , (2.11)
, (2.11)
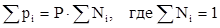 . (2.12)
. (2.12)
То есть парциальное давление газа в смеси равно произведению его молярной доли в смеси на общее давление смеси газов.
Аддитивность парциальных объёмов (Vi) компонентов газовой смеси выражается законом Амага:
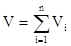 , (2.13)
, (2.13)
где V – объём смеси газов;
Vi – объём i-го компонента в смеси.
или аналогично уравнениям 2.11–2.12 объём компонента газа можно оценить:
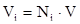 . (2.14)
. (2.14)
Как аддитивную величину рассчитывают и плотность смеси газов:
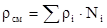 , (2.15)
, (2.15)
где сi – плотность i–го компонента;
Ni – мольная доля i–го компонента.
Молекулярная масса смеси рассчитывается по принципу аддитивности для смесей, состав которых выражен в мольных или объёмных долях по формуле 2.14 (левое выражение). Для смесей, состав которых выражен в массовых процентах по формуле 2.14 (правое выражение):
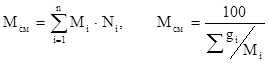 . (2.16)
. (2.16)
Рассмотрим пример. При приготовлении рекомбинированной пробы смешивают следующие объёмы (V) газов: 100 м3 пропана (C3H8), 75 м3 изобутана (i-С4Н10) и 75 м3 нормального бутана (n-С4Н10).
|
|
|
Найти молекулярную массу смеси (Мсм).
Дано: Vi , м 3 Mi , кг/моль
C3H8 100 44
i-C4H10 75 58
n-C4H10 75 58
Решение. Находим общий объём газовой смеси: 100+75+75=250 (м3), и рассчитываем ее состав в объёмный процентах:
250 м3 – 100 %,
100 м3 – Х %;
Х = 100100 / 250 = 40 (%) или VC3H8 = 0,4 (в долях);
i-C4H10 – X % X = 75100 / 250 = Vi-C4H10 = 30 % = 0,3 (в долях);
n-C4H10 – 30 % Vn-C4H10 = 30 % = 0,3 (в долях).
Зная, что Vi = Ni, и зная молекулярные массы компонентов смеси: C3H8 – 44; C4H10 – 56, рассчитаем величину Mсм:
Mсм = MiNi = 440,4 + 580,3 + 580,3 = 17,6 + 17,42 = 52,4 (кг/моль).
Уравнение состояния
Уравнение состояния
Для определения многих физических свойств природных газов используется уравнение состояния.
Уравнением состояния называется аналитическая зависимость между параметрами, описывающими изменение состояние вещества. В качестве таких параметров используется давление, температура, объём.
Состояние газа при нормальных и стандартных условиях описывается уравнением Менделеева–Клапейрона:
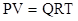 , (2.17)
, (2.17)
где Р – абсолютное давление, Па;
V – объём, м3;
Q – количество вещества, кмоль;
Т – абсолютная температура, К;
|
|
|
R – универсальная газовая постоянная, Па×м3/(кмоль×град).
На основе уравнения состояния газа можно рассчитать много параметров для системы нефтяного газа: плотность, мольный объём, количество молекул, число молекул, парциальные давления и др., если рассматривать уравнение состояния газа для 1 моля, т.е., Q = 1 моль. С учетом этого, уравнение состояния газа можно преобразовать следующим образом:
P·V = ∑N·R·T. (2.18)
При ∑N = 1 моль, следует, что: P·V = R·T. Зная, что масса (m) одного моля идеального газа равна его молекулярной массе (М), умножив левую и правую части на молекулярную массу и массу газа, соответственно получим:
P·V·M = m·R·T. (2.19)
Поделив обе части на V·R·T: и преобразовав 2.19, получим выражение для расчета плотности:
P·M / R·T = m / V, m / V = M·P / R·T r = M·P / R·T. (2.20)
Рассмотрим пример. Дан один моль метана CH4.
Найти его плотность?
Решение. Зная, что молекулярная масса метана равна 16 г/моль и метан занимает объём при н.у. = 22,414 л, а при с.у. = 24,055 л, найдем:
1. rCH4 (н.у.) = 16/22,414 = 0,717 (г/л);
2. rCH4 (с.у.) = 16/24,055 = 0,665 (г/л).
Плотность смеси газовых компонентов рассчитывают с учетом средней молекулярной массы смеси газа (Mсм), как отношение его молекулярной массы к его мольному объёму (Vм). Например, при нормальных условиях (н.у.) она будет рассчитываться по выражению:
|
|
|
rсм = Mсм / 22,414. (2.21)
Из расчетов и из выражений 2.20, 2.21 следует, что плотность газа с возрастанием температуры будет уменьшаться, а с возрастанием давления (2.20) будет расти.
Рассмотрим другой пример. Определить плотность метана СН4 при избыточном давлении, например при давлении 3,5 атм и температуре 0°С. Решение. В этом случае общее давление в системе будет равно:
Р = (3,5 + 1) = 4 (атм).
Зная, что молекулярная масса метана = 16 г/моль, универсальная газовая постоянная (R) = 0,08206 атмл/(Кмоль), а температура (T) = 273,15 К, найдем плотность метана:
rCH4 = Р·М / R·T = (3,5 + 1)·16 /0,08206 ·273,15 = 3,21 (г/л).
Относительная плотность газов рассчитывается по отношению к плотности воздуха, определенного при тех же условиях:
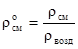 . (2.22)
. (2.22)
При нормальных условий (н.у.) плотность воздуха (свозд) » 1,293; при стандартных условий (с.у.) - свозд » 1,205.
Если плотность газа (со) задана при атмосферном давлении = 0,1013 МПа, то пересчёт её на другое давление (Р) при той же температуре для идеального газа производится по формуле:
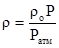 . (2.23)
. (2.23)
Рассмотрим пример. Для условий задачи, рассмотренной выше (см. пример раздела 2.2) можно рассчитать абсолютные (r) и относительные (сосм) плотности смеси, используя правое выражение (2.16) для расчета молекулярной массы:
Мсм = 100 / (36,5 / 16 +17,2 / 30 +19,8 / 44 +14,7 / 58 +11,8 / 72)
= 26,874 (кг/кмоль);
rcv = 26,874 / 22,41 = 1,119 (кг/м3);
сосм (н.у.) = 1,119 / 1,293 = 0,927.
Аналогично из (2.20) находится и выражение для мольного объёма:
V = R ·T / P. (2.24)
Отсюда, мольный объём при давлениях равному 1 атм или близких к атмосферному и для физических процессов, когда не происходит изменения числа молей в системе оценивается соотношением:
V = R·T, (2.25)
где R – универсальна газовая постоянная, R = 0,08206 атм·л/(К·моль);
Т – температура, К;
Рассмотрим пример. Найти вид зависимости изменения мольного объёма газа от температуры V = f(T).
Решение. Воспользуемся выражением 2.25 и получим объём, занимаемый одним молем идеального газа при условиях задачи:
Vн.у. = 0,08206273,15 = 22,414 (л),
Vс.у. = 0,08206293,15 = 24,055 (л).
Любой газ при нормальных условиях (н.у. Т = 0оС и Р = 760 мм рт. ст.) занимает объём равный 22,414 м3, а при стандартных (с.у. Т = 20 оС и Р = 760 мм рт. ст.) объём равный 24,055 м3.
С увеличением температуры мольный объём газа увеличивается. Мольный объём газов с возрастанием температуры будет расти, а с возрастанием давления (см. 2.24) уменьшаться.
У этого уравнения есть свои граничные условия. Оно справедливо для описания поведения газов при давлениях близких к атмосферному (от 1 до 10–12 атм) и при температурах до 20оС. При повышенном давлении газ сжимается и его состояние отличается от поведения идеальных газов.
Состояние реальных газов
Состояние реальных газов
При повышенных давлениях для реальных газов характерно межмолекулярное взаимодействие, молекулы газов начинают притягиваться друг к другу, за счет физического взаимодействия.
Для учёта этого взаимодействия уравнение 2.17 на протяжении многих лет модифицировалось (голландским физиком Ван–дер–Ваальсом и др.). Однако на практике используется уравнениеМенделеева–Клапейрона для реальных газов, содержащее коэффициент сверхсжимаемости z, предложенный Д. Брауном и Д. Катцом и учитывающий отклонения поведения реального газа от идеального состояния:
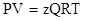 , (2.26)
, (2.26)
где Q – количество вещества, моль;
z – коэффициент сверхсжимаемости газа (см. 2.8).
Физический смысл коэффициента сверхсжимаемости заключается в расширении граничных условий уравнения Менделеева–Клапейрона для высоких давлений.
Коэффициент z зависит от давления и температуры (приведенных, критических давлений и температур), природы газа:
z = f (Тприв, Рприв), (2.27)
где Тприв – приведенная температура;
Рприв – приведенное давление.
Приведёнными параметрами индивидуальных компонентов называются безразмерные величины, показывающие, во сколько раз действительные параметры состояния газа (температура, давление, объём, плотность и др.) больше или меньше критических.
Тприв.. = Тпл. / Тср. кр; Р прив. = Рпл. / Рср. кр; Vприв. = Vпл. / Vср. кр. (2.28)
А для смесей газов они характеризуются отношением действующих параметров (температура, давление и др.) к среднекритическим параметрам смеси:
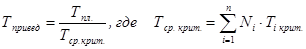 (2.29)
(2.29)
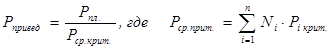 (2.30)
(2.30)
Критическая температура – температура, при которой жидкий углеводород переходит в газообразное состояние (табл. 2.4.).
Критическое давление – давление, при котором газообразный углеводород переходит в жидкое состояние (табл. 2.4).
Таблица 2.4
Дата добавления: 2019-02-12; просмотров: 839; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
