Указать роль буферных систем в организме?
1) для повышения рН среды 2) для понижения рН среды
3) для поддержания рН среды 4) для ускорения биохимических реакций
У какой буферной системы организма самая большая буферная ёмкость?
1) фосфатной 2) белковой
3) гемоглобиновой 4) бикарбонатной
Алкалоз - это
1) смещение рН крови в кислую область
2) смещение рН желудочного сока в щелочную область
3) смещение рН крови в щелочную область
4) смещение рН желчи в кислую область
Ацидоз - это
1)  смещение рН крови в кислую область
смещение рН крови в кислую область
2) смещение рН желудочного сока в кислую область
3) смещение рН крови в щелочную область
4) смещение рН желчи в кислую область
Укажите формулу бикарбонатного буфера
1) CH3COONa/CH3COOH
2) Na2HPO/NaH2PO4
3) NaHCO 3/ H2 CO3
4) NH4OH/NH4Cl
51. Какая буферная система входит в состав организма:
1) CH3COONa/CH3COOH
2) Na2 HPO / NaH 2 PO4
3) NH4OH / NH4Cl
4) HCOOK / HCOOH
5) ХИМИЧЕСКАЯ КИНЕТИКА
1. При 0 °С гранула железа растворяется в соляной кислоте за 20 мин. Если температурный коэффициент реакции равным 2, то такой же по массе кусочек железа растворится при 20 °С за _____ минут.
1) 5 2) 12 3) 60 4) 10
2. Если температурный коэффициент скорости химической реакции равен 2, то при повышении температуры от 200С до 500С скорость реакции …
1) увеличивается в 8 раз 2) уменьшается в 2 раза
3) увеличивается в 6раз 4) уменьшается в 4 раза
3. Температурный коэффициент реакции равен 3. Во сколько раз увеличивается скорость реакции при повышении температуры на 200С
1) в 1,5 раза 2) в 3 раза
3) в 6 раз 4) в 9 раз
4. Кинетическое уравнение для реакций I-го порядка имеет вид:
1) 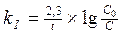
2) 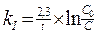
3) 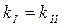
4) 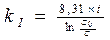
5. Кинетическое уравнение для реакций II-го порядка имеет вид:
1) 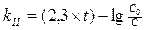
2) 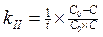
3) 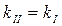
4) 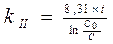
6. Согласно закону Вант-Гоффа при повышении температуры на 10ºС скорость химической реакции возрастет в:
1) 5-6 раз 2) 2-4 раза 3) 10 раз 4) 1,75 раза
7. Энергия активации – это …
1) кинетическая энергия
2) потенциальная энергия
3) энергия, образующаяся при столкновении молекул
4) избыточная энергия, которую необходимо передать 1 моль вещества, чтобы перевести все молекулы в активное состояние
8. Как изменится скорость химической реакции при увеличении температуры на 20ºС, при температурном коэффициенте равном 4
1) возрастет в 16 раз
2) уменьшится в 2 раза
3) сначала увеличится в 3 раза затем уменьшится в 1,5 раза
4) не изменится
9. Катализаторы, ускоряющие скорость химической реакции называются …
1) ингибиторы 2) инициаторы
3) антиоксиданты 4) окислители
10. Принято выделять следующие виды катализа:
1) гомогенный 2) гетерогенный
3) мономолекулярный 4) нулевой
11. В организме роль катализаторов выполняют:
1) жирные кислоты 2) витамины
3) ферменты 4) ДНК и РНК
12. При увеличении температуры на 50ºС скорость химической реакции возрастет в 32 раза. Чему равен температурный коэффициент реакции?
1) ¾ 2) 8×10-2 3) 2 4) 5,08
13. Реакция разложения Н2О2 в водном растворе протекает как реакция I-го порядка. Период полураспада составляет 15,86 мин. Какое время потребуется для разложения 99% взятого количества Н2О2 – ?
1) 11 часов 2) 1 сутки
3) 50 мин 34 сек 4) 106,96 мин
14. При 60ºС вещество «Х» подвергается термическому разложению по уравнению I-го порядка с константой скорости 0,05 мин-1. Сколько времени нужно нагревать раствор при 60ºС, чтобы исходная концентрация вещества равная 0,1 моль/л уменьшилась до 0,01 моль/л – ?
1) 34 сек 2) 1 час 58 мин 3) 46 мин 4) 2 сут
Дата добавления: 2019-01-14; просмотров: 371; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
