Следствия из основного уравнения
Молекулярно-кинетической теории
Из основного уравнения молекулярно-кинетической теории можно:
- найти связь между давлением и средним значением кинетической энергии поступательного движения молекул;
- дать молекулярно-кинетическое толкование абсолютной температуры;
- определить значение среднеквадратичной скорости движения молекул.
Среднее значение кинетической энергии поступательного
Движения молекул
Умножим и разделим равенство (2.1.8) на 2.
 .
.
Средняя кинетическая энергия поступательного движения молекул:
 .
.
Тогда
 .
.
Вывод: давление газа пропорционально числу молекул и среднему значению кинетической энергии хаотического движения молекул и не зависит ни от формы, ни от размеров сосуда.
Молекулярно-кинетическое толкование температуры
Формула для определения давления газа:
 .
.
С другой стороны:
 .
.
Приравняв правые части, получим
 ,
,
откуда средняя кинетическая энергия поступательного движения молекул:
 .
.
Формула справедлива не только для газов, но и для вещества в любом состоянии. Эта формула замечательна в том отношении, что средняя кинетическая энергия хаотического движения молекул зависит только от абсолютной температуры и не зависит от массы молекулы.
Вывод: при одинаковой температуре средние кинетические энергии молекул различных веществ одинаковы, несмотря на различие масс.
Из последнего равенства:  , следовательно, температура тела есть количественная мера энергии теплового движения молекул, из которых состоит это тело.
, следовательно, температура тела есть количественная мера энергии теплового движения молекул, из которых состоит это тело.
Абсолютный нуль Т = 0 (  С) является такой температурой, при которой в теле прекращается тепловое (а не вообще) движение молекул (
С) является такой температурой, при которой в теле прекращается тепловое (а не вообще) движение молекул ( 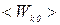 = 0) и остается движение частиц, связанное с нулевой энергией. Это означает, что при абсолютном нуле сохраняются некоторые виды движения внутри молекул и атомов (движение электронов, протонов, нейтронов), так что в целом внутреннее движение материи не прекращается и при абсолютном нуле. Абсолютный нуль является самой низкой из всех возможных температур.
= 0) и остается движение частиц, связанное с нулевой энергией. Это означает, что при абсолютном нуле сохраняются некоторые виды движения внутри молекул и атомов (движение электронов, протонов, нейтронов), так что в целом внутреннее движение материи не прекращается и при абсолютном нуле. Абсолютный нуль является самой низкой из всех возможных температур.
Вывод: нулем температуры в абсолютной шкале является температура, при которой тепловое движение молекул отсутствует.
Средняя квадратичная скорость
Средняя кинетическая энергия поступательного движения молекул:
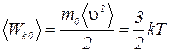 ,
,
откуда
 .
.
Средней квадратичной скоростью  называется корень квадратный из среднего квадрата скорости:
называется корень квадратный из среднего квадрата скорости:
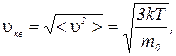
Учитывая, что  , а
, а  (молярная масса), то можно получить
(молярная масса), то можно получить

Мы получили расчетную формулу для определения среднеквадратичной скорости хаотического движения молекул.
Для одного и того же газа (m = const) с увеличением температуры средняя квадратичная скорость увеличивается. Для различных газов (  ) при одинаковой температуре Т средняя квадратичная скорость больше у молекул того газа, молекулярная масса которого меньше.
) при одинаковой температуре Т средняя квадратичная скорость больше у молекул того газа, молекулярная масса которого меньше.
При комнатной температуре 293 К для кислорода 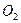 :
:
 м/с;
м/с;
для водорода  :
:
 м/с
м/с  км/с.
км/с.
Из приведённых примеров видно, что молекулы окружающего нас воздуха движутся со скоростью порядка скорости полёта пули.
Дата добавления: 2019-09-13; просмотров: 167; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
